随着现代工业的迅猛发展,化石燃料的大量燃烧,工业排放的SO2日益增加,随之带来的环境污染问题也日益严重。SO2是目前危害最大的大气污染源之一[1],当它进入大气环境并达到一定浓度后,不仅会对建筑物造成毁坏,致使土壤酸化,影响人体健康,甚至导致全球气候变化。经济的加速发展,煤炭的大量使用,导致粉煤灰(fly ash,FA)的排放量持续增加,进而导致一系列生态环境问题亟待解决,粉煤灰的传统利用方式简单且经济价值低。
为了控制SO2的超标排放,我国开展了多种脱硫剂的研究工作,并将其应用于实际工业,粉煤灰就是其中之一。魏先勋等[2]利用改性后的粉煤灰吸附低浓度SO2,发现改性粉煤灰在控制相对湿度为30%,烟气量为200 L/h,混合气体流量中SO2的质量浓度为5.1 g/m3时,脱硫效果优于市售一级活性炭;蒋历辉等[3]以粉煤灰、Ca(OH)2、活化剂为主要原材料制备了脱硫率可高达93%粉煤灰负载的高效钙基脱硫剂;崔同明等[4]利用Na2CO3和Ca(OH)2对粉煤灰进行改性,并进行模拟烟气脱硫,探究其脱硫机制,发现高温下粉煤灰与Na2CO3熔融煅烧会释放出无定型SiO2、Al2O3等,随即与Ca(OH)2水合消化生成比表面积较大的多孔晶体水合硅酸钙、水合铝酸钙、水合硅铝酸钙,此类产物可用于脱硫。上述粉煤灰的改性利用均是在水热条件下发生火山灰反应得到新产物而实现的。粉煤灰中含有一种特殊的微珠,按其结构性质可以分为漂珠(floating bead,FB)、沉珠(sink bead,SB)、磁珠(magnetic bead,MB),其中沉珠的质量分数高达40%[5],其成分与粉煤灰基本相似,二者均以SiO2、Al2O3、CaO等为主。沉珠中所含的活性SiO2、Al2O3相对于常规粉煤灰而言更高,且其火山灰活性高于常规粉煤灰[6]。因为我国各地区燃烧煤的种类及燃烧方式的不同,所以各火电厂产生的粉煤灰中沉珠的含量各不相同,有的几乎没有,有的含量较高[7],且当前学者对沉珠鲜有研究,其应用范围也十分有限。进一步深入开展对沉珠性质的研究,拓展沉珠的应用范围,对大气环境保护具有重要的实际意义。本研究通过物理化学法对沉珠进行改性,利用自建的干法烟气脱硫试验台,对比分析改性沉珠与传统Ca(OH)2脱硫剂吸附脱除SO2的效率,并探究改性沉珠对吸附脱除SO2效率的影响。
1 实验
1.1 原料
粉煤灰沉珠(汇丰新材料有限公司),无水碳酸钠(分析纯,天津市登峰化学试剂有限公司),氢氧化钙(分析纯,天津市登峰化学试剂有限公司),蒸馏水(实验室自制)。粉煤灰沉珠主要化学组分见表1。
表1 沉珠的化学组分
Tab.1 Chemical components of sink beads

组分SiO2Al2O3Fe2O3CaOTiO2K2O烧失物质量分数/%59.4631.533.841.191.311.281.39
1.2 装置
实验装置包括模拟烟气、烟气预处理、烟气分析处理、管式反应炉和剩余烟气回收装置等5部分。模拟烟气装置包括气瓶(N2、O2、SO2)、电子流量控制器和烟气混合塔。将模拟烟气的体积流量调节至700 mL/min,其中SO2的质量浓度为850 mg/m3,O2的质量分数为12%(根据中国环境科学研究院提供的数据分析,脱硫塔内气体中O2的质量分数为11.2%~18.5%)[8];气体前处理装置包括高精度水泵和水蒸气发生器;烟气分析处理装置为粉尘过滤系统、防倒吸干燥器和烟气分析仪(崂应3012H-D 型烟气分析测试仪);烟气反应装置由滤料吸附反应器、脱硫剂以及固定管式炉组成;尾气回收装置为盛装NaOH水溶液的集气瓶,用于吸收未完全反应的硫氧化物。根据脱硫塔前后出口SO2浓度计算脱硫率
(1)
式中:η为脱硫效率,%;ρ0为SO2的初始质量浓度,本实验设定为850 mg/m3;ρt为脱硫塔后端出口SO2质量浓度,mg/m3。
2 沉珠的改性
沉珠的主要成分为SiO2、Al2O3、Fe2O3、CaO、TiO2、K2O等[9],其中SiO2和Al2O3在改性过程中能够提供大量的活性点,有利于其对SO2的吸附。原状粉煤灰沉珠本身是具有稳定晶格结构的玻璃体,其活性物质被包裹固定在玻璃体内部,不能有效释放,无法充分利用。
本实验中向沉珠加入助熔剂(Na2CO3),在850 ℃下煅烧熔融,目的是破坏沉珠稳定的晶格结构,使其将无定型SiO2和Al2O3等释放出来,增强沉珠的活性,从而提升沉珠的利用率;然后向熔融后的产物中加入Ca(OH)2,进行水合消化,使其发生如下水热化合反应:
xCa(OH)2+ySiO2+(z-1)H2O→(CaO)x(SiO2)y(H2O)z,
(2)
xCa(OH)2+yAl2O3+(z-1)H2O→(CaO)x(Al2O3)y(H2O)z,
(3)
xCa(OH)2+yAl2O3+zSiO2+(w-1)H2O→(CaO)x(Al2O3)y(SiO)z(H2O)w。
(4)
反应生成水合硅酸钙、水合铝酸钙、水合硅铝酸钙等有较大比表面积的多孔晶体物质,此类物质可以提升脱硫效率,具体反应式为
(CaO)x(Al2O3)y(SiO2)z(H2O)w+mSO2→(CaO)(x-m)(Al2O3)y(SiO2)z(CaSO4)m(H2O)w,
(5)
式中的x、y、z、w、m可取任意值[10]。由以上反应式可以看出,水化期间SiO2的释放情况对脱硫剂的活性有很大的影响[11]。
3 结果与分析
3.1 X射线衍射图谱分析
对改性沉珠和原状沉珠进行X射线衍射(XRD)图谱分析,结果见图1。其中原状沉珠中富含SiO2、Al2O3,沉珠经过高温煅烧及添加氢氧化钙水合改性后,生成较多的水合硅酸钙((CaO)x(SiO2)y(H2O)z)、水合铝酸钙((CaO)x(Al2O3)y(H2O)z)、水合硅铝酸钙((CaO)x(Al2O3)y(SiO2)z(H2O)w)等有较大比表面积的多孔晶体物质,有利于提升脱硫效率。
3.2 扫描电镜表征
通过扫描电镜(SEM)表征原状沉珠、改性沉珠和Ca(OH)2的形貌,结果如图2、3所示。图2(a)、3(a)分别为放大5 000、10 000倍的原状沉珠,由图可知,原状沉珠呈现不规则的粉珠状,以表面光滑的球形颗粒和玻璃质颗粒为主,颗粒表面较为致密,孔洞较少,比表面积小。图2(b)、3(b)分别为放大5 000、10 000倍的改性沉珠,从图可以看出,改性后的沉珠完全看不到初始形貌,在5 000倍时能看到颗粒表面呈现明显规律性的絮状结构,10 000倍下观察到颗粒表面错综复杂,分布散乱,饱含多孔蓬松的网络架构。图2(c)、图3(c)分别为放大5 000和10 000倍的Ca(OH)2,由图可以观察到,Ca(OH)2呈现规律的絮状与片状结构。对比分析三者的形貌可以得出,改性后的沉珠表面孔洞与比表面积明显增大,为SO2的吸附脱除提供了更优的物理条件。
3.3 比表面积对比
通过比表面积分析仪对沉珠、改性沉珠2组样品进行测试,结果如表2所示。由表可知,改性沉珠的峰面积约为沉珠峰面积的6.5倍,改性沉珠的比表面积约为沉珠比表面积的6.3倍。说明向沉珠加入助熔剂(Na2CO3)煅烧,然后向熔融后的产物中加入Ca(OH)2,进行水合消化并发生水热化合反应后,生成的物质比表面积大于原状沉珠,为其吸附脱除SO2提供了更大的空间。
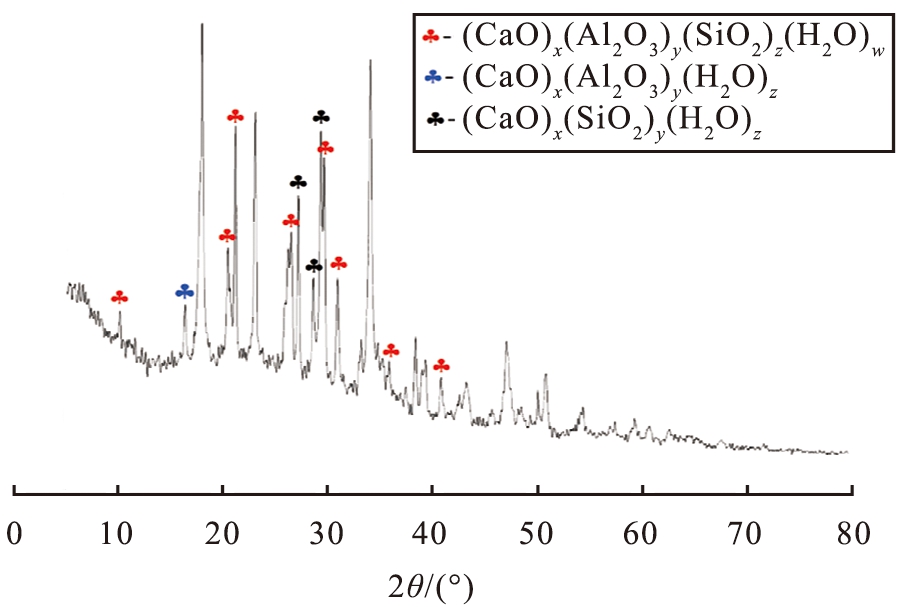
(a)改性沉珠
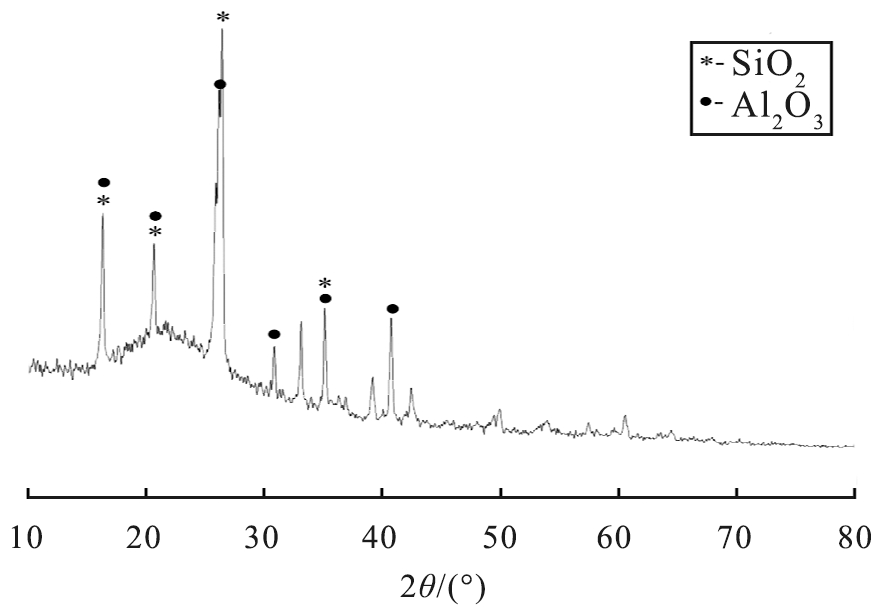
(b)原状沉珠
图1 原状沉珠与改性沉珠的XRD图谱
Fig.1 XRD analysis of undisturbed and modified sink beads


表2 沉珠与改性沉珠的比表面积
Tab.2 Specific surface area of sink beads and modified sink beads

样品质量/mg峰面积/(mV·min)比表面积/(m2·g-1)沉珠1144460320.5247改性沉珠1144297317.813.3254
3.4 脱硫效率对比
选取Ca(OH)2、改性沉珠2组样品进行脱硫评价,实验结果如图4所示。图4(a)反映了二氧化硫出口浓度随脱硫时间的变化情况。图4(b)反映了脱硫剂的脱硫效率与脱硫时间的关系。从图中可以看出,在烟气脱硫中,改性沉珠与Ca(OH)2均表现出随着反应时间的增加,出口SO2浓度逐渐增加,脱硫效率逐渐降低的趋势,但可以明显看出,改性沉珠的脱硫效果远优于Ca(OH)2。
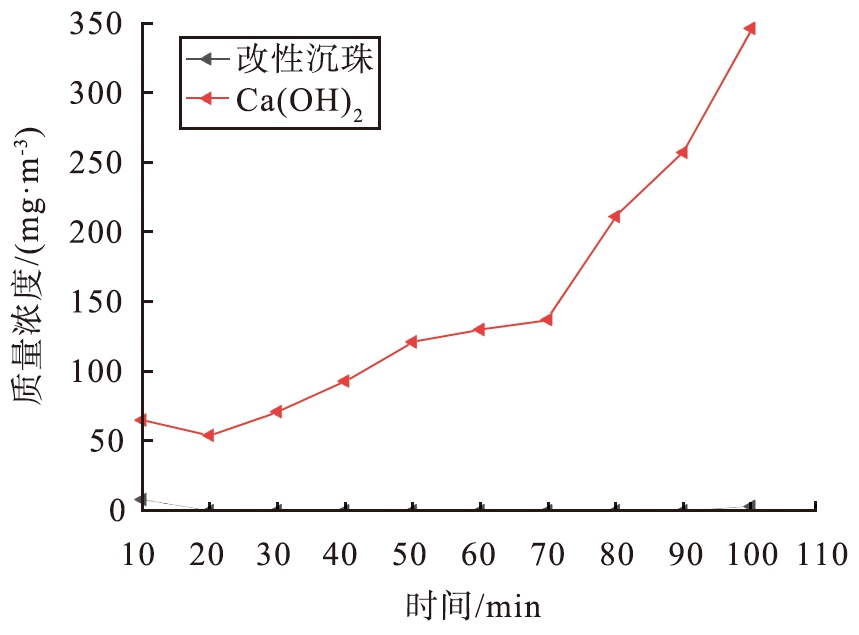
(a)SO2出口浓度
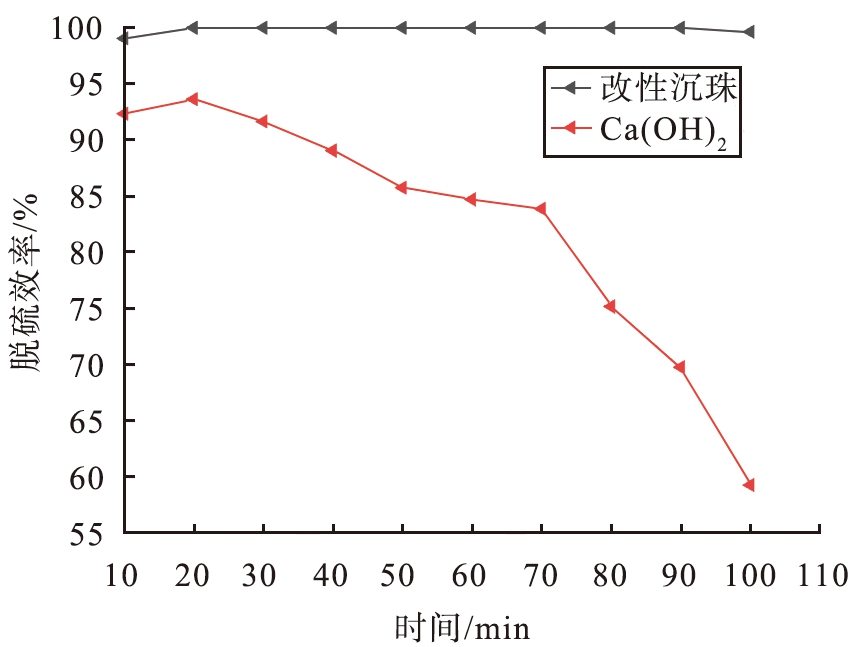
(b)脱硫效率
图4 改性沉珠、Ca(OH)2模拟烟气脱硫效果随时间的变化情况
Fig.4 Change of modified sink beads and Ca(OH)2 simulated flue gas desulfurization with time
由图4(a)可以看出,脱硫剂的种类在脱硫时对出口SO2浓度的影响比较显著,反应前10 min出口SO2浓度较高,10 min后出口SO2浓度呈现先降低后升高的趋势。这是因为在脱硫反应初期炉内相对湿度不稳定,相对湿度在反应进行一段时间后才稳定在30%。将反应时间设定为100 min,结合图4(a)、4(b)可以发现,随着反应时间的增加,Ca(OH)2作为脱硫剂的脱硫效率有明显的下降趋势,出口SO2浓度在20~70 min呈现缓慢升高,70 min后急速升高,当反应进行到100 min时脱硫效率降至59.29%;而改性沉珠作为脱硫剂时脱硫效率更为稳定,出口SO2浓度在10~90 min均为0,脱硫率为100%的反应时间持续了80 min,当反应进行到100 min时脱硫率仍高达99.65%。由此可以得出,改性沉珠的脱硫效果远优于Ca(OH)2。
4 讨论
1)本实验采用沉珠煅烧-水热化合改性,在高温煅烧时沉珠内部的Si—O、Al—O、≡Si—Al≡、≡Si—Si≡之间的化学键能减弱,使其与Na2CO3反应生成大量Na2SiO3、NaO·Al2O3·2SiO2等具有强烈活性的物质,一方面增大了沉珠后期在Ca(OH)2溶液中的溶解度,另一方面有利于后期水热化合改性实验。孔隙结构是影响脱硫效率的主要因素[12],水热化合改性过程改善了沉珠的表面孔隙结构,生成了水合硅酸钙、水合铝酸钙、水合硅铝酸钙等活性物质,为改性沉珠吸附脱除SO2提供了更多活性点。
2)熔融煅烧时加入的Na2CO3在高温下能分解放出CO2气体,在一定程度上CO2对沉珠具有“发泡”的效果,使得煅烧后的沉珠更加疏松多孔,经水热化合后生成的水合硅酸钙为粗大纤维状凝胶体[13],改性沉珠的扫描电镜图呈现的纤维状与之吻合,其复杂的物理表面特性有助于提升改性沉珠的脱硫效率。
3)沉珠经改性后生成了水合硅酸钙、水合铝酸钙、水合硅铝酸钙等多孔晶体物质,此类物质均呈现纤维状。这些具有网络结构的水化产物的形成,使改性沉珠颗粒表面变得更加粗糙多孔,增大了改性沉珠的比表面积。吸附SO2是在气、固两相界面上进行的,比表面积大,相界面就大,有效分子碰撞概率随之增大,从而吸附速率也越快。
4)传统Ca(OH)2脱硫剂吸附脱除SO2是利用其化学特性,使Ca2+与SO2反应生成CaSO4从而达到脱硫目的。Ca(OH)2脱硫效率低可能是因为SO2与Ca(OH)2的反应发生在Ca(OH)2外表面,生成的CaSO4堵塞了Ca(OH)2的微孔,使其内表面无法反应[14]。但在本实验中,将Ca(OH)2作为沉珠的改性激发剂与沉珠中大量活性SiO2、Al2O3发生火山灰反应,生成比表面积更大、活性更强的产物,既可以利用其多孔结构和较大的比表面积对SO2进行物理吸附,又可以利用其特殊的化学性质对SO2进行化学吸附,使得改性沉珠实现高效率脱硫。
5 结论
通过对沉珠进行物理化学改性,生成了有利于提升吸附脱除烟气中SO2效率的多孔晶体物质,对改性前后沉珠的物化性质进行对比分析,并分析比较Ca(OH)2、改性沉珠的脱硫效率,得出以下结论:
1)对比分析沉珠、改性沉珠的XRD图谱,表明原状沉珠经水热化合改性后生成了水合硅酸钙、水合铝酸钙、水合硅铝酸钙等产物,其较大的比表面积与多孔性质有利于提升烟气脱硫效率。
2)通过对沉珠、改性沉珠的SEM图像分析对比得出,原状沉珠以表面光滑的球形颗粒和玻璃质颗粒为主,颗粒表面较为致密,孔洞较少,比表面积小,而改性沉珠颗粒表面错综复杂,分布散乱,饱含多孔蓬松的网络架构,为吸附SO2提供了优异的物理条件。
3)测试沉珠、改性沉珠的比表面积发现,改性后的沉珠的比表面积约为原状沉珠比表面积的6.3倍,表明此物理化学改性增大了沉珠的比表面积,提升了吸附脱除SO2的利用率。
4)在本实验条件下,对比分析100 min内Ca(OH)2与改性沉珠作为脱硫剂的脱硫效率,结果发现改性沉珠的脱硫效果远优于Ca(OH)2。当反应进行到100 min时,改性沉珠脱硫率仍高达99.65%,而Ca(OH)2的脱硫率降至59.29%,且改性沉珠达到100%脱硫效率的运行时间为80 min。
[1]黄利华,张腾祥,郎莹婕,等.硅钙渣用于烟气脱硫的可行性[J].环境工程学报,2017,11(8):4696-4700.
HUANG L H,ZHANG T X,LANG Y J,et al.Feasibility of using silicon calcium slag for flue gas desulfurization[J].Chinese Journal of Environmental Engineering,2017,11(8):4696-4700.
[2]魏先勋,楚凯锋,翟云波,等.改性粉煤灰脱除二氧化硫的实验研究[J].湖南大学学报(自然科学版),2004(4):77-80.
WEI X X,CHU K F,ZHAI Y B,et al.Experimental study on sulfur dioxide removal by modified fly ash[J].Journal of Hunan University (Natural Science Edition),2004(4):77-80.
[3]蒋历辉,曾智文,唐新村,等.粉煤灰负载的钙基脱硫剂的制备[J].广州化工,2009,37(9):86-88.
JIANG L H,ZENG Z W,TANG X C,et al.Preparation of calcium based desulfurizer supported by fly ash[J].Guangzhou Chemical Industry,2009,37(9):86-88.
[4]崔同明,李水娥,李慧赢.粉煤灰的改性及从模拟烟气中吸附脱除SO2试验研究[J].湿法冶金,2017,36(3):234-237.
CUI T M,LI S E,LI H Y.Experimental study on modification of fly ash and adsorption of SO2 from simulated flue gas[J].Hydrometallurgy,2017,36(3):234-237.
[5]杜杰,欧阳平,张贤明,等.粉煤灰分选研究进展[J].应用化工,2020,49(7):1851-1856.
DU J,OUYANG P,ZHANG X M,et al.Research progress of fly ash separation[J].Applied Chemical Industry,2020,49(7):1851-1856.
[6]YIN W,LI X,SUN T,et al.Experimental investigation on the mechanical and rheological properties of high-performance concrete (HPC) incorporating sinking bead[J].Construction and Building Materials,2020,243:118293.
[7]李策镭.粉煤灰——空心微珠简介[J].环境科学,1980(4):72-74.
LI C L.Fly ash—introduction of hollow microbeads[J].Environmental Science,1980(4):72-74.
[8]吕娟,黄利华,滕德亮,等.相对湿度对钙基脱硫剂干法烟气脱硫效率的影响[J].环境工程学报,2020,14(6):1563-1569.
LYU J,HUANG L H,TENG D L,et al.Effect of relative humidity on dry flue gas desulfurization efficiency of calcium based desulfurizer[J].Chinese Journal of Environmental Engineering,2020,14(6):1563-1569.
[9]WANG Y,SHUI Z,SUN T,et al.Effect of fly ash,sinking beads and metakaolin on the workability,strength,free shrinkage and chloride resistance of concretes:a comparative study[J].Arabian Journal for Science &Engineering,2018,43(10):5243-5254.
[10]SANDERS J F,KEENER T C,WANG J.Heated fly ash/hydrated lime slurries for SO2 removal in spray dryer absorbers[J].Industrial &Engineering Chemistry Research,1995,34(1):302-307.
[11]王晋刚,胡金榜,王道斌,等.粉煤灰与氢氧化钙火山灰反应制备烟气脱硫剂的动力学分析[J].化学反应工程与工艺,2006(4):329-334.
WANG J G,HU J B,WANG D B,et al.Kinetic analysis on preparation of flue gas desulfurization agent by reaction of fly ash with calcium hydroxide volcanic ash[J].Chemical Reaction Engineering and Technology,2006(4):329-334.
[12]黄昶,黄汝玲,郑仙荣,等.钙基水合改性飞灰吸附剂脱除模拟烟气中SO2的实验研究[J].科学技术与工程,2017,17(23):108-114.
HUANG C,HUANG R L,ZHENG X R,et al.Experimental study on removal of SO2 from simulated flue gas by calcium based hydration modified fly ash adsorbent[J].Science Technology and Engineering,2017,17(23):108-114.
[13]王建宏,齐美富.石灰/粉煤灰水合反应制备高活性脱硫剂机理分析[J].环境污染治理技术与设备,2003(5):34-36.
WANG J H,QI M F.Mechanism analysis of preparation of high activity desulfurizer by lime/fly ash hydration reaction[J].Technology and Equipment for Environmental Pollution Treatment,2003(5):34-36.
[14]TSUCHIAI H,ISHIZUKA T,UENO T,et al.Highly active absorbent for SO2 removal prepared from coal fly ash[J].Ind Eng Chem Res,1995,34(4):1404-1411.