碳酸钙(CaCO3)是一种重要的无机化工原材料,有天然和人工合成2种[1],粉体形式分为沉淀碳酸钙(PCC)和研磨碳酸钙(GCC)[2-3]。CaCO3具有白度高、光学性能优异、吸油值低和无毒等特点[4],且来源广泛、价格低廉,在化工、轻工、建材、医药和食品等领域已得到广泛应用,主要用作橡胶、塑料、涂料、造纸和油墨等各类材料中的填料[5-9],起到改善材料力学等性能和降低材料成本的作用。目前,大部分CaCO3仅作为惰性填料在使用,应用价值和产品附加值较低。拓展CaCO3的应用范围,在维持优势的基础上提高应用性能,以CaCO3为原材料制备其他较为昂贵、稀有、高价值的材料,或提升材料制备过程的环境友好行为,成为现今研究人员的热点课题之一。
目前,制约CaCO3提高应用价值和产品附加值的因素主要有以下几方面:首先,GCC在研磨粉碎细化的同时,颗粒表面形成了平整且棱角尖锐的形态,所以GCC在作填料填充时不易与基体形成良好的界面结合,界面处通常成为微观应力的集中点[10-11];其次,CaCO3耐酸性较差,在酸性介质中会分解释放CO2,CaCO3的热稳定性也较差,在约900 ℃的高温条件下可分解为CaO和CO2[12-13],限制了它在许多场景的应用[12,14-15];再者,CaCO3对紫外光基本无屏蔽作用,一些填充CaCO3的有机材料耐老化性能较差,在户外使用时的寿命减少[16-17],因此,对CaCO3的制备和产品设计,不仅需要将控制粒径(制备纳米碳酸钙)、形貌(球形)和实施表面有机改性作为目标,还应注重通过在其表面包覆无机物以改善颗粒外观,基于包覆物的作用弱化酸和紫外线对CaCO3的作用,从而提高产品的力学性能、耐酸性和耐老化性能。在该背景下,研究人员对以CaCO3表面包覆SiO2的核-壳结构复合颗粒的制造和应用产生了较大的兴趣。
以CaCO3表面包覆SiO2为特征的CaCO3@SiO2复合颗粒有诸多优势。第一,包覆在CaCO3表面的SiO2粒子一般为纳米或亚微米大小,SiO2的包覆使CaCO3颗粒表面光滑程度降低,棱角被钝化和赋予纳米粒子表面,由此能最大程度提高CaCO3与基体间的相容性和界面结合程度;第二,SiO2比表面积大且产生一定量的堆积孔隙,它包覆在CaCO3表面除起到一定的物理隔离作用外,还可以增加比表面积并提高表面活性[18];第三,SiO2的羟基基团可用来增强与纸张纤维和橡胶等材料的化学键结合,从而提高力学性能。SiO2表面羟基还可以作为进一步化学功能化的基础,如再与改变表面性质的改性剂紧密结合[19-20],即可赋予CaCO3@SiO2复合颗粒新的功能;第四,SiO2耐酸腐蚀且对紫外光有反射作用的特性可使CaCO3@SiO2复合颗粒形成显著优于CaCO3的抗酸和耐紫外老化性能,使复合颗粒在恶劣环境中的应用成为可能[21-22]。本文中整理了近年来有关CaCO3@SiO2复合颗粒的研究论文和专利,并针对CaCO3@SiO2的制备方法、应用及性能的研究现状进行了归纳和阐述。图1所示为CaCO3@SiO2的制备方法、功能作用及性能应用示意图。
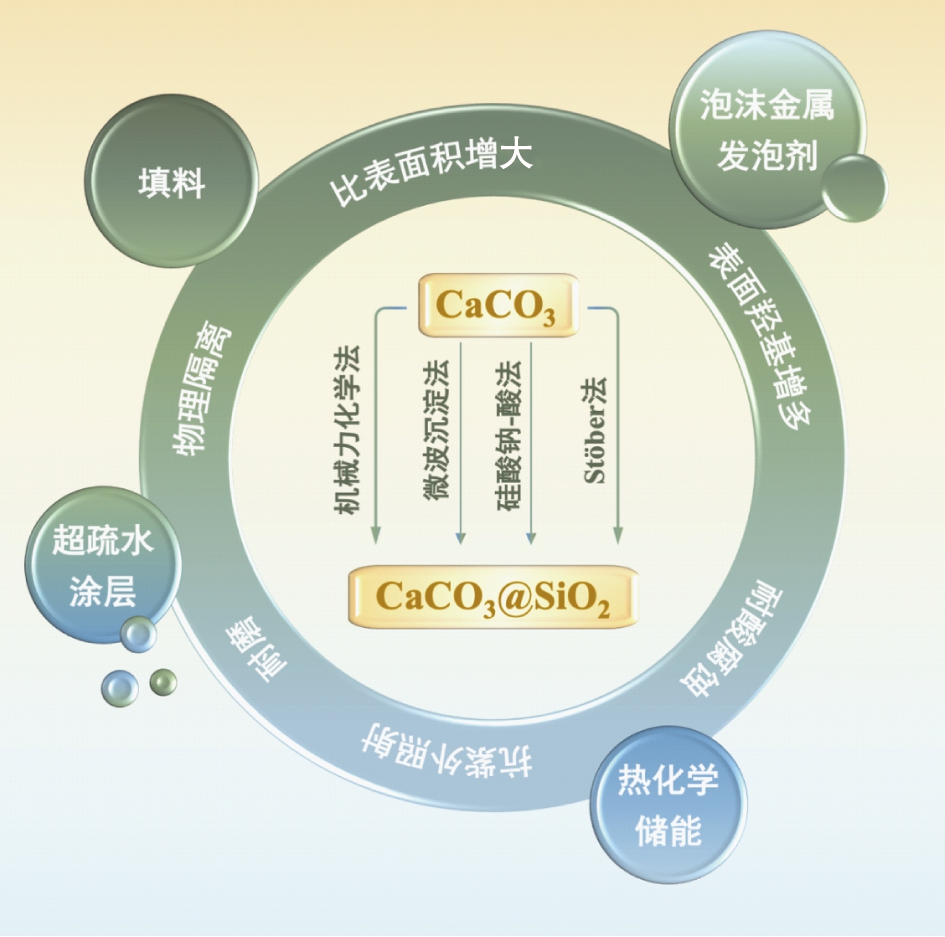
图1 CaCO3@SiO2的制备方法、功能作用及性能应用
Fig.1 Preparation method,functional role and performance application of CaCO3@SiO2
1 CaCO3@SiO2复合颗粒的制备方法
目前,CaCO3@SiO2复合颗粒的制备方法主要有机械力化学法[16,23-31]、微波沉淀法[32]、硅酸钠-酸沉淀法[33-47]和Stöber法[48-55]。其中,机械力化学法和微波沉淀法是利用已有的SiO2与CaCO3形成复合颗粒,而硅酸钠-酸沉淀法和Stöber法是在复合过程中首先形成硅酸(H2SiO3),再经由稳定透明的溶胶体系陈化、絮凝并缩聚成为SiO2,最终在CaCO3表面形成三维空间网络结构的凝胶并沉淀[56-57]。H2SiO3在较为宽泛的pH条件下均可缩聚为SiO2,并在酸性或碱性条件下的缩聚反应较中性时更为迅速。与酸性反应条件相比,碱性条件由于表面强负电荷的作用不利于SiO2形成凝胶网络和最终絮凝沉淀,而是形成稳定存在的悬浮液[58],因而,在制备SiO2的过程中可利用上述现象,先在碱性条件下快速生成稳定的SiO2颗粒,然后在偏酸性条件下产生凝胶聚集体形成沉淀。本文中详细综述了制备CaCO3@SiO2复合颗粒的方法,并说明CaCO3和SiO2之间的结合方式及制备方法对所得复合颗粒形貌和性能的影响。
1.1 以原有SiO2为原料的制备方法
1.1.1 机械力化学法
以机械力对固体材料进行挤压、剪切或研磨不仅可以使粒子高度分散,还能改变物质的结构、性能和赋予其较高的表面能[59-60]。若同时研磨2种不同的物质可能在二者界面处发生化学反应,利用此现象制备复合材料的方法称为机械力化学法[61-62]。
杨卓如团队[16,23-26]利用均质器对PCC和纳米SiO2进行预混(转速为1 000 r/min,时间为10 min)和搅拌(转速为7 000 r/min,时间为30 min),制备了以CaCO3为核、SiO2为壳的桑椹状前体,形成了超疏水材料所需的微-纳二元结构,并通过红外测试证实CaCO3和SiO2之间是以物理作用进行结合。Espin等[27]利用半满的转鼓(转速为55 r/min,时间为1 h)制备CaCO3@SiO2复合颗粒,表明SiO2存在于CaCO3表面会增加复合颗粒的流动性,同时阐明了SiO2可均匀负载于CaCO3表面的原因为剧烈机械力作用下产生的静电电荷转移行为。在实际应用过程中,通常会添加研磨介质以增强冲击力和达到更好的复合效果[63],Chen等[28]将纳米SiO2和CaCO3置于研磨罐中,放入固定数量的直径分别为6、10 mm的玛瑙球作为研磨介质,以顺时针和逆时针方向交替进行球磨(交替时间为90 min,转速为580 r/min),整个过程需在氩气气氛下持续15 h,随后将样品干燥获得CaCO3@SiO2复合颗粒。结果表明,SiO2纳米颗粒牢固地包覆在CaCO3上,防止了SiO2纳米颗粒的团聚和保持了纳米特性。Cui等[30]将SiO2和聚丙烯酸钠(PAAS)制浆后与锆质研磨介质混合,在超细搅拌磨中预磨90 min解聚SiO2,然后向上述混合物中添加GCC,并利用氨水将pH控制在10左右,在转速为1 600 r/min的条件下研磨40 min,经离心、干燥和研磨打散制得CaCO3@SiO2复合颗粒,如图2所示。红外光谱(FTIR)显示在机械力化学作用前后![]() 的化学环境发生了变化,同时硅羟基官能团(Si—OH)参与了SiO2和CaCO3之间的结合,说明研磨过程使SiO2和CaCO3颗粒表面活化,并通过化学键紧密地结合在一起。
的化学环境发生了变化,同时硅羟基官能团(Si—OH)参与了SiO2和CaCO3之间的结合,说明研磨过程使SiO2和CaCO3颗粒表面活化,并通过化学键紧密地结合在一起。
以机械力化学法制备CaCO3@SiO2复合颗粒还具有制备工艺简单、能力大和环境友好等特点,适合大规模工业生产,具有一定应用前景[64-65]。然而,由于机械力化学法的随机性和过程不可控性,目前仍然无法精准控制负载物质SiO2的团聚尺寸、形态和程度[66],在一定程度上影响了CaCO3@SiO2复合颗粒的形貌和性能。
1.1.2 微波沉淀法
Pach等[32]通过向CaCO3中通入CO2并过滤多余CaCO3的方式,制备了饱和的碳酸氢钙溶液,并以CO2控制稳定性,将SiO2质量分数为29.7%的硅溶胶与之混合,置于功率为900 W的微波炉中进行沉淀,随后在室温条件下静置24 h并干燥,最终得到CaCO3@SiO2复合颗粒。结果表明,溶液中的Ca2+与硅溶胶中SiO2的相互作用使CaCO3在SiO2表面成核,形成的CaCO3含方解石和文石两晶相,且晶体尺寸与SiO2的含量密切相关。由于微波的能量与H2O脱离碳酸氢钙所需能量接近,因此微波沉淀法相较于等温沉淀法更为有效。

1.2 以合成SiO2的前驱体为原料的方法
1.2.1 硅酸钠-酸沉淀法
工业上生产沉淀SiO2大多是利用硫酸(H2SO4)和盐酸(HCl)等强酸,也有采用碳酸(H2CO3,水体系中通入CO2形成)等弱酸与一定浓度的硅酸钠(Na2SiO3或Na2O·mSiO2)溶液反应,生成H2SiO3,并进一步得到SiO2·nH2O,再经过陈化、分离、干燥和研磨得到沉淀SiO2成品。原理可总结为化学反应方程式(1)。其中,采用碳酸(H2CO3)与Na2SiO3溶液反应的方法也被称为碳酸化法。
Na2O·mSiO2+2H++nH2O→2Na++mSiO2·(n+1)H2O↓。
(1)
1.2.1.1 使用硫酸和盐酸为代表的强酸
利用硅酸钠-强酸沉淀法制备CaCO3@SiO2复合颗粒的过程可描述为:利用搅拌或超声等手段将CaCO3和Na2SiO3混合均匀,并将混合液置于固定温度的水浴中,以一定速度加入H2SO4或HCl,搅拌,使pH保持在某范围内,保温陈化,再经冷却、过滤、洗涤、干燥和研磨等步骤处理即获得CaCO3@SiO2复合颗粒[33-38]。另有研究选择将CaCO3与分散剂混合均匀,放置在水浴中,同时滴入酸和Na2SiO3[39-41]。此外,制备CaCO3@SiO2复合颗粒的Na2SiO3原料并不一定是化工原料成品,如Morsy等[43]通过碱浸法将工业废弃物半燃烧稻草灰制成Na2SiO3,并利用碳酸化法制备纳米CaCO3以作原料。王宪伟等[40]将石灰石煅烧形成CaO,加水制成Ca(OH)2,再与Na2CO3反应生成CaCO3原料。在上述方法中,CaCO3的固含量(质量分数)、Na2SiO3浓度、强酸浓度、水浴温度、加酸速度、体系pH、陈化时间均对复合颗粒的形貌和结构有影响,本文中将现有以硅酸钠-强酸沉淀法制备CaCO3@SiO2复合颗粒文献中的相关参数如表1、2所示。
表1 硅酸钠-强酸沉淀法制备CaCO3@SiO2复合颗粒的工艺参数(1)
Tab.1 Process parameters for preparation of CaCO3@SiO2 composite particles by sodium silicate-strong acid precipitation method (1)
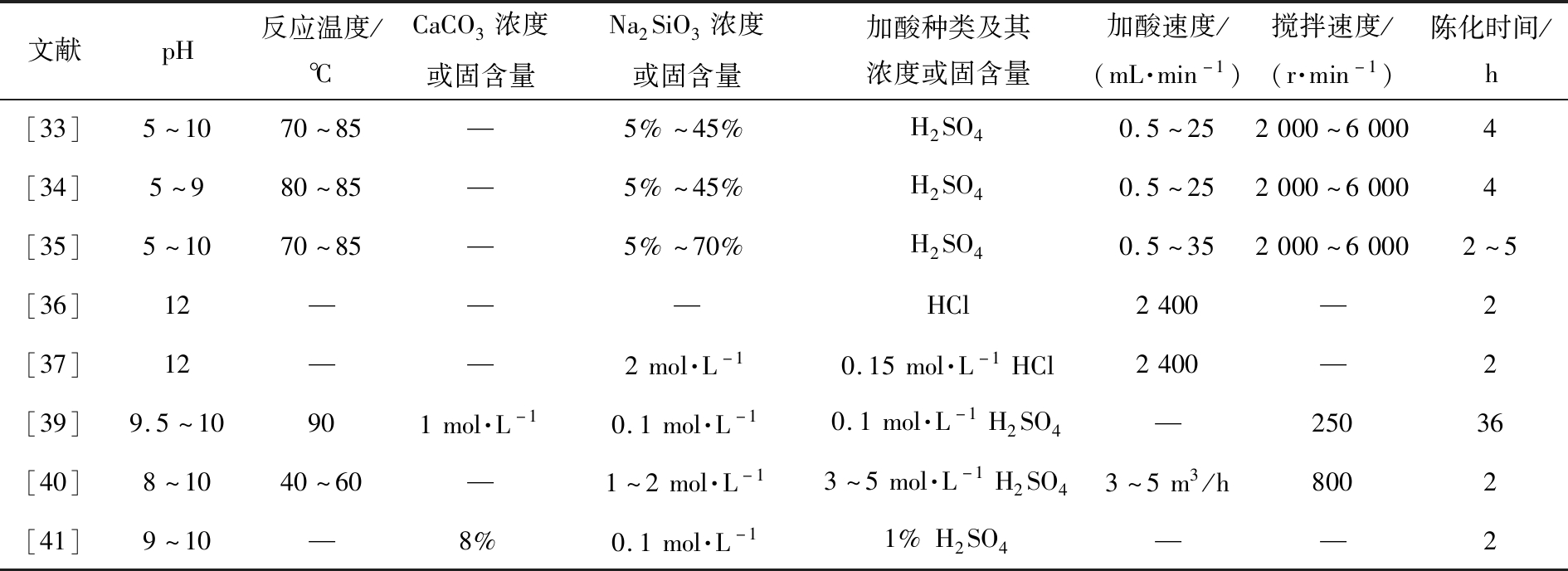
文献pH反应温度/℃CaCO3浓度或固含量Na2SiO3浓度或固含量加酸种类及其浓度或固含量加酸速度/(mL·min-1)搅拌速度/(r·min-1)陈化时间/h[33]5~1070~85—5%~45%H2SO40.5~252000~60004[34]5~980~85—5%~45%H2SO40.5~252000~60004[35]5~1070~85—5%~70%H2SO40.5~352000~60002~5[36]12———HCl2400—2[37]12——2mol·L-10.15mol·L-1HCl2400—2[39]9.5~10901mol·L-10.1mol·L-10.1mol·L-1H2SO4—25036[40]8~1040~60—1~2mol·L-13~5mol·L-1H2SO43~5m3/h8002[41]9~10—8%0.1mol·L-11%H2SO4——2
表2 硅酸钠-强酸沉淀法制备CaCO3@SiO2复合颗粒的工艺参数(2)
Tab.2 Process parameters for preparation of CaCO3@SiO2 composite particles by sodium silicate-strong acid precipitation method (2)
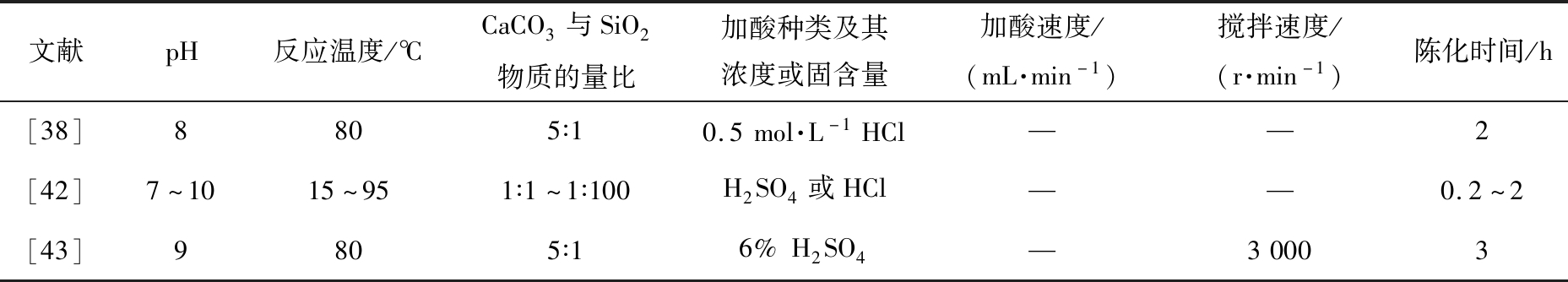
文献pH反应温度/℃CaCO3与SiO2物质的量比加酸种类及其浓度或固含量加酸速度/(mL·min-1)搅拌速度/(r·min-1)陈化时间/h[38]8805∶10.5mol·L-1HCl——2[42]7~1015~951∶1~1∶100H2SO4或HCl——0.2~2[43]9805∶16%H2SO4—30003
1.2.1.2 使用碳酸(碳酸化法)为代表的弱酸
相比硅酸钠-强酸沉淀法,碳酸化法通常不设置搅拌装置,而是利用CO2气体的流动压力使反应体系搅动。由于CaCO3也可通过向Ca(OH)2中通入CO2制得,因此,以碳酸化法制备CaCO3@SiO2复合颗粒的大多研究均以CaO或Ca(OH)2作为CaCO3的前驱体原料[19,44-45],以一定流速通入CO2或CO2与N2的混合气体,得到CaCO3后,再向体系中加入Na2SiO3,继续通气,一步制成CaCO3@SiO2复合颗粒,如图3所示。现将相关文献中的CaCO3的固含量、Na2SiO3的浓度、CO2浓度、反应温度、CO2流量、体系pH值变化及陈化时间总结如表3所示。
表3 碳酸化法制备CaCO3@SiO2复合颗粒的相关制备参数
Tab.3 Relevant preparation parameters of CaCO3@SiO2 composite particles prepared by carbonation method

文献初始pH最终pH反应温度/℃CaCO3与SiO2质量比或物质的量比CO2质量分数CO2流量/(mL·min-1)陈化时间/h[44]9780n(SiO2)∶n(CaCO3)=16.67%100%1202[19]9~127.5~8.075~80m(SiO2)∶m(CaCO3)=5%~8%100%——[45]9不再下降50m(SiO2)∶m(CaCO3)=5%33%—2[46]9~12不再下降90m(SiO2)∶m(CaCO3)=5%~25%100%—2~5
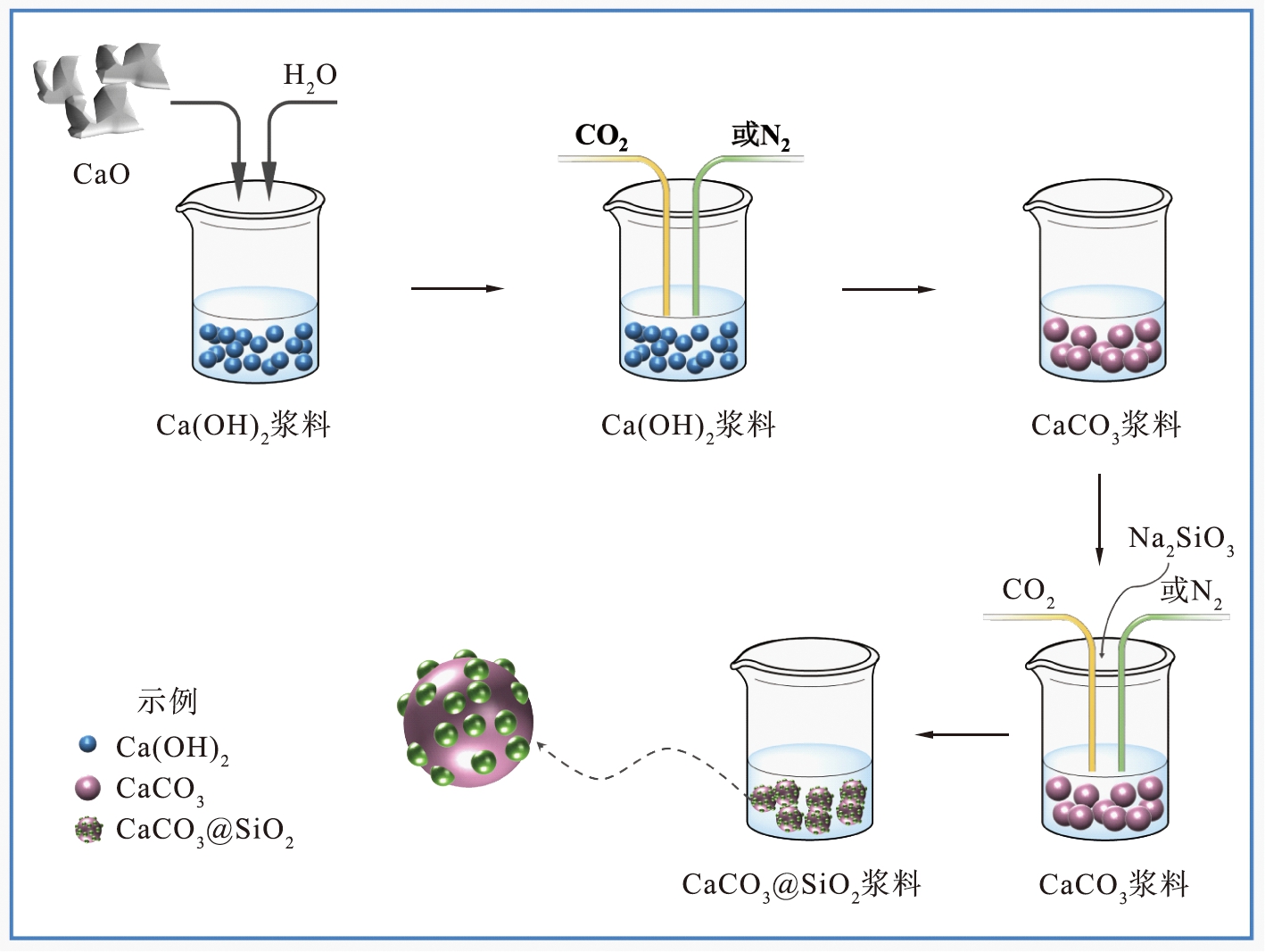
图3 碳酸化法制备CaCO3@SiO2复合颗粒的流程图
Fig.3 Flow chart of CaCO3@SiO2 composite particles prepared by carbonation method
于岩等[47]利用改进的硅酸钠-酸沉淀法一步合成了CaCO3@SiO2纳米管。首先,将浓度为2~3 mmol/L的Na2SiO3溶液和浓度为5~10 mmol/L的Na2CO3溶液混合制成溶液A,再配置浓度为5~10 mmol/L的CaCl2记为溶液B。然后,将A和B分别置于温度为30 ℃的水浴中保温,期间将B以1~3 mL/min的滴定速度加入至A中,随后静置30 min。最后,将得到的白色沉淀先后用去离子水、稀盐酸和去离子水洗涤,经冷冻干燥后得到CaCO3@SiO2纳米管。
通过对以上2种方法所得CaCO3@SiO2复合颗粒的结构与形貌进行表征,可知以硅酸钠-酸沉淀法制备的复合颗粒,SiO2均匀包覆于CaCO3表面,形成致密的无定形态SiO2壳层[36],该壳层呈膜状[41]、网状[37]或絮状[44],CaCO3原本凸起的棱角消失,变得圆滑[36]。通过红外光谱或XPS等手段可以确定,复合颗粒中CaCO3与SiO2之间是以—Si—O—Ca—化学键紧密结合的[33-36,41]。另外,研究发现SiO2的加入可降低复合颗粒的密度[43],同时会对CaCO3晶体生长有限制作用[41],各制备参数对SiO2壳层的生长均有不同影响,其中体系pH因对表面电荷产生影响而对SiO2的形成和沉积具有较大作用[36,45]。
1.2.2 Stöber法
Stöber法是以烷氧基硅烷(主要是四乙氧基硅烷,TEOS)作为硅源,通过水解和缩聚反应合成SiO2而制备CaCO3@SiO2的方法,TEOS(结构式表示为![]() 水解化学反应方程式见式(2)。反应过程中常以氨水(NH3·H2O)为催化剂,最终形成近球形且分散性较好[49]的SiO2颗粒。以Stöber法制备CaCO3@SiO2复合颗粒一般形成膜状或乳突状SiO2壳层[48,55],可大幅提高CaCO3的表面粗糙度[54]。
水解化学反应方程式见式(2)。反应过程中常以氨水(NH3·H2O)为催化剂,最终形成近球形且分散性较好[49]的SiO2颗粒。以Stöber法制备CaCO3@SiO2复合颗粒一般形成膜状或乳突状SiO2壳层[48,55],可大幅提高CaCO3的表面粗糙度[54]。
(2)
Ferreira团队[52-54]将去离子水(体积为13.5 mL)、乙醇(体积为126.5 mL)和NH3·H2O(体积为3.37 mL)混合为A液,以PCC(质量为1.5 g)和TEOS(体积为6.75 mL)混合记为B液,将B液加入至A液中,并在室温下以200 r/min的转速搅拌24 h,再经过滤,乙醇洗涤和真空干燥,最终得到CaCO3@SiO2复合颗粒。利用Zeta电位测试发现,负载SiO2的复合颗粒电位为负,这是由于碱性条件下Si—OH将H+释放所致。另外,有研究发现在制备过程中增加NH3·H2O的量(即增强碱性),可使H2SiO3缩聚加快[51],从而增加CaCO3表面SiO2的负载量。Wang等[51]以Ca(CH2COO)2·H2O和NaHCO3溶液混合制备CaCO3,向其中添加NH3·H2O(体积为1 mL)、TEOS(体积为10 mL)和十六烷基三甲基溴化铵(CTAB,质量为0.1 g),保持pH在8~9之间,磁搅4 h后,经过滤、洗涤和干燥得到SiO2壳层厚为100~200 nm的CaCO3@SiO2复合颗粒,并将二者结合的机制阐述为Si—OH与CaCO3表面羟基的脱水缩合反应,并形成了—Si—O—Ca—牢固的化学键。此外,Chen等[50]通过设置对比实验发现在高温条件下TEOS水解更迅速,归因于吸热反应在高温下易正向进行。
2 CaCO3@SiO2复合颗粒的应用及性能
CaCO3@SiO2复合颗粒应用范围较广泛。CaCO3和SiO2由于本身的一些特质而广泛应用于橡胶和造纸等行业中,研究人员发现二者的互补特质可弥补在上述行业应用中存在的一些不足,从而将二者有机地结合到一起。对CaCO3@SiO2复合颗粒进行有机改性可获得表面超疏水特性,从而扩展应用范围。利用CaCO3的分解或CaCO3与CaO之间的钙循环特性,可设计将CaCO3@SiO2复合颗粒应用于热化学储能及泡沫金属发泡剂方向,从而实现提升材料性能及材料综合化利用等目的。
2.1 改性CaCO3@SiO2复合颗粒制备超疏水涂层
通过观察荷叶、稻叶[67]、蝴蝶翅膀[68]和壁虎脚[69]等表面的天然超疏水现象,研究人员对特殊的粘附性和自清洁性产生了浓厚兴趣,开展了大量研究[70-71]。超疏水是指水滴在材料表面近乎呈球形且几乎没有粘附性的现象[72],其中,用于评估静态润湿性的接触角(WCA)应大于150°,评估动态润湿性的滑动角(SA)应小于10°[31,73]。研究表明,表面粗糙度和自由能与其超疏水特性具有较强的相关性[74-75],因此,可通过构建高粗糙度的微-纳二元结构和利用低表面能物质对材料表面的改性以制备超疏水表面。近年来,有研究将微米级CaCO3与纳米级SiO2复合形成多层次结构并利用硬脂酸[49]、聚二甲基硅氧烷(PDMS)[17,24-25]或六甲基二硅氮烷(HMDS)[26]等低表面能的有机物对CaCO3@SiO2复合颗粒表面进行改性制备超疏水材料。
另外,超疏水涂层在恶劣环境和大型建筑材料表面应用时的稳定状况,即涂层的耐久性也是亟需解决的重要问题之一[76-77]。杨卓如团队[16,24-26]利用简单的机械力化学法制备了CaCO3@SiO2复合颗粒,改性后添加至室温硫化(RTV)硅橡胶中,并将所得硅橡胶涂覆在输电系统的高压绝缘子上制成了具有超疏水特性的RTV涂层,如图4所示,涂层的WCA和SA分别约为165°和5°。该RTV涂层优异的超疏水性能可进一步有效抑制绝缘子在复杂环境中因累积污物和污层润湿而产生电弧最终闪络的发生,超疏水RTV绝缘子闪络电压比普通RTV绝缘子高6.56 kV。此外,对该超疏水RTV涂层的化学稳定性(耐酸、耐碱和耐海水腐蚀性)、抗冲击性及撕裂强度进行了测试,表明均可达到RTV涂层的标准。Wang等[17]将PDMS改性的CaCO3@SiO2复合颗粒通过简单的刷涂方式应用于大型建筑的外墙表面,测得表面WCA为159°,SA为1°。将该涂层建材浸泡于酸性环境下放置3 d、经质量为60 g的沙子摩擦或在室外放置3 m后,仍能保持表面超疏水的特性,验证了复合颗粒的耐酸、机械稳定及抗紫外等特性。正是由于SiO2耐酸[78]和反射紫外光[79-80]的性质,使CaCO3@SiO2复合颗粒除构成超疏水涂层必要的微-纳二元结构以外,还赋予了涂层较强的化学耐久性,因此增加了在恶劣条件下使用性能的稳定。
2.2 CaCO3@SiO2复合颗粒作填料
CaCO3具有广泛易得、色白及价廉的特点,因而成为橡胶、造纸和涂料等工业中用量最大的浅色矿物填料之一[81];然而,由于CaCO3具有亲水性及表面活性低等问题,导致CaCO3与基体或改性物质之间无法形成良好的结合,且研磨获得的GCC粒度相对较大,因此CaCO3仅能发挥减少主体材料用量和成本即填充增量的作用[82]。已有研究发现,利用耐酸、耐磨、粒径小且界面活性强的SiO2对CaCO3改性可提升CaCO3的应用价值,并进一步增加其填料用量[43]。

PCC作为印刷纸和高级书写纸最常见的填料,可增加纸张的亮度、白度、光泽度和不透明度,然而,PCC的添加不仅因降低纸张的机械强度而无法大量添加,从而导致降低成本作用有限,添加PCC的喷墨打印纸还因渗透性和吸收能力不佳而影响打印质量。Gamelas等[52]、Ferreira等[53-54]将PCC表面包覆SiO2的复合颗粒添加至造纸纤维中,使纸张在保持因添加PCC而获得的优异光学性能的前提下,提升了拉伸、破裂及撕裂指数等机械性能,填料用量也提高了5%。同时SiO2赋予了纸张耐酸性,在弱酸至中性环境中能稳定生产。Wang等[51]将SiO2颗粒负载于CaCO3表面并应用在喷墨纸打印纸中,充分利用了CaCO3在成本和光学性能方面、SiO2在表面积和孔隙率方面的优势,解决了CaCO3和SiO2孔隙率不适合的问题。结果表明,应用CaCO3@SiO2的纸张具有比应用纯SiO2纸张更高的平滑度(60.8%)和光泽度(78.4%),具有比应用纯CaCO3纸张更高的密度(28.8%)和清晰度(4.1%)。另外,研究人员发现在制备硅橡胶时加入核壳结构的CaCO3@SiO2复合颗粒除可解决CaCO3与基体结合不佳及附加值低的问题外,还可解决纯SiO2作为补强剂聚集程度高及流动性强导致的成本高和补强效果不佳的问题。Cui等[30]以GCC和沉淀SiO2为原料,制备了CaCO3@SiO2复合颗粒,CaCO3表面的SiO2颗粒分布均匀,将复合颗粒加入至甲基乙烯基硅橡胶中,所得硅橡胶的断裂拉伸强度比添加纯SiO2时提高18%,断裂伸长率虽比添加纯SiO2略低,但比添加CaCO3提高了121%。Liu等[33]、Liu等[44]、Yu等[83]也采用SiO2对CaCO3表面进行修饰,利用SiO2表面的Si—OH官能团与硅烷类改性剂形成化学键的特点,使复合颗粒与橡胶基体的结合更为牢固,从而进一步提升了硅橡胶的机械性能,并增加了填料含量和降低了制品成本。由此可见,SiO2通过增加CaCO3的表面活性而增强了与其他物质之间的连接程度[84-85],并且CaCO3通过均匀分散SiO2暴露了更多活性表面,这对提高SiO2的补强作用,增强材料的力学性能,降低成本和将CaCO3转化为高附加值材料起到了积极作用。
2.3 CaCO3因表面包覆SiO2而提升热化学储能能力
CaCO3可在高温条件下分解为CaO和CO2,并吸收能量(178 kJ/mol),而CaO又可通过碳酸化过程将这部分能量释放[86-87]。加之CaCO3在自然界中存储量大和具有成本低、环保、热分解-碳酸化反应过程无副反应、能量密度高且产物(CaO)稳定易分离等优点,因此,CaO-CaCO3系统成为热化学储能系统中最具潜力的高温反应对之一[88-89]。已有大量研究证实,在CaO-CaCO3系统中添加惰性材料(如SiO2、CeO2、AlOOH、Li2SO4、TiO2或Ca3Al2O6等),一方面可降低CaCO3煅烧温度,提高CaO和CaCO3的活性,降低反应活化能[90];另一方面可防止CaO颗粒团聚后在高温下烧结而导致整个系统逐渐失效,从而提高循环稳定性,同时可保证CO2能在碳酸化过程中利用较低的压力均匀扩散至CaO颗粒的内部缝隙中。Chen等[28]通过机械力化学法将5%的SiO2与CaCO3复合,系统研究了CaO-CaCO3系统加入SiO2后的动力学、热力学和循环稳定性,结果表明,SiO2的加入降低了反应活化能约40 kJ/mol,比热容提高了20%,循环稳定性提高了28%,说明加入SiO2的CaO-CaCO3系统可稳定高效地运行。Khosa等[29]发现SiO2可大大降低CaCO3的煅烧脱碳温度(近150 ℃)并显著提高脱碳反应的速率,根本原因是SiO2抑制了CaO的烧结,从而在下一次放热过程中节省了热量。Espin等[27]提出,在能量储存的实际应用中,固体颗粒的流动对气、固接触效率及循环稳定性起到至关重要的作用,而颗粒的流动行为主要取决于粒径大小,因此该团队对粒径为15、30 μm的CaO-CaCO3和极细颗粒(粒径<4 μm)的流动特性进行了研究,并尝试添加少量SiO2以提高CaO-CaCO3系统的粉体流动性。这些研究表明,通过将经济且分布广泛的SiO2与CaCO3复合用作一种热化学储能系统,在能源存储再利用和工业废热回收方面存在潜在应用价值。
2.4 钝化层SiO2改善CaCO3发泡剂发泡性能和热稳定性
镁泡沫金属因具有孔隙率高、密度低和强度高等特性,可广泛应用于阻燃材料、轻质结构材料、隔音降噪材料及可生物降解支撑材料等领域[91]。碳酸盐(如CaCO3)是熔融发泡法和粉末冶金法制备镁泡沫金属的常用发泡剂之一[92-93],但CaCO3可能存在的过早分解问题会导致镁泡沫金属的质量严重下降,因此,Erryani等[36]采用以SiO2钝化层包覆CaCO3表面的方式缩小了CaCO3分解的温度范围,从而提升了CaCO3的热稳定性并控制其发泡速度,使所得镁泡沫金属具有更均匀的孔径、孔分布和更高的孔隙率。另外,Lu等[37]发现以CaCO3@SiO2复合颗粒代替CaCO3不仅可以使起泡温度上升40 ℃,起泡过程匀速平稳,还可在没有CO2和SF6的混合气体保护下得到孔隙率为60%~70%的大尺寸可阻燃的镁泡沫金属,良好地适应了大规模生产的便捷性需求。
3 结论及展望
综上所述,CaCO3@SiO2复合颗粒可通过机械力化学法、微波沉淀法、硅酸钠-酸沉淀法和Stöber法等方法制得,并可应用于超疏水涂层、橡胶造纸等行业填充、CaO-CaCO3热化学储能系统和镁泡沫金属发泡剂等领域。
1)以硅酸钠-酸沉淀法和Stöber法制备的复合颗粒中SiO2的分布和粒径较为均匀,在CaCO3表面的形态丰富,但硅酸钠-酸沉淀法和Stöber法的生产工艺复杂,且在大规模工业生产中需要处理大量废液。机械力化学法制备CaCO3@SiO2复合颗粒方法具有工艺简单、产能大和绿色环保等优势。
2) CaCO3@SiO2复合颗粒以SiO2颗粒牢固地包覆在CaCO3表面为特征,具有连续的核壳结构或不连续的二元结构,CaCO3原本的棱角被钝化,平滑的表面形貌变得粗糙;CaCO3和SiO2之间大多以Si—O—Ca化学键紧密结合;SiO2对CaCO3的密度、比表面积和孔隙率等物理性能均有一定影响。
3)SiO2可增加CaCO3的耐酸性、耐磨性和抗紫外照射性,从而提升CaCO3的耐老化性能;SiO2对CaCO3的界面活性具有提升作用,有利于增强填料与基体的结合强度及纸张和橡胶的机械强度;SiO2可降低CaCO3的热分解反应的反应活化能,并通过增加CaO-CaCO3系统的流动性而提升系统的循环稳定性;利用SiO2可控制CaCO3发泡速度和均匀程度的特点,制备孔隙率高的镁泡沫金属。
CaCO3@SiO2是一种由CaCO3和SiO2通过有序结构复合形成的功能粉体材料,CaCO3和SiO2二者之间相互协作而发挥各自优势,可满足更多应用研究的需求。CaCO3和SiO2是2种应用较为广泛且研究较为成熟的传统材料,将二者复合可使其焕发新生,拓展应用领域。
今后,深入探究SiO2对CaCO3结构和性能的具体影响及其原因,并进一步拓展CaCO3@SiO2复合颗粒的应用范围将是研究人员的一个重点突破方向。如研究利用CaCO3高温时释放CO2的特性,以CaCO3@SiO2复合颗粒为阻燃剂[55],但并未探究SiO2在系统中的作用。又如,大量研究提出利用CO2矿物碳酸化的特性将CO2封存于碳酸盐中,达到CO2减排的目的[95-96],但CaCO3@SiO2复合颗粒是否在捕获CO2气体方面有优于CaCO3的表现还有待研究。此外,利用CaCO3@SiO2复合颗粒表面具有丰富羟基和空隙特征,以及可弥补CaCO3在表面羟基基团少、耐酸性和抗紫外老化性较差等不足的特点,使之在吸附重金属离子废水和作为负载其他功能材料(如TiO2等)载体方面发挥积极作用。同时,还应探索CaCO3@SiO2复合颗粒功能特性的预先(实际应用前)评价方法。
[1]MALLAKPOUR S,TABESH F,HUSSAIN C M,et al.Water decontamination using CaCO3 nanostructure and its nanocomposites:current advances[J/OL].Polymer Bulletin.2022,https://doi.org/10.1007/s00289-022-04431-8.
[2]SAULAT H,CAO M,KHAN M M,et al.Preparation and applications of calcium carbonate whisker with a special focus on construction materials[J].Construction and Building Materials,2020,236:117613.
[3]JIMOH O A,ARIFFIN K S,HUSSIN H B,et al.Synthesis of precipitated calcium carbonate:a review[J].Carbonates and Evaporites,2017,33(2):331-346.
[4]LI C Q,LIANG C,CHEN Z M,et al.Surface modification of calcium carbonate:a review of theories,methods and applications[J].Journal of Central South University,2021,28(9):2589-2611.
[5]YADAV V K,YADAV K K,CABRAL PINTO M M S,et al.The processing of calcium rich agricultural and industrial waste for recovery of calcium carbonate and calcium oxide and their application for environmental cleanup:a review[J].Applied Sciences,2021,11(9):4212.
[6]MATTILA H P,ZEVENHOVEN R.Production of precipitated calcium carbonate from steel converter slag and other calcium-containing industrial wastes and residues[J].CO2 Chemistry,2014,66:347-384.
[7]MEDEIROS S K,ALBUQUERQUE E L,MAIA F F,et al.Electronic and optical properties of CaCO3 calcite,and excitons in Si@CaCO3 and CaCO3@SiO2 core-shell quantum dots[J].Journal of Physics D:Applied Physics,2007,40(18):5747-5752.
[8]CAETANO E W S,MAIA F F,FREIRE V N,et al.Si-SiO2-Si and Si-CaCO3-Si core-double-shell nanoparticles:tuning light emission from infrared to ultraviolet[J].Journal of Applied Physics,2007,102(2):023712.
[9]FADIA P,TYAGI S,BHAGAT S,et al.Calcium carbonate nano- and microparticles:synthesis methods and biological applications[J].3 Biotech,2021,11(11):457.
[10]盖国胜.微纳米颗粒复合与功能化设计[M].北京:清华大学出版社,2008:89-131.
GAI G S.Micro-nanometer particle composition and functional design[M].Beijing:Tsinghua University Press,2008:89-131.
[11]YANG Y F,GAI G S,FAN S M.Surface nano-structured particles and characterization[J].International Journal of Mineral Processing,2006,78(2):78-84.
[12]NIU Y Q,LIU J H,AYMONIER C,et al.Calcium carbonate:controlled synthesis,surface functionalization,and nanostructured materials[J/OL].Chemical Society Reviews,2022.https://doi.org/10.1039/D1CS00519G.
[13]VANDEGINSTE V.Food waste eggshell valorization through development of new composites:a review[J].Sustainable Materials and Technologies,2021,29:e00317.
[14]LI Z,HUANG C,GUO L,et al.Mass production and application of TiO2@CaCO3 composites in interior emulsion coatings[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects,2016,498:98-105.
[15]DIZAJ S M,BARZEGAR JALALI M,ZARRINTAN M H,et al.Calcium carbonate nanoparticles as cancer drug delivery system[J].Expert Opinion on Drug Delivery,2015,12(10):1649-1660.
[16]HAI J,YANG J X,CHENG J,et al.Preparation and performance of RTV coating for anti-pollution flashover with superhydrophobicity by filling CaCO3/SiO2 composite particles into silicone rubber[C]//International Conference on Mechatronics and Materials Processing (ICMMP 2011).Guangzhou,China,2011,328-330:1263-1267.https://doi.org/10.4028/www.scientific.net/AMR.
[17]WANG M,TAN X Y,TU Y T,et al.Self-healing PDMS/SiO2-CaCO3 composite coating for highly efficient protection of building materials[J].Materials Letters,2020,265:127290.
[18]VALENCIA D,CONDE R I,GARCíA B,et al.Development of bio-inspired supports based on Ca-SiO2 and their use in hydrodeoxygenation of palmitic acid[J].Renewable Energy,2020,148:1034-1040.
[19]SHUI M,RENG Y L,PU B Y,et al.Variation of surface characteristics of silica-coated calcium carbonate[J].Journal of Colloid and Interface Science,2004,273(1):205-210.
[20]ZOU B,HU Y,CUI F,et al.Effect of surface modification of low cost mesoporous SiO2 carriers on the properties of immobilized lipase[J].Journal of Colloid and Interface Science,2014,417:210-216.
[21]DAO N N,NGUYEN T H C,DOAN T D,et al.Effect of CeO2-Fe2O3 coated SiO2 nanoparticles on the thermal stability and UV resistance of polyurethane films[J].Journal of Polymer Research,2021,28(4):139.
[22]YU F Y,GAO J,LIU C P,et al.Preparation and UV aging of nano-SiO2/fluorinated polyacrylate polyurethane hydrophobic composite coating[J].Progress in Organic Coatings,2020,141:105556.
[23]YANG J X,WEN X F,PI P H,et al.Preparation of CaCO3/SiO2 composite particles and their application in superhydrophobic coating[J].Journal of the Chinese Silicate Society,2009,37(1):12-17.
[24]YANG J X,PI P H,WEN X F,et al.A novel method to fabricate superhydrophobic surfaces based on well-defined mulberry-like particles and self-assembly of polydimethylsiloxane[J].Applied Surface Science,2009,255(6):3507-3512.
[25]YANG J X,ZHOU Z H,WEN X F,et al.Mechano-chemical surface modification of nano silica[J].Journal of the Chinese Silicate Society,2010,38(2):320-326.
[26]WEN X F,LIU Y,XU Z J,et al.Mechano-chemical preparation and application of mulberry-like CaCO3/SiO2 composite particles in superhydrophobic films[J].Soft Materials,2012,10(4):435-448.
[27]ESPIN M J,EBRI J M P,VALVERDE J M.Tensile strength and compressibility of fine CaCO3 powders:effect of nanosilica addition[J].Chemical Engineering Journal,2019,378:122166.
[28]CHEN X Y,JIN X G,LIU Z M,et al.Experimental investigation on the CaO/CaCO3 thermochemical energy storage with SiO2 doping[J].Energy,2018,155:128-138.
[29]KHOSA A A,ZHAO C Y.Heat storage and release performance analysis of CaCO3/CaO thermal energy storage system after doping nano silica[J].Solar Energy,2019,188:619-630.
[30]CUI C,DING H,CAO L,et al.Preparation of CaCO3-SiO2 composite with core-shell structure and its application in silicone rubber[J].Polish Journal of Chemical Technology,2015,17(4):128-133.
[31]方京男,洪碧圆,童威,等.基于CaCO3/SiO2复合粒子的超疏水表面制备[J].浙江大学学报(理学版),2011,38(2):189-193.
FANG J N,HONG B Y,TONG W,et al.Preparation of super water-repellent surfaces on the basis of CaCO3/nano-SiO2 composite particles[J].Journal of Zhejiang University(Science Edition),2011,38(2):189-193.
[32]PACH L,HRABE Z,SVETIK S,et al.Preparation and thermal behavior of CaCO3/SiO2 nanocomposite[J].Materials Research Bulletin,1998,33(11):1653-1660.
[33]LIU G,ZENG H.A study of in-situ organic hybrid and application of nanometered CaCO3/SiO2 composite partiocles[J].Materials Review,2002,16(12):71-73.
[34]刘国军,曾汉民.纳米CaCO3/SiO2核-壳结构复合粒子的制备[J].宇航材料工艺,2003(3):57-61.
LIU G J,ZENG H M.Preparation of Nanometer CaCO3/SiO2 Composite Particles with Core-shell Structure[J].Aerospace Materials &Technology,2003(3):57-61.
[35]曾汉民,刘国军.纳米CaCO3/SiO2核-壳结构粒子的制备方法:02115028.1[P].2004-09-22.
ZENG H M,LIU G J.Preparation method of nano CaCO3/SiO2 core-shell structure particles:02115028.1[P].2004-09-22.
[36]ERRYANI A,LESTARI F P,ANNUR D,et al.Preparation and characterization of coating sodium trisilicate (Na2O center dot n SiO2) at calcium carbonate (CaCO3) for blowing agent in Mg alloy foam[C]//1st International Seminar on Metallurgy and Materials (ISMM).Jakarta,Indonesia,2017,1964:020002.https://doi.org/10.1063/1.5038284.
[37]LU G Q,HAO H,WANG F Y,et al.Preparation of closed-cell Mg foams using SiO2-coated CaCO3 as blowing agent in atmosphere[J].Transactions of Nonferrous Metals Society of China,2013,23(6):1832-1837.
[38]法文君,王威,魏亚君,等.具有核壳结构的纳米CaCO3@SiO2的制备与表征[J].化工新型材料,2012,40(5):71-73.
FA W J,WANG W,WEI Y J,et al.Preparation and characterization of CaCO3@SiO2 nanoparticles with core-shell structure[J].New Chemical Materials,2012,40(5):71-73.
[39]朱天孝,徐林冲,朱勇,等.CaCO3@SiO2的制备及其壳层SiO2生长动力学分析[J].中国粉体技术,2022,28(4):43-53.
ZHU T X,XU L C,ZHU Y,et al.Preparation of CaCO3@SiO2 and analysis of growth kinetics of SiO2 shell[J].China Powder Science and Technology,2022,28(4):43-53.
[40]王宪伟,郑松玲,庹文喜,等.一种轻质碳酸钙二氧化硅复合材料的制备方法:202010470749.8[P].2020-09-01.
WANG X W,ZHENG S L,TUO W X,et al.A preparation method of light calcium silica composite:202010470749.8[P].2020-09-01.
[41]吴嵘,吴素芳.包硅改性纳米碳酸钙应用于高温CO2吸附的性能[J].化工学报,2006,57(7):1722-1726.
WU R,WU S F.Performance of nano-CaCO3 coated with SiO2 on CO2 adsorption at high temperature[J].CIESC Journal,2006,57(7):1722-1726.
[42]雅克布·A.具有增加的表面积和中孔率的二氧化硅涂覆的碳酸钙的制备:201880079859.2[P].2020-07-24.
JACOB·A.Preparation of silica coated calcium carbonate with increased surface area and mesoporous ratio:201880079859.2[P].2020-07-24.
[43]MORSY F A,EL-SHEIKH S M,BARHOUM A.Nano-silica and SiO2/CaCO3 nanocomposite prepared from semi-burned rice straw ash as modified papermaking fillers[J].Arabian Journal of Chemistry,2019,12(7):1186-1196.
[44]LIU M,KANG M,CHEN K X,et al.Synthesis and luminescent properties of CaCO3:Eu3+@SiO2 phosphors with core-shell structure[J].Applied Physics A:Materials Science &Processing,2018,124(3):249.
[45]马翠翠,陈雪梅.核-壳结构纳米CaCO3/SiO2复合粒子的制备[J].化学世界,2010,51(4):196-199,213.
MA C C,CHEN X M.Preparation of Nanometer CaCO3/SiO2 Composite Particles with Core-shell Structure[J].Chemical World,2010,51(4):196-199,213.
[46]郭奋,吴海霞,刘润静,等.纳米碳酸钙耐酸性处理、表征及其在阳极电泳漆中的应用[J].涂料工业,2003,33(1):1-4,54.
GUO F,WU H X,LIU R J,et al.Acid resistant surface treatment and characterization of nano-calcium carbonate and its application in anodic electrodeposition paint[J].Paint &Coatings Industry,2003,33(1):1-4,54.
[47]于岩,曹若丹,庄赞勇.一种碳酸钙/二氧化硅纳米管的无模板一步合成调控方法:202010920551.5[P].2020-11-20.
YU Y,CAO R D,ZHUANG Z Y.A templateless one-step synthesis control method for calcium carbonate/silica nanotubes:202010920551.5[P].2020-11-20.
[48]范佳晨.一种碳酸钙-二氧化硅复合粉末的制备方法:201710730524.X[P].2019-03-05.
FAN J C.A preparation method of calcium carbonate silica composite powder:201710730524.X[P].2019-03-05.
[49]MA Y T,TIAN P,BOUNMYXAY M,et al.Calcium carbonate@silica composite with superhydrophobic properties[J].Molecules,2021,26(23):7180.
[50]CHEN Y R,YU H J,YI L Y,et al.Preparation of ground calcium carbonate-based TiO2 pigment by a two-step coating method[J].Powder Technology,2018,325:568-575.
[51]WANG H M,CHEN Y Z,ZHANG Z J.Enhanced ink-absorption performance of inkjet printing paper-based patterns with core-shell-structure CaCO3@SiO2 pigments[J].Nordic Pulp &Paper Research Journal,2019,34(4):525-533.
[52]GAMELAS J A F,LOURENCO A F,FERREIRA P J.New modified filler obtained by silica formed by sol-gel method on calcium carbonate[J].Journal of Sol-Gel Science and Technology,2011,59(1):25-31.
[53]LOURENCO A F,GAMELAS J A F,ZSCHERNECK C,et al.Evaluation of silica-coated PCC as new modified filler for papermaking[J].Industrial &Engineering Chemistry Research,2013,52(14):5095-5099.
[54]LOURENCO A F,GAMELAS J A F,FERREIRA P J.Increase of the filler content in papermaking by using a silica-coated PCC filler[J].Nordic Pulp &Paper Research Journal,2014,29(2):240-245.
[55]KONG H S,KIM B J,KANG K S.Synthesis of CaCO3-SiO2 composite using CO2 for fire retardant[J].Materials Letters,2019,238:278-280.
[56]MUHAMMUD A M,GUPTA N K.Nanostructured SiO2 material:synthesis advances and applications in rubber reinforcement[J].RSC Advances,2022,12(29):18524-18546.
[57]张周赫,张忆,李春山,等.白炭黑合成工艺研究[J].无机盐工业,2016,48(11):49-51.
ZHANG Z H,ZHANG Y,LI C S,et al.Study of preparation process of white carbon black[J].Inorganic Chemicals Industry,2016,48(11):49-51.
[58]HYDE E D E R,SEYFAEE A,NEVILLE F,et al.Colloidal silica particle synthesis and future industrial manufacturing pathways:a review[J].Industrial &Engineering Chemistry Research,2016,55(33):8891-8913.
[59]LI X,LEI Z,QU J,et al.Separation of copper from nickel in sulfate solutions by mechanochemical activation with CaCO3[J].Separation and Purification Technology,2017,172:107-112.
[60]QU J,ZHANG Q,LI X,et al.Mechanochemical approaches to synthesize layered double hydroxides:a review[J].Applied Clay Science,2016,119:185-192.
[61]FUENTES A F,TAKACS L.Preparation of multicomponent oxides by mechanochemical methods[J].Journal of Materials Science,2012,48(2):598-611.
[62]FISS B G,RICHARD A J,DOUGLAS G,et al.Mechanochemical methods for the transfer of electrons and exchange of ions:inorganic reactivity from nanoparticles to organometallics[J].Chemical Society Reviews,2021,50(14):8279-8318.
[63]PATEL C M,CHAKRABORTY M,MURTHY Z V P.Enhancement of stirred media mill performance by a new mixed media grinding strategy[J].Journal of Industrial and Engineering Chemistry,2014,20(4):2111-2118.
[64]LEONARDI M,VILLACAMPA M,MENENDEZ J C.Multicomponent mechanochemical synthesis[J].Chemical Science,2018,9(8):2042-2064.
[65]MICHALCHUK A A L,EMMERLING F.Time-resolved in-situ monitoring of mechanochemical reactions[J].Angewandte Chemie-International Edition,2022,61(21):e202117270.
[66]TSUZUKI T.Mechanochemical synthesis of metal oxide nanoparticles[J].Communications Chemistry,2021,4(1):143.
[67]FENG L,LI S H,LI Y S,et al.Super-hydrophobic surfaces:from natural to artificial[J].Advanced Materials,2002,14(24):1857-1860.
[68]ZHENG Y M,GAO X F,JIANG L.Directional adhesion of superhydrophobic butterfly wings[J].Soft Matter,2007,3(2):178-182.
[69]LIU K S,DU J X,WU J T,et al.Superhydrophobic gecko feet with high adhesive forces towards water and their bio-inspired materials[J].Nanoscale,2012,4(3):768-772.
[70]TIAN Y,SU B,JIANG L.Interfacial material system exhibiting superwettability[J].Advanced Materials,2014,26(40):6872-6897.
[71]GU Y,ZHANG W,MOU J,et al.Research progress of biomimetic superhydrophobic surface characteristics,fabrication,and application[J].Advances in Mechanical Engineering,2017,9(12):1687814017746859.
[72]郭永刚,张鑫,耿铁,等.超疏水表面耐久性能的研究进展[J].中国表面工程,2018,31(5):63-72.
GUO Y G,ZHANG X,GENG T,et al.Research progress on durability of superhydrophobic surfaces[J].China Surface Engineering,2018,31(5):63-72.
[73]JEEVAHAN J,CHANDRASEKARAN M,BRITTO J G,et al.Superhydrophobic surfaces:a review on fundamentals,applications,and challenges[J].Journal of Coatings Technology and Research,2018,15(2):231-250.
[74]WANG Z,YANG A,TAN X,et al.A veil-over-sprout micro-nano PMMA/SiO2 superhydrophobic coating with impressive abrasion,icing,and corrosion resistance[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects,2020,601:124998.
[75]WANG S,LIU K,YAO X,et al.Bioinspired surfaces with superwettability:new insight on theory,design,and applications[J].Chemical Reviews,2015,115(16):8230-8293.
[76]SCARRATT L R J,STEINER U,NETO C.A review on the mechanical and thermodynamic robustness of superhydrophobic surfaces[J].Advances in Colloid and Interface Science,2017,246:133-152.
[77]TAN X,WANG Y,HUANG Z,et al.Facile fabrication of a mechanical,chemical,thermal,and long-term outdoor durable fluorine-free superhydrophobic coating[J].Advanced Materials Interfaces,2021,8(11):2002209.
[78]HE Y H,LI H B,OU L G,et al.Preparation and characterisation of water-based aluminium pigments modified with SiO2 and polymer brushes[J].Corrosion Science,2016,111:802-810.
[79]CAI H H,GAO L Z,CHEN L,et al.An effective,low-cost and eco-friendly method for preparing UV resistant silk fabric[J/OL].Journal of Natural Fibers,2021.https://doi.org/10.1080/15440478.2021.1875362
[80]WANG J,SUN S J,DING H,et al.Preparation of a composite photocatalyst with enhanced photocatalytic activity:smaller TiO2 carried on SiO2 microsphere[J].Applied Surface Science,2019,493:146-156.
[81]赵丽娜.碳酸钙的形貌控制及表面改性研究[D].长春:吉林大学,2009.
ZHAO L N.Morphology control and surface modification of calcium carbonate[D].Changchun:Jilin University,2009.
[82]崔程琳.碳酸钙表面包覆二氧化硅复合颗粒的制备与表征[D].北京:中国地质大学(北京),2015.
CUI C L.Preparation and characterization of silica coated calcium carbonate composite[D].Beijing:China University of Geosciences (Beijing),2015.
[83]YU Y,ZHANG J,WANG H,et al.Silanized silica-encapsulated calcium carbonate@natural rubber composites prepared by one-pot reaction[J].Polymers,2020,12(11):2668.
[84]SHARMA P,PRAKASH J,KAUSHAL R.An insight into the green synthesis of SiO2 nanostructures as a novel adsorbent for removal of toxic water pollutants[J].Environmental Research,2022,212:113328.
[85]PANAYOTOV D,YATES J T.Bifunctional hydrogen bonding of 2-chloroethyl ethyl sulfide on TiO2-SiO2 powders[J].Journal of Physical Chemistry B,2003,107(38):10560-10564.
[86]YANG Y,LI Y J,YAN X Y,et al.Development of thermochemical heat storage based on CaO/CaCO3 cycles:a review[J].Energies,2021,14(20):6847.
[87]YUAN Y,LI Y J,ZHAO J L.Development on thermochemical energy storage based on CaO-based materials:a review[J].Sustainability,2018,10(8):2660.
[88]MA Z,LI Y,ZHANG W,et al.Energy storage and attrition performance of limestone under fluidization during CaO/CaCO3 cycles[J].Energy,2020,207:118291.
[89]SUN H,LI Y,YAN X,et al.CaO/CaCO3 thermochemical heat storage performance of CaO-based micrometre-sized tubular composite[J].Energy Conversion and Management,2020,222:113222.
[90]SHUI M,YUE L H,HUA Y M,et al.The decomposition kinetics of the SiO2 coated nano-scale calcium carbonate[J].Thermochimica Acta,2002,386(1):43-49.
[91]KUCHARCZYK A,NAPLOCHA K,KACZMAR J W,et al.Current status and recent developments in porous magnesium fabrication[J].Advanced Engineering Materials,2018,20(1):1700562.
[92]YANG D H,HUR B Y,YANG S R.Study on fabrication and foaming mechanism of Mg foam using CaCO3 as blowing agent[J].Journal of Alloys and Compounds,2008,461(1/2):221-227.
[93]YANG D,CHEN J,CHEN W,et al.Fabrication of cellular Zn-Mg alloy foam by gas release reaction via powder metallurgical approach[J].Journal of Materials Science &Technology,2017,33(10):1141-1146.