锂离子电池作为一种高效便捷亦可重复充放电的绿色电源, 近年来已被广泛应用于便携式通信工具和电动车中[1-3]。 具有橄榄石结构的磷酸铁锂(LiFePO4)电池的工作电压适中, 电容量大, 放电功率高, 安全性好, 环保性高[4-5]。 LiFePO4可以通过液相法[6]、 固相法[7]、 共沉淀法[8]和碳热还原法[9]等成熟的批量化工艺流程进行制造。
LiFePO4正极材料充放电的过程实质是具有异位结构的LiFePO4和FePO4两相的相互转变[10]。 LiFePO4电池经多次充、 放电循环后,一方面电解液容易降解, 导致电解液匮乏, 不能完全浸润电极片,电极反应不能完全进行,电池容量产生损耗[11-12];另一方面,多次循环后正极材料中的锂与负极材料中的石墨容易形成 LiC6枝晶,致使放电后在负极的锂离子不能全部回到正极而使得正极材料处于缺锂状态[13],因此,LiFePO4电池失效的主要原因为电解液的降解和正极材料中锂的损失。
LiFePO4电池正极材料在失效过程中发生物理和化学性质(简称理化性质)的变化[14],导致LiFePO4电池的平均使用年限不长(小型乘用车4~8 a,大型商用车3~5 a)[15],并且存在失效电极材料的回收和再利用问题。三元锂电池回收技术[16-17]只能分离、提纯正极材料中含有的Co、 Mn等贵重金属,如果将该技术用于LiFePO4电池的回收将失去经济上的优势,因此,对LiFePO4电池的回收应着眼于正负极电极材料全组分、高位化的综合利用[18-19]。梁力勃等[20]将失效LiFePO4电池洗涤、烘干后进行剥蚀处理,得到目标前驱体后再加入葡萄糖,然后在氮气氛围中进行高温焙烧得到再生LiFePO4产物,此方法仅能对废料进行简单处理,虽然容易实现批量生产,但是所再生的LiFePO4产物性能欠佳。王子璇等[21]采用湿法冶金技术处理失效的LiFePO4电极材料,通过向电解液中加入氨水得到主产物二水合磷酸铁和磷酸锂(副产物仅有磷酸二氢铵),该方法可以较为绿色、高效地实现对Fe和Li元素的回收,但磷酸酸性较弱,浸出效率有限。
综上,本文中采用仪器分析和表征方法,对失效前、后的LiFePO4正极材料进行对比,研究失效过程中LiFePO4正极材料的理化性质及微观形貌的变化,为后续研究废弃LiFePO4电池电极材料的分选、纯化以及电极材料的回收和再利用提供理论依据与数据基础。
1 实验
1.1 试样制备

(a)LiFePO4电池

(b)正极片
图1 LiFePO4电池和正极片
Fig.1 LiFePO4 battery and cathode plate
LiFePO4电池和正极片如图1所示,实验所用失效前、 后的LiFePO4电池来自珠海中力新能源科技有限公司。测试制样时使用的化学纯C2H5OH来自国药集团化学试剂有限公司。
将LiFePO4电池模组置于质量分数为10%的NaCl溶液中浸泡48 h, 去除电池模组内可能残余的剩电, 然后放入干燥箱中进行干燥; 用工具拆开模组外壳后, 从正极片上刮下LiFePO4正极材料进行研磨; 用孔径分别为0.045、 0.074 μm标准试验筛进行筛选; 将失效前LiFePO4正极材料粉末中位粒径为>0.045~0.074 μm的记为S1, 中位粒径≤0.045 μm的记为S2; 将失效后LiFePO4正极材料粉末中粒径为>0.045~0.074 μm的记为S3, 中位粒径≤0.045 μm的记为S4。
1.2 测试与表征
实验仪器如表1所示。采用仪器对失效后的正极片、失效前和失效后的未过筛颗粒以及4种粉末颗粒进行测试和表征,测试条件如表2所示。
2 结果与分析
2.1 XRF分析
在温度为25 ℃、 空气相对湿度为65%的测试环境下,对失效前、 后LiFePO4电池正极材料的未过筛颗粒进行X射线荧光光谱分析。失效前、 后未过筛颗粒的组分如表3所示。 由表3可知,失效后LiFePO4电池正极材料中含有大量的Fe、 P、 Ni, 少量的Cu、 Co和微量的F元素。
表1 实验仪器
Tab.1 Experimental apparatus
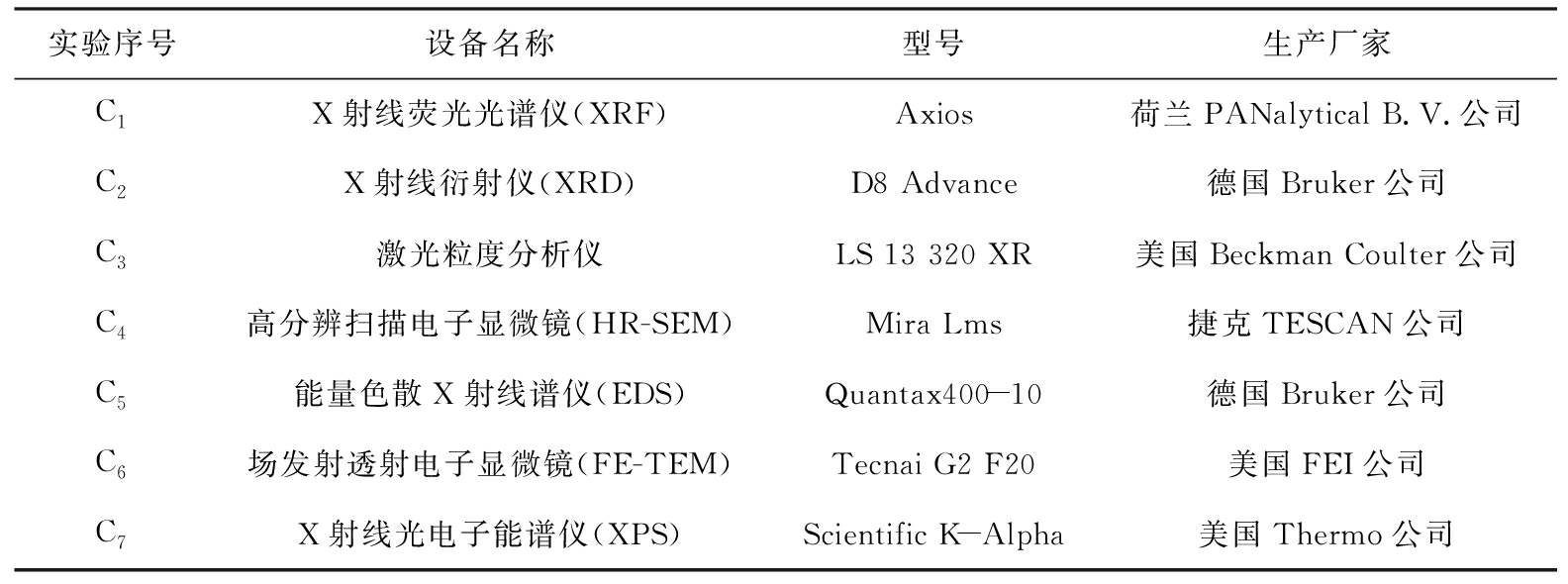
实验序号设备名称型号生产厂家C1X射线荧光光谱仪(XRF)Axios荷兰PANalytical B.V.公司C2X射线衍射仪(XRD)D8 Advance德国Bruker公司C3激光粒度分析仪LS 13 320 XR美国Beckman Coulter公司C4高分辨扫描电子显微镜(HR-SEM)Mira Lms捷克TESCAN公司C5能量色散X射线谱仪(EDS)Quantax400-10德国Bruker公司C6场发射透射电子显微镜(FE-TEM)Tecnai G2 F20美国FEI公司C7X射线光电子能谱仪(XPS)Scientific K-Alpha美国Thermo公司
表2 测试条件
Tab.2 Test conditions
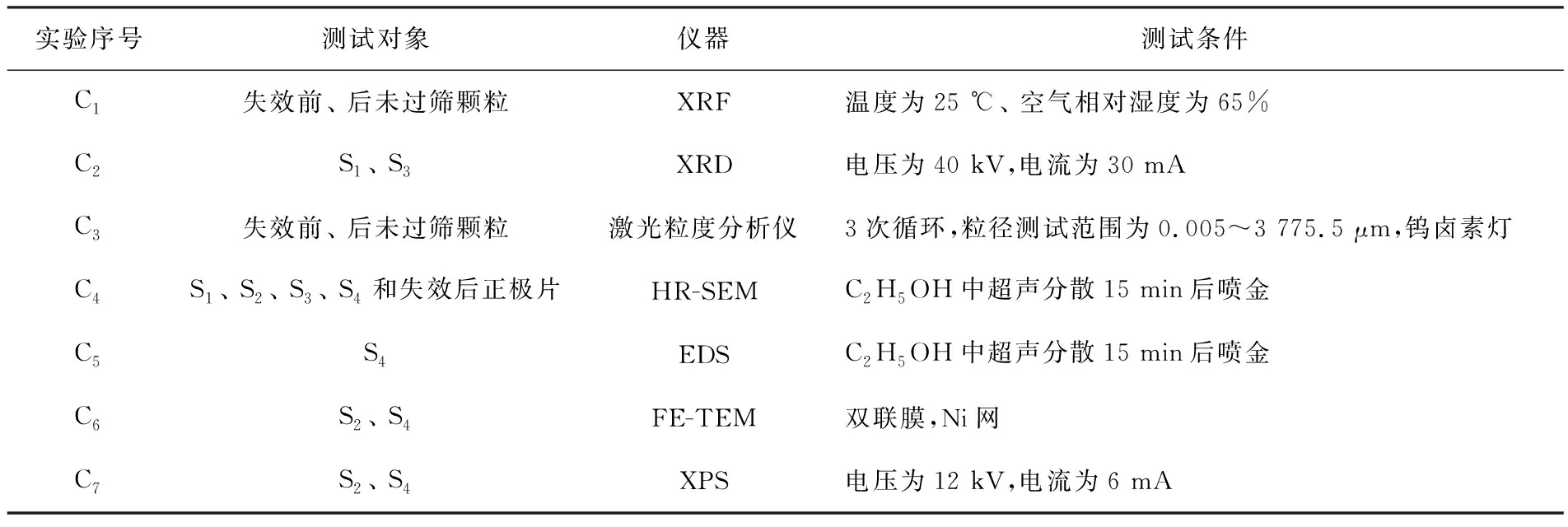
实验序号测试对象仪器测试条件C1失效前、 后未过筛颗粒XRF温度为25 ℃、 空气相对湿度为65%C2S1、 S3XRD电压为40 kV,电流为30 mAC3失效前、 后未过筛颗粒激光粒度分析仪3次循环,粒径测试范围为0.005~3 775.5 μm,钨卤素灯C4S1、 S2、 S3、 S4和失效后正极片HR-SEMC2H5OH中超声分散15 min后喷金C5S4EDSC2H5OH中超声分散15 min后喷金C6S2、 S4FE-TEM双联膜,Ni网C7S2、 S4XPS电压为12 kV,电流为6 mA
表3 失效前、 后未过筛颗粒的组分
Tab.3 Components of unsieved particles before and after failure %
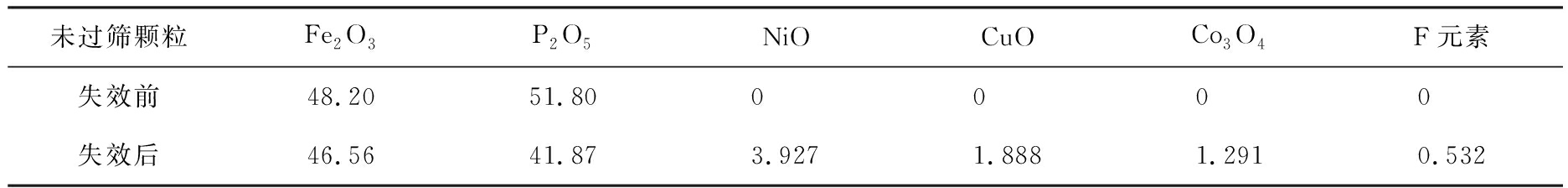
未过筛颗粒Fe2O3P2O5NiOCuOCo3O4F元素失效前48.2051.800 0 0 0 失效后46.5641.873.9271.8881.2910.532
2.2 XRD图谱
为了研究LiFePO4电池正极材料在长期使用后的晶型变化, 采用X射线衍射仪对失效前、 后LiFePO4电池正极材料粉末S1和S3进行表征。 失效前、 后颗粒试样S1和S3的XRD谱图如图2所示。 由图2可知, 将S3与标准卡片进行对比后可以基本确定正极材料的晶相结构未发生明显改变, 仍保持为LiFePO4, 但是在2θ为18.7°、 32.67°、 44.34°处出现了一组较强的杂峰, 寻峰结果表明可能是CoC2O4(草酸钴)。 结合表3结果进行分析发现, 由于LiFePO4本身的能量密度较低, 而钴酸锂(LiCoO2)的能量密度相对较高, 因此生产厂家在考虑成本许可的情况下, 在LiFePO4正极材料中混配少量LiCoO2可以提高电池的能量密度。
2.3 粒度分析
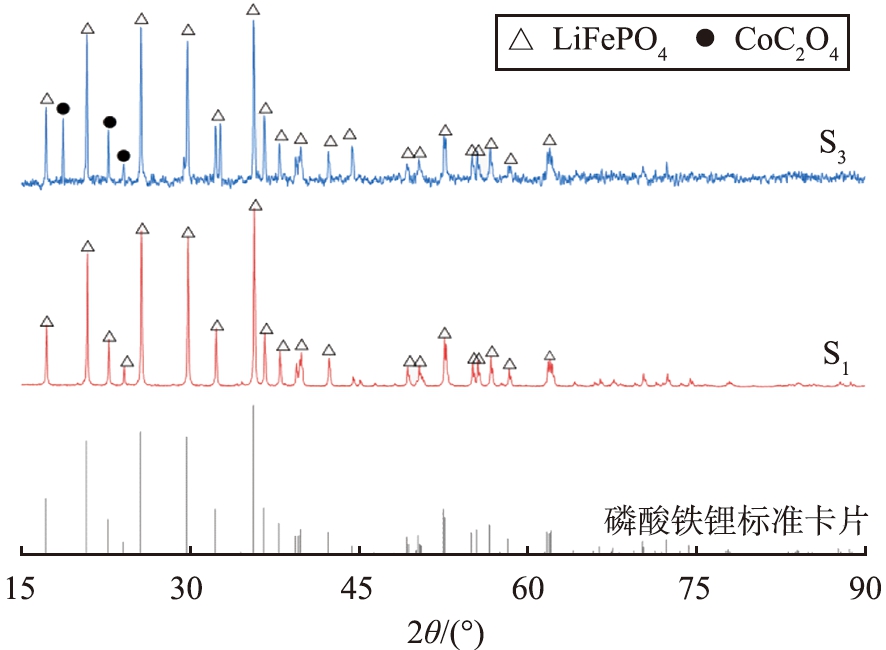
图2 失效前、 后颗粒试样S1和S3的XRD谱图
Fig.2 XRD patterns of particle samples S1 and S3 before and after failure
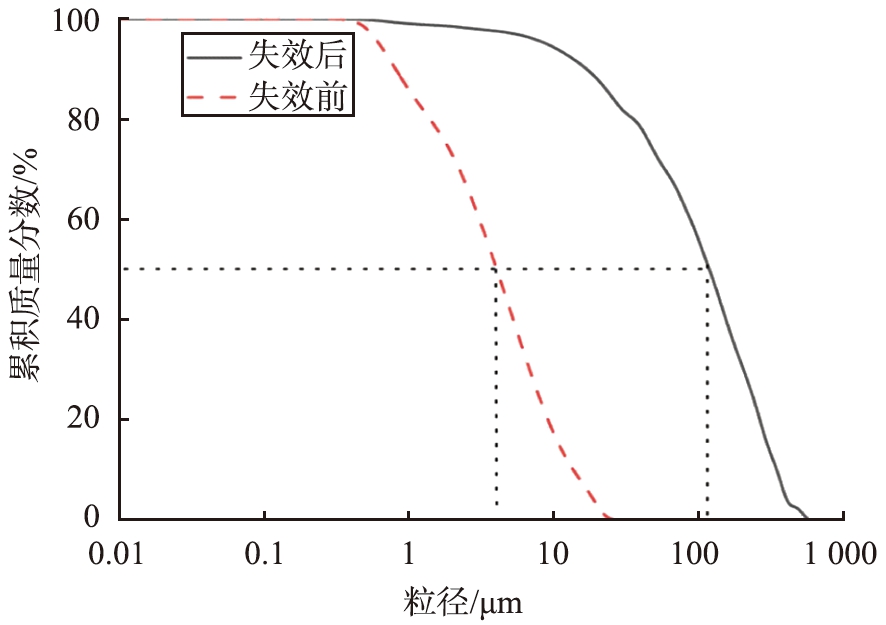
图3 失效前、 后未过筛颗粒的粒度累积分布曲线
Fig.3 Cumulative size distribution curves of unsieved
particles before and after failure
采用激光粒度分析仪对失效前、 后未过筛的颗粒进行3次粒度分析, 取3次测量的平均值绘制曲线。 失效前、 后未过筛颗粒的粒度累积分布曲线如图3所示。 从图3可知, 失效前未过筛颗粒的粒度分布较为均匀, 中位粒径约为5.62 μm, 整体粒度较小; 失效后LiFePO4未过筛颗粒的粒度分布范围为1~600 μm, 颗粒粒度差异较大, 中位粒径为155.07 μm, 颗粒整体粒度较大, 且大部分颗粒的粒径大于100 μm, 远大于失效前的。 这是由于受黏结剂和电解液以及长期充、 放电的影响, LiFePO4正极材料在失效过程中颗粒产生了团聚、 膨胀, 降低了正极材料的电化学性能。
2.4 HR-SEM图像

(a)放大800倍

(b)放大5 000倍

(c)放大10 000倍
图像
Fig.4 HR-SEM images of LiFePO4 battery cathode plate after failure at different magnification
高分辨扫描电子显微镜将失效后LiFePO4电池正极片进行扫描, 不同放大倍数下失效后LiFePO4电池正极片的HR-SEM图像如图4所示。 由图4(a)、 (b)可以看出, 即使经过长期使用后, LiFePO4电池正极片上的颗粒之间仍以紧密、 平整的状态结合, 但本来平整地涂覆于正极铝箔表面的LiFePO4材料表面出现了不规则的波浪状缺陷和坑状凹陷; 由图4(c)白圈处可见, 在凹陷处边缘有条带状物质黏连。 LiFePO4电池在长期充放电循环使用过程中, 正极材料与有机电解液发生反应, 导致正极材料颗粒间的联结破裂后使得颗粒无序化, 进而导致集流体表面出现不规则波浪状缺陷或坑状凹陷。
失效前、 后中位粒径>0.045~0.074 μm的颗粒试样S1和S3的HR-SEM图像如图5所示。由图5可以看出,LiFePO4正极材料由失效前的颗粒S1松散、 均匀和平铺,失效后的颗粒S3变得黏连、 杂乱和团聚。

(a) S1(放大5 000倍)

(b) S3(放大5 000倍)
图像
Fig.5 HR-SEM images of S1 and S3
失效前、 后中位粒径≤0.045μm的颗粒试样S2和S4的HR-SEM图像如图6所示。由图6可以看出,与S2相比,S4颗粒表面的包覆纹路随着锂的沉积而消失;同时,由于长期发生的电化学反应,S4粒表面产生裂纹,因此大颗粒破碎成更细碎的小颗粒并黏附在剩余大颗粒表面。

(a) S2(放大50 000倍)

(d) S4(放大50 000倍)
图像
Fig.6 HR-SEM images of S2 and S4
综上,在锂离子电池充放电过程中,电极材料与电解液会在固液两相界面上发生复杂的化学反应,生成一层覆盖于正极材料表面的钝化膜,该钝化膜虽是电子绝缘体但却是锂离子的良导体,锂离子可以自由地嵌入和脱出,该钝化膜被称作正极电解质界面膜(cathode electrolyte interface, CEI)。在长期使用过程中,由于PVDF黏结剂的侵蚀和电解液的浸泡作用,因此LiFePO4正极材料颗粒间的原有连接发生破裂,并发生化学反应生成非晶型盐,原颗粒由类球形转变为不规则外形的颗粒并且互相黏连。在长时间地进行充放电后,锂离子会完全进入LiFePO4电池正极材料原有的橄榄石结构,使LiFePO4正极材料变形和塌陷,最终导致集流体上的正极材料膨胀,晶体结构发生改变。
2.5 EDS能谱
使用能量色散X射线谱仪对S4进行面扫描分析,S4的F元素分布和EDS能谱图如图7所示。由图7(a)、 (b)可以看出,代表黏结剂PVDF的F元素主要分布在颗粒的边缘,光点分布较为均匀分散,表明S4颗粒表面即使经过破碎研磨以后仍然广泛存在PVDF黏结剂。由图7(c)可以看出,黏结剂的相对含量处在较低水平,残余的PVDF一方面使得正极材料颗粒团聚成大粒级颗粒,另一方面也会影响颗粒表面的疏水性,导致颗粒在后续浮选富集回收过程中无法正常上浮,影响浮选效率。
2.6 FE-TEM图像

(a)S4颗粒形貌图

(b)F元素分布
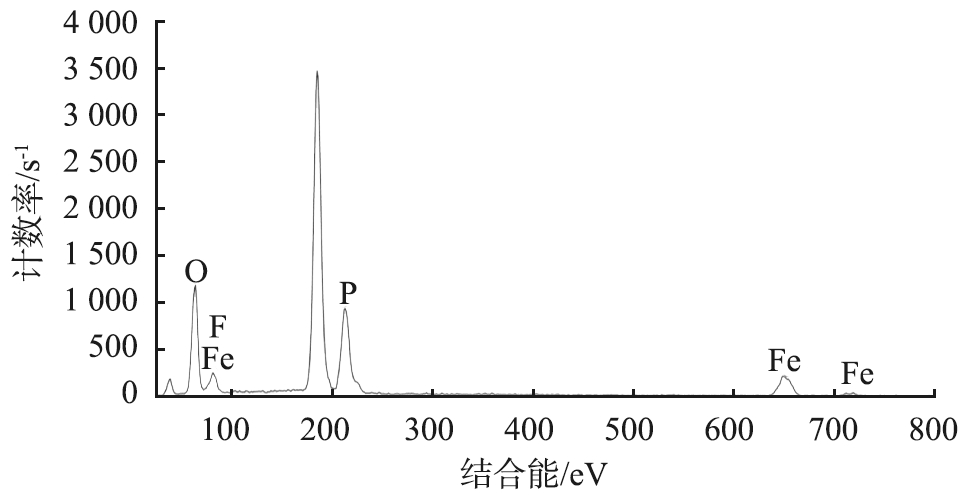
(e)EDS 能谱图
图7 S4中F元素分布和EDS能谱图
Fig.7 Distribution of F element and EDS energy spectrum in S4
为了研究LiFePO4电池正极材料的晶型变化,采用场发射透射电子显微镜对失效前、 后的颗粒试样S2和S4进行表征。 S2和S4的FE-TEM图像如图8所示。 由图8可见, S2和S4表面都有层状结构的物质存在;S2表面存在厚度约2~10 nm的连续层状结构,这是为了增强电化学性质而使用表面改性手段包覆的无定型碳;S4表面存在厚度约20 nm的非连续层状膜结构,结合EDS能谱与XPS谱图分析可以确定这是黏结剂PVDF形成的有机层状结构。

(a)S2

(b)S4
图像
Fig.8 FE-TEM images of S2 and S4
2.7 XPS谱图
为研究LiFePO4电池正极材料失效前、 后的基团变化, 采用X射线光电子能谱仪对颗粒试样S2和S4进行表征。 S2和S4中C元素的XPS能谱图如图9所示。 由图9可见, 将S2、 S4的C表征曲线与XPS吸收峰数据库进行对比可以确定, S4曲线中拟合出的结合能为284.39、 286.13、 284.77、 288.98、 290.80 eV处的吸收峰分别对应的基团为炭黑、 —CF2CH2—、 C—C或C—H、 O—C![]() O、 —CF2CH2—。 在实际电池组装过程中, —CF2CH2—和—CF2CH2—对应为正极片表面的黏结剂PVDF, C—C或C—H、 O—C
O、 —CF2CH2—。 在实际电池组装过程中, —CF2CH2—和—CF2CH2—对应为正极片表面的黏结剂PVDF, C—C或C—H、 O—C![]() O对应有机电解液, 常见的有机电解液为乙烯碳酸酯(EC)、 二甲基碳酸酯(DMC)和二乙基碳酸酯(DEC)。 结合能为284.77 eV处的基团为O—C
O对应有机电解液, 常见的有机电解液为乙烯碳酸酯(EC)、 二甲基碳酸酯(DMC)和二乙基碳酸酯(DEC)。 结合能为284.77 eV处的基团为O—C![]() O, 也验证了XRD图谱中存在CoC2O4。
O, 也验证了XRD图谱中存在CoC2O4。
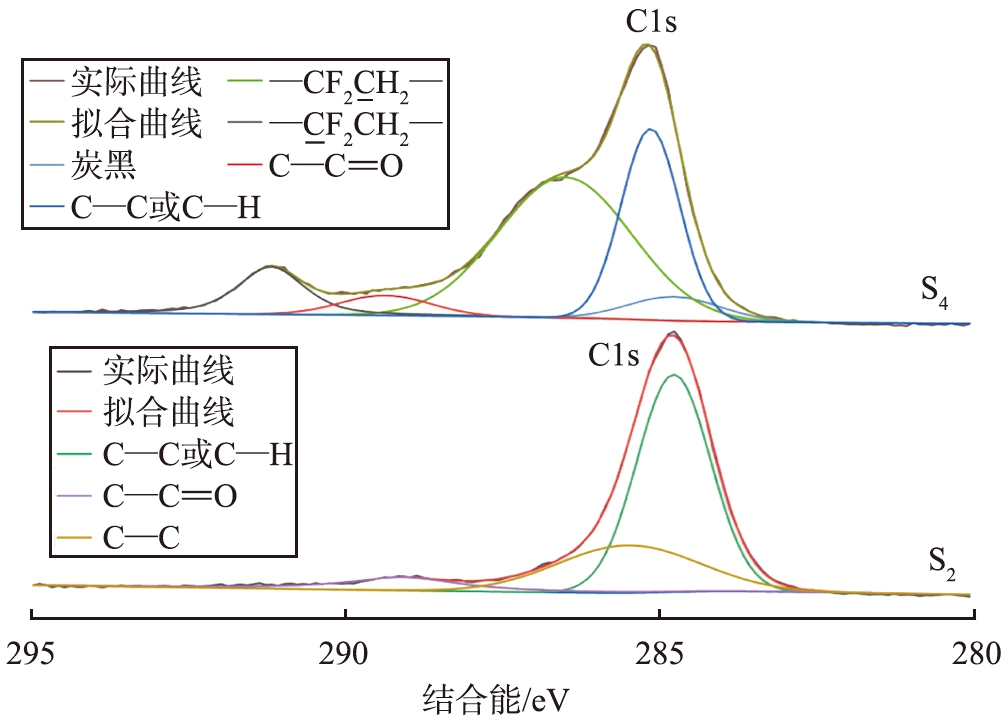
图9 S2和S4中C元素的XPS谱图
Fig.9 XPS spectrum of C in S2 and S4
S2和S4中Fe元素的XPS谱图如图10所示。由图10可知,将S2、 S4中的Fe表征曲线与XPS吸收峰数据库进行对比后可以确定,Fe2p3/2和Fe2p1/2分裂之间的能量差ΔE约为13.6 eV,符合Fe2+、 Fe3+的XPS图谱中存在双峰的原则, S2、 S4中在710.10、 723.58 eV处的吸收峰均来自LiFePO4中的Fe2+。 S2中711.32、 724.92 eV和S4中711.59、 725.21 eV处的Fe3+吸收峰的存在形式为Fe2O3,推测可能是失效前、 后正极材料粉末在储存、 测试过程中与空气中的氧气发生氧化反应由Fe2+氧化变成Fe3+; S4中713.07、 726.67 eV处的吸收峰则是由于LiFePO4经过长期使用发生电化学反应后生成的FePO4中Fe3+的离子吸收峰;S4中715.90、 729.50 eV处则是Fe2p3/2的卫星峰。
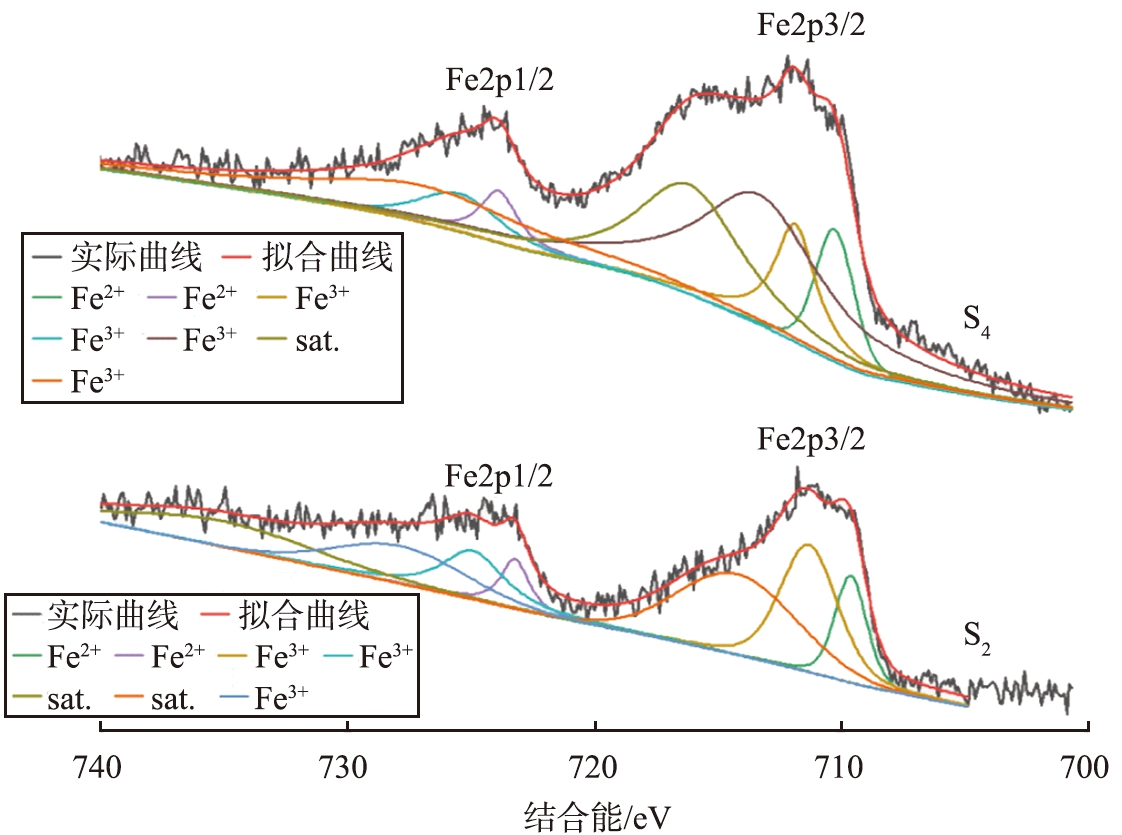
图10 S2和S4中Fe元素的XPS谱图
Fig.10 XPS spectrum of Fe in S2 and S4
3 结论
1)失效后LiFePO4电池正极材料中含有大量的Fe、 P、 Ni, 少量的Cu、 Co和微量的F元素,晶相结构未发生明显改变;在LiFePO4正极材料中混配少量LiCoO2可以提高电池的能量密度。
2)LiFePO4电池正极片失效后表面出现了不规则的波浪状缺陷和坑状凹陷; 在失效过程中, LiFePO4正极材料颗粒产生了团聚和膨胀, 降低了正极材料的电化学性能; 失效后颗粒的表面产生裂纹, 大颗粒破碎成更细碎的小颗粒, 小颗粒变得黏连、 杂乱和团聚, 失效前颗粒表面的包覆纹路随着锂的沉积而消失。
3)失效前LiFePO4正极材料颗粒表面包覆厚度为2~10 nm的连续层状无定型碳;失效后LiFePO4正极材料颗粒表面出现厚度为20 nm的非连续层状膜结构PVDF。代表黏结剂的F元素主要分布在失效后LiFePO4颗粒的边缘,光点分布较为均匀分散,F元素相对含量较低。残余的PVDF会影响颗粒表面的疏水性,影响浮选效率。
4)失效后LiFePO4电池正极材料中C的主要基团存在形式为炭黑、 —CF2CH2—、 C—C与C—H、 O—C![]() O和—CF2CH2—; Fe主要以Fe2+和Fe3+形式存在。
O和—CF2CH2—; Fe主要以Fe2+和Fe3+形式存在。
[1]JAI K, RANA R, NEIBER C D, JAEWON P, et al. Recent progress in sustainable recycling of LiFePO4-type lithium-ion batteries:strategies for highly selective lithium recovery[J]. Chemical Engineering Journal, 2022, 431: 133993.
[2]张伟刚, 何亚群, 张涛, 等. 废弃锂离子电池富钴粉体可浮性的改善[J]. 中国粉体技术, 2016, 22(1): 23-27.
[3]WALVEKAR H, BELTRAN H, SRIPAD S, et al. Implications of the electric vehicle manufacturers’ decision to mass adopt lithium-iron phosphate batteries[J]. IEEE Access, 2022, 10: 63834-63843.
[4]王韵珂, 延卫, 万邦隆, 等. 废旧锂电池磷酸铁锂正极材料回收工艺研究进展[J]. 云南化工, 2022, 49(6): 1-6.
[5]SHAO J Y, LI X R, WEUI J L, et al. Synthesis of iron phosphate and their composites for lithium/sodium ion batteries[J]. Advanced Sustainable Systems, 2018, 2: 1700154.
[6]JOEY C Y J, SUI P C, ZHANG J J. A review of recycling spent lithium-ion battery cathode materials using hydrometallurgical treatments[J]. Journal of Energy Storage, 2021, 35: 102217.
[7]CAO Z X, ZHU G S, ZHANG R R, et al. Biological phytic acid guided formation of monodisperse large-sized carbon LiFePO4/graphene composite microspheres for high-performance lithium-ion battery cathodes[J]. Chemical Engineering Journal, 2018, 351: 382-390.
[8]PADHI A K, NANJUNDASWAMY K S, GOODENOUGH J B. Phospho-olivines as positive-electrode materials for rechargeable lithium batteries[J]. Journal of the Electrochemical Society, 1997, 144(4): 1188-1194.
[9]JIANG D P, ZHANG X J, LU S G, et al. Research on process of preparation and performance of iron phosphate as precusor of lithium iron phosphate[J]. Rare Metals, 2011, 30: 52-54.
[10]何栋. 磷酸铁锂电池的工作原理及其在通信基站中的应用[D]. 南京: 南京邮电大学, 2018.
[11]任冬燕, 李晶, 宋月丽. LiFePO4锂离子电池容量的衰减机制[J]. 中国粉体技术, 2013, 19(1): 68-71.
[12]NING G, HARAN B, POPOV B N. Capacity fade study of lithium-ion batteries cycled at high discharge rates[J]. J Power Sources, 2003, 117(1): 160-169.
[13]贺浩. 磷酸铁锂18650动力键锂离子电池失效机理及动态脱嵌锂键机理研究[D]. 长沙: 湖南大学, 2016.
[14]WU Y F, CHONG S K, LIU Y N, et al. Review on Li-insertion/extraction mechanisms of LiFePO4 cathode materials[J]. Chinese Journal of Structure Chemistry, 2018, 37(12): 2011-2023.
[15]FEDERICA F, MASSIMILIANA P, STEFANO P, et al. Lithium iron phosphate batteries recycling: an assessment of current status[J]. Critical Reviews in Environmental Science and Technology, 2021, 51: 2232-2259.
[16]JHA A K, JHA M K, KUMARI A, et al. Selective separation and recovery of cobalt from leach liquor of discarded Li-ion batteries using thiophosphinic extractant[J]. Sep Purif Technol, 2013, 104: 160-166.
[17]ZHU S, HE W Z, LI G M, et al. Recovery of Co and Li from spent lithium-ion batteries by combination method of acid leaching and chemical precipitation[J]. Trans Nonferrous Met Soc China, 2012, 22(9): 2274-2281.
[18]ZHOU L F, YANG D R, DU T, et al. The current process for the recycling of spent lithium-ion batteries[J]. Frontiers in Chemistry, 2020, 12: 578044.
[19]原晓菲, 钟睿, 洪若瑜, 等. 等离子体法制备及改性石墨烯粉体的研究进展[J]. 中国粉体技术, 2021, 27(5): 134-140.
[20]梁力勃, 杨生龙, 罗茂枭, 等. 高温固相法再生废旧磷酸铁锂电池正极材料[J]. 矿冶工程, 2021, 41(3): 120-128.
[21]王子璇, 李俊成, 李金东, 等. 废磷酸铁锂正极材料资源化回收工艺[J]. 储能科学与技术, 2022, 11(1): 45-52.