近年来,染料废水处理已经成为水处理行业的关注重点,其中,吸附法染料废水处理因具有低成本、操作简单灵活、高效率和环境友好等优点,脱颖而出[1-2]。罗丹明B(rhodamine B, RhB)是常用染料之一,对人体损害严重,可能导致皮肤和内脏充血、呼吸障碍、肠胃道损伤、致癌等[3-4],因此,寻找合适的吸附剂对RhB进行有效处理十分关键。处理RhB常用的吸附剂有沸石[5]、金属有机骨架(MOFs)[6]、活性炭[7]、六方氮化硼[8-9]等。沸石是一种广泛应用于气体分离和金属离子吸附的多孔材料,包括天然形式和合成形成,但其性能和适用性易受到各种因素的影响[5]。MOFs作为新型多孔化合物,具有比表面积大、物理化学性质稳定和结构易调控等特点,被广泛应用于吸附无机和有机污染物,但MOFs用于吸附RhB时,吸附时间长,掺杂原子后去除率仍较低[6]。活性炭是最常用的吸附剂之一,但对水中有机物的去除能力较差[7]。六方氮化硼(hexagonal boron nitride, h-BN)作为类石墨烯材料,具有与石墨烯相似的层状结构,由B原子和N原子交替组成六边形的原子平面层,层之间由范德华力相互作用结合在一起[8]。h-BN具有优异的绝缘性、抗氧化性和化学惰性,在处理组成复杂的废水时优势明显。h-BN具有较大的比表面积,能够为吸附提供更多的活性位点,可应用领域广泛[9]。
目前,关 h-BN吸附RhB的研究存在吸附去除率低、吸附时间较长、吸附条件范围窄等缺点。在水溶液体系中,由于h-BN的疏水特性不利于吸附亲水性染料,通常要对h-BN的表面进行改性。典型h-BN表面改性方法包括水热法[10]、超声分解法[11]、等离子体处理法[12]、球磨法[12]等。其中,球磨法具有操作简单、成本低、收率高、易大规模生产等优点[12],因此,本文中采用球磨法对h-BN进行剥离和表面改性。
另一种提高h-BN吸附性能的方法是改变形貌结构。二维六方氮化硼纳米片(BNNSs)比块状h-BN具有更大的比表面积,为吸附提供更多的活性位点。具有三维多孔结构的氮化硼微球在保留较大比表面积的同时,改善了二维BNNSs吸附后不易分离的问题。目前,制备氮化硼微球常见的方法主要有模板生长法和组装法。模板生长法是以模板为载体合成并控制材料尺寸、形状、结构、性质的方法,例如化学气相沉积法(chemical vapour deposition,CVD)[13]。组装一般是将二维纳米材料采用物理或化学的手段得到三维多孔结构的微球,例如冷冻干燥法[14]和喷雾干燥法[15]。冷冻干燥法存在制备时间长的问题;喷雾干燥法是将含有所需固体的溶液或者悬浮液分散在干燥热介质中,脱水后即可得到产品的方法,具有耗时短、操作简单等优点,被广泛应用于制备球形颗粒[15]。
本文中采用易分解铵盐对h-BN进行球磨改性处理,增强亲水性;在水溶液中经过高速搅拌后剥离得到BNNSs,亲水性将得到进一步提升;再通过喷雾干燥技术简单、快捷地得到功能化氮化硼微球,以增强对RhB的吸附效果和可利用性。同时,探讨RhB溶液质量浓度、温度和pH对功能化氮化硼微球吸附性能的影响。
1 实验
1.1 主要试剂、仪器
氢氧化钠(NaOH,分析纯)、聚乙烯醇(PVA,分析纯)(阿拉丁试剂(上海)有限公司);RhB(化学纯,上海恒远生物技术发展有限公司);浓盐酸(分析纯,北京化工厂);氮化硼(h-BN,质量分数≥99%,天元新材公司);去离子水(实验室自制)。
FA1004型电子分析天平(长沙湘平科技发展有限公司);DHG-9000型电热鼓风干燥箱(上海一恒科学仪器有限公司);KQ5200DE 型超声清洗器(昆山市超声仪器有限公司);78型磁力搅拌器(国华电器);HH-SJ型恒温水浴锅(上海丙林电子科技有限公司);SHB-Ⅱ型循环水式多用真空泵(博山源泉正恒工业泵厂);YXQM-4L型行星式球磨机(长沙米琪仪器设备有限公司);FJ300-SH型高速搅拌器/数显高速分散均质机(上海标本模型厂);YC-015型喷雾干燥机(上海雅程仪器设备有限公司);SMG-60-12型管式炉(河南三特炉业科技有限公司);Hitachi S-4700型扫描电子显微镜(SEM,株式会社日立制作所);Hitachi HT7700型透射电子显微镜(TEM,株式会社日立制作所);Nicolet-8700型傅里叶变换红外光谱仪(FTIR,美国Thermo公司);UV-5200PC型紫外可见分光光度计(上海元析仪器有限公司);ASAP-2020型表面分析仪(美国Micromeritics Instruments公司)。
1.2 方法
1.2.1 样品制备
将质量为5 g的h-BN(记为样品1)、质量为10 g易分解碳酸氢铵、一定质量的氧化锆珠放入球磨罐中,在转速为320 r/min条件下球磨10 h。将球磨后的样品反复洗涤后,干燥,得到白色粉末。称取一定质量白色粉末,按20 mg/mL的比例添加到去离子水中,使用高速均质机在转速为6 000 r/min条件下剥离4 h,然后静置24 h,得上清液。将部分上清液干燥,得到功能化BNNSs,记为样品2。向另一部分上清液中按0.5 mg/mL的比例加入一定质量的PVA,混合均匀,在温度为180 ℃时喷雾干燥,得到煅烧前功能化氮化硼微球,记为样品3。使用管式炉在温度为500 ℃时将样品煅烧32 h,制备得到具有多孔结构的功能化氮化硼微球,记为样品4。实验制备工艺流程见图1所示。
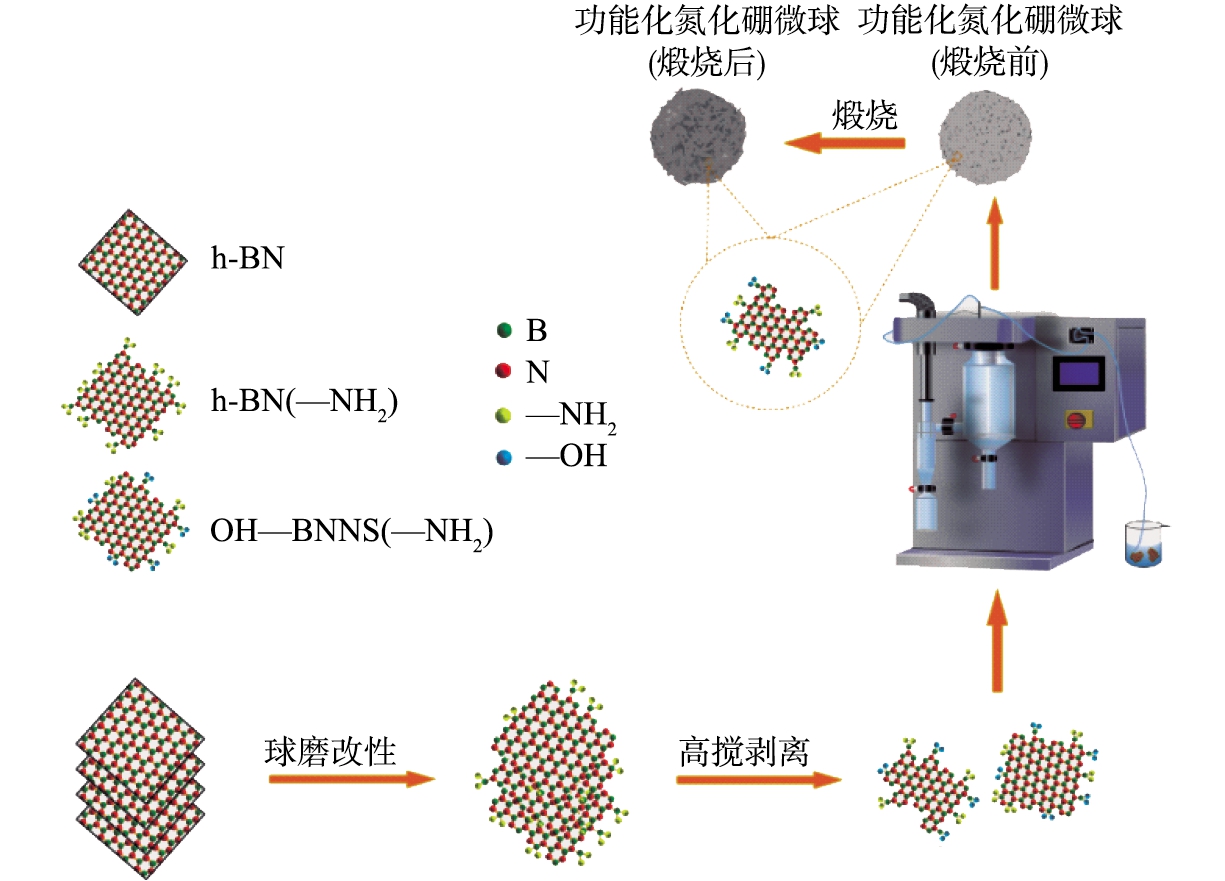
图1 功能化氮化硼微球制备工艺流程示意图
Fig.1 Schematic diagram of preparation process of functionalized boron nitride microspheres
1.2.2 吸附作用
以样品2—4为吸附剂,用于RhB吸附。研究RhB溶液在质量浓度分别为40、60、80、100 mg/L,温度分别为15、25、35、45 ℃,pH分别为3、6、9、12时对功能化氮化硼微球吸附效果的影响,并优化吸附条件。
在烧杯中加入100 mL的RhB溶液和一定量的吸附剂,匀速搅拌。每隔一定时间取样过滤分离,取滤液用紫外-可见分光光度计测吸光度,计算吸附率A和吸附容量q:
(1)
(2)
式中:ρ0为RhB吸附前的初始质量浓度,mg/L;ρt为RhB在某t时刻吸附后的质量浓度,mg/L;m为加入的吸附剂质量,g;m0为RhB吸附前的初始质量,mg;mt为RhB在某t时刻吸附后的质量,mg。
1.2.3 样品的表征
利用SEM和TEM观察对比样品1—4的形貌、大小和分散状态。利用比表面积孔径测定仪测试样品2—3的比表面积,仪器所用测试方法为氮气吸附法。利用FTIR测试样品1、4的官能团结构。
2 结果与讨论
2.1 功能化氮化硼微球的表征
2.1.1 微观结构
图2和图3所示为样品的SEM图像和粒径分布直方图。由图2(a)、(b)可知,相比h-BN,BNNSs呈现的片状结构更小、更薄,说明成功剥离得到BNNSs。对比图2(b)、(c)、(e)可以看出,加入PVA喷雾干燥后的样品由二维片状结构转变为三维球状结构。由图2(d)、(f)和图3可以看出,样品3颗粒更加紧致,表面存在微孔结构;样品4表面存在大孔结构,同时其尺寸存在更宽的分布范围。这是由于在煅烧过程中,高温作用导致PVA分解形成CO2气体,气体从球中逸出,使得孔结构扩大,微球更松散。这种松散的微球多孔结构使氮化硼微球的比表面积更大,由此提供的吸附活性位点更多,更有利于功能化氮化硼微球对RhB的吸附。其中,样品3的粒径分布主要在2~7 μm,平均直径约为5 μm;功能化氮化硼微球的粒径分布主要在3~9 μm,平均直径约为6 μm。

(a)样品1(b)样品2(c)样品3(d)样品3局部(e)样品4(f)样品4局部图2 不同样品的SEM形貌图像Fig.2 SEMimagesofdifferentsamples
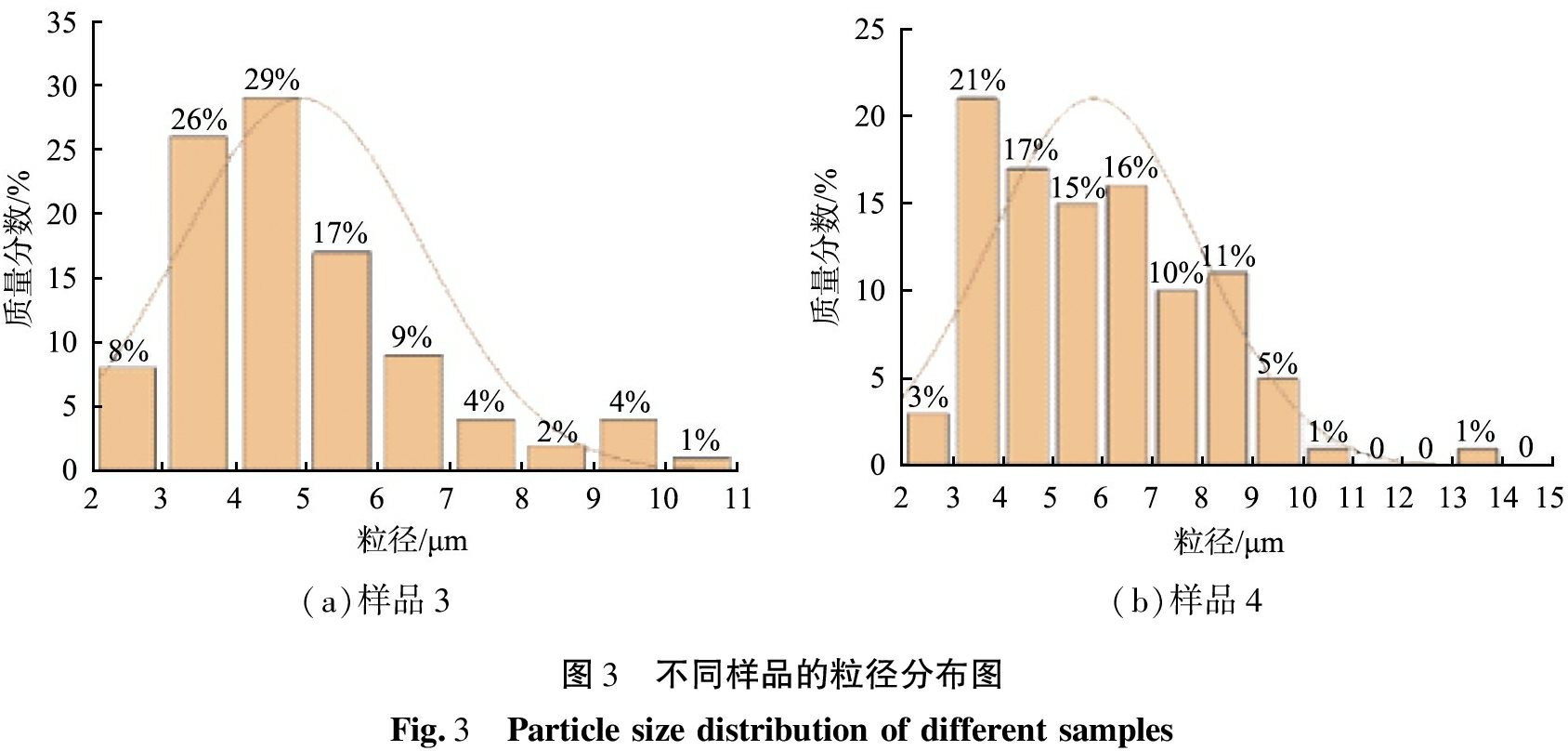
(a)样品3(b)样品4图3 不同样品的粒径分布图Fig.3 Particlesizedistributionofdifferentsamples
2.1.2 比表面积
为了得到样品的比表面积,使用表面分析仪测试样品的氮气吸附-脱附等温线,结果表明,样品2、3和4的比表面积分别为68.87、39.91、72.89 m2/g。对比样品2、3的比表面积,可以发现,样品3的比表面积减少了29 m2/g,其原因是加入PVA后致使BNNSs相互粘结;样品4比表面积比样品2的增大4 m2/g,原因可能是微球的立体球状结构略微减少了BNNSs之间的堆叠;同时,样品4比样品3的比表面积增大33 m2/g,可能是微球因为黏结剂PVA高温分解而导致微孔增大。综上,不同样品比表面积顺序为样品4>样品2>样品3,大的比表面积为能更好地吸附RhB。
2.1.3 FTIR表征的元素结构特点
图4所示为样品1、4的红外光谱图。由图中可以看出,样品1、4在1 400、800 cm-1处有较强的特征峰,对应h-BN典型伸缩振动和弯曲振动。同时,样品4在3 435、3 527 cm-1处多出了 O—H 单键的伸缩振动峰,说明样品剥离时成功接枝了羟基,而在3 298、3 674 cm-1处可以推断为N—H单键的伸缩振动峰,则球磨时易分解铵盐成功为h-BN接枝上氨基。
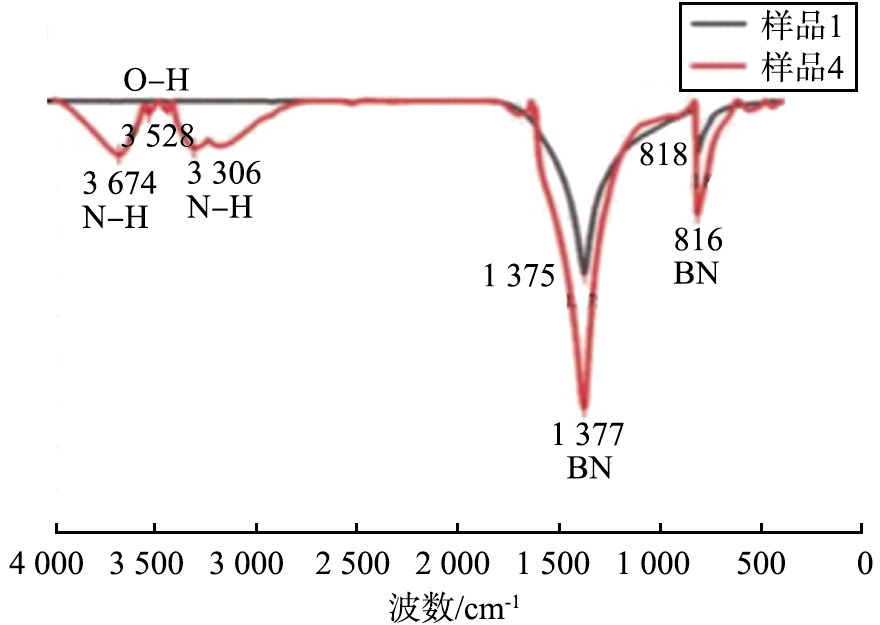
图4 不同样品的红外光谱
Fig.4 FTIR spectra of different samples
2.2 功能化氮化硼微球对罗丹明B吸附性能
2.2.1 吸附性能对比
图5所示为不同样品对RhB溶液的吸附效果对比图。从图中可以看出,相同实验条件下,样品3、4在短时间内均可达到吸附平衡,但样品3的平衡吸附率远低于样品4的,这是因为由BNNSs组合的多孔微球结构的功能化氮化硼微球的粒径分布、平均直径和比表面积上比样品3的均有明显提高,且大孔结构更利于RhB的分子吸附。样品2、4的平衡吸附率都较高,样品4的吸附速率更快,在5 min内的吸附率可达到95%以上,原因是功能化氮化硼微球比表面积稍高于BNNSs的,并且微球中形成了疏松大孔道结构,利于RhB分子在内部快速扩散,提高了吸附效率[10]。综上可知,在相同条件下实验制备的功能化氮化硼微球对RhB的吸附容量和吸附速率均优于未煅烧的样品和BNNSs的。
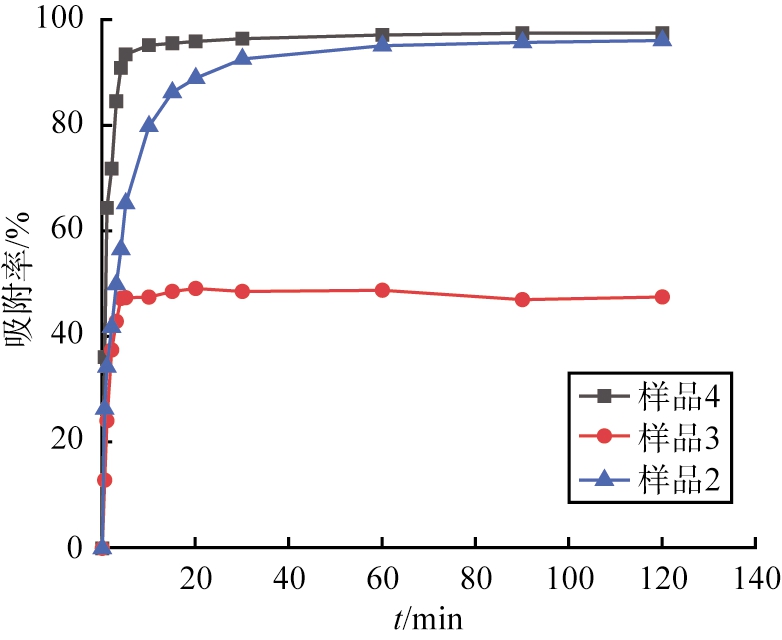
图5 不同样品对RhB溶液的吸附效果对比
FIg.5 Comparison of adsorption effects of different samples
2.2.2 吸附相关影响因素
1)罗丹明B的质量浓度。图6所示为样品4对不同初始质量浓度的RhB溶液的吸附效果。如图可知,样品4对溶液中RhB的吸附速率很快,在5 min内均可达到吸附平衡。当吸附时间相同时,随着RhB溶液质量浓度的增加,样品4对RhB的吸附率逐渐下降,吸附容量上升至70 mg/L时达到最大值。RhB溶液的质量浓度为50、60、70 mg/L时,平衡去除率在80%以上,其中质量浓度为50 mg/L的RhB溶液的平衡去除率在90% 以上。结合图5还可以看出,达到吸附平衡的时间几乎不随RhB溶液的浓度的改变而变化。
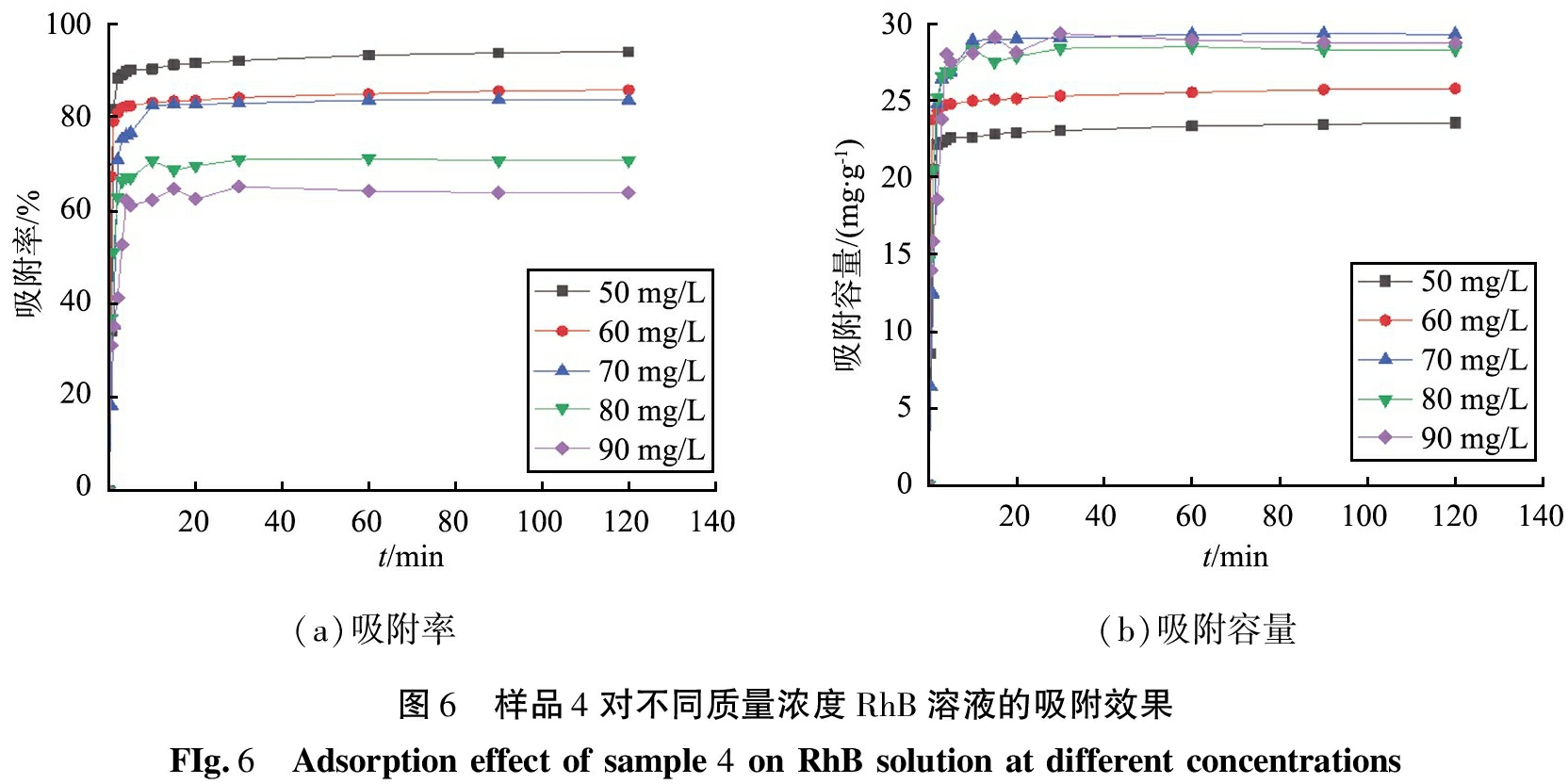
(a)吸附率(b)吸附容量图6 样品4对不同质量浓度RhB溶液的吸附效果FIg.6 Adsorptioneffectofsample4onRhBsolutionatdifferentconcentrations
2)温度和pH影响。图7所示为温度和pH对功能化氮化硼微球吸附RhB的影响。由图7(a)可以看出,温度从15 ℃升高到45 ℃时,平衡吸附容量变化不大,均在24 mg/g左右。同时,由图7(b)可以看出,随着pH从3变化至12,功能化氮化硼微球吸附RhB的平衡吸附容量也基本不变,均维持在25 mg/g左右。综上结果可得,功能化氮化硼微球吸附RhB在实验范围内不受温度和pH的影响,因此在实际使用功能化氮化硼微球作为吸附剂时,不需要特别关注溶液的温度和pH。
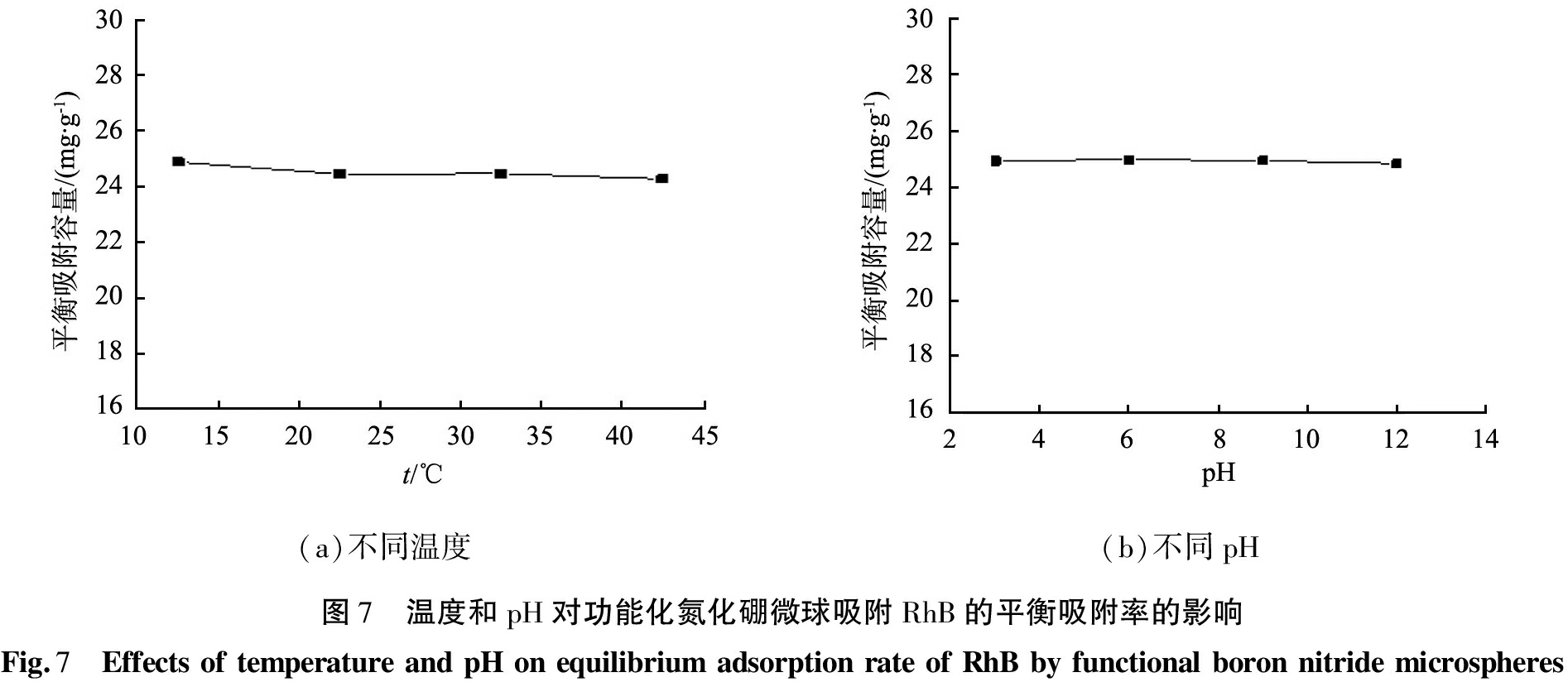
(a)不同温度(b)不同pH图7 温度和pH对功能化氮化硼微球吸附RhB的平衡吸附率的影响Fig.7 EffectsoftemperatureandpHonequilibriumadsorptionrateofRhBbyfunctionalboronnitridemicrospheres
2.2.3 吸附热力学和吸附动力学
1)吸附热力学。吸附等温线用于描述吸附剂的吸附能力以及与被吸附物之间相互作用机理,本文中采用Langmuir吸附模型、Freundlich吸附模型、Dubinin Radushkevich(D-R)吸附模型对吸附平衡数据进行了分析,拟合方程[16]如下。
Langmuir吸附模型:
ρe/qe=1/bqm+ρe/qm,
(3)
Freundlich吸附模型:
lg qe=lg kf+(1/n)lg ρe,
(4)
D-R吸附模型:
ln qe=ln qm-βε2,
(5)
式中:ρe为吸附平衡时RhB的质量浓度,mg/L;qe为达到平衡时的吸附容量,mg/g;b是Langmuir常数,L/mg;qm为单层吸附时的最大吸附量,mg/g;kf 和1/n为Freundlich常数;β为D-R等温线常数,mol/kJ2;ε为Polanyi势能,ε= RTln(1+1/e),J/mol。
图8所示为平衡吸附容量随平衡浓度变化曲线和模型拟合曲线,模型数据见表1。由图8和表1可知,Langmuir模型拟合的R2高于Freundlich、D-R模型的,说明功能化氮化硼微球吸附 RhB 符合 Langmuir 等温吸附模型,即功能化氮化硼微球对RhB的吸附机理为单分子层吸附[17]。
表1 Langmuir、Freundlich、D-R模型参数
Tab.1 Data parameters of Langmuir, Freundlich and D-R models

Langmuirqm/(mg·g-1)b/(L·mg-1)Freundlichkf/(mg·g-1)1/nD-Rqm/(mg·g-1)β/(mol·kJ-2)E/(kJ·mol-1)29.331.4521.970.0844.281.5324×10-071811.7R2=0.99876R2=0.74906R2=0.78678
吸附过程的可行性可用分离系数RL计算公式为
(6)
RL的大小将吸附等温线的类别分为不利的(RL>1)、线性的(RL=1)、不可逆的(RL=0)、有利的(0<RL<1)[27],对不同初始浓度的RhB溶液计算得到的RL的值均在0~1之间,则说明功能化氮化硼微球容易吸附RhB。
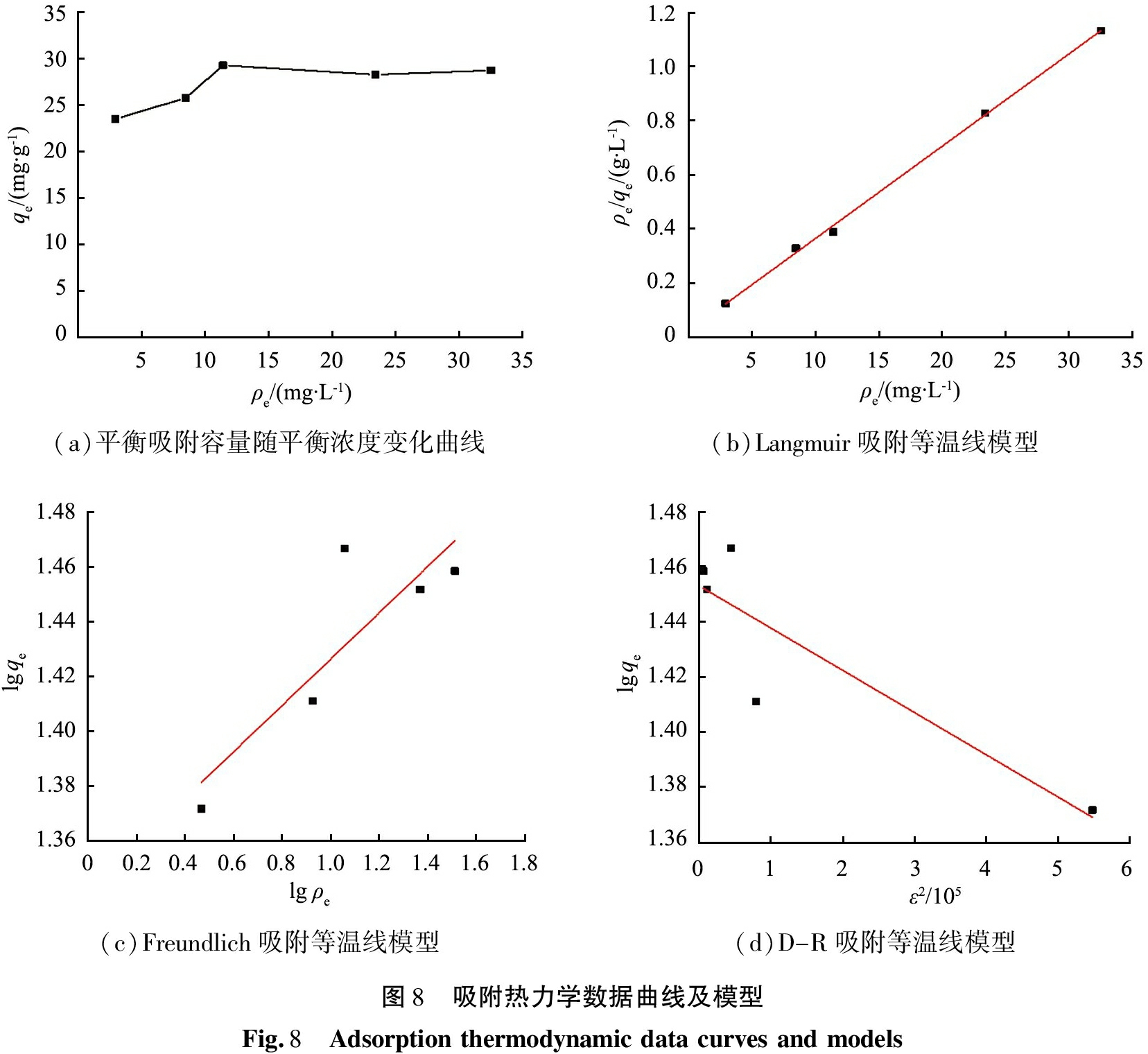
(a)平衡吸附容量随平衡浓度变化曲线(b)Langmuir吸附等温线模型(c)Freundlich吸附等温线模型(d)D-R吸附等温线模型图8 吸附热力学数据曲线及模型Fig.8 Adsorptionthermodynamicdatacurvesandmodels
2)吸附动力学。采用拟一级动力学模型、拟二级动力学模型、颗粒内扩散模型分别分析了功能化氮化硼微球吸附 RhB 的吸附速率以及吸附过程的机理。拟合方程[16,18]如下。
拟一级动力学模型:
lg(qe-qt)=lg qe-k1×t/2.303,
(7)
拟二级动力学模型:
(8)
颗粒内扩散模型:
qt=kit0.5+C,
(9)
式中:qt为吸附时间t后功能化氮化硼微球对RhB的吸附量,mg/g;k1为拟一级动力学模型速率常数,min-1;k2为拟二级动力学模型速率常数,g·min/mg;ki为颗粒内扩散模型的速率常数,mg·min0.5/g;C为纵坐标截距。
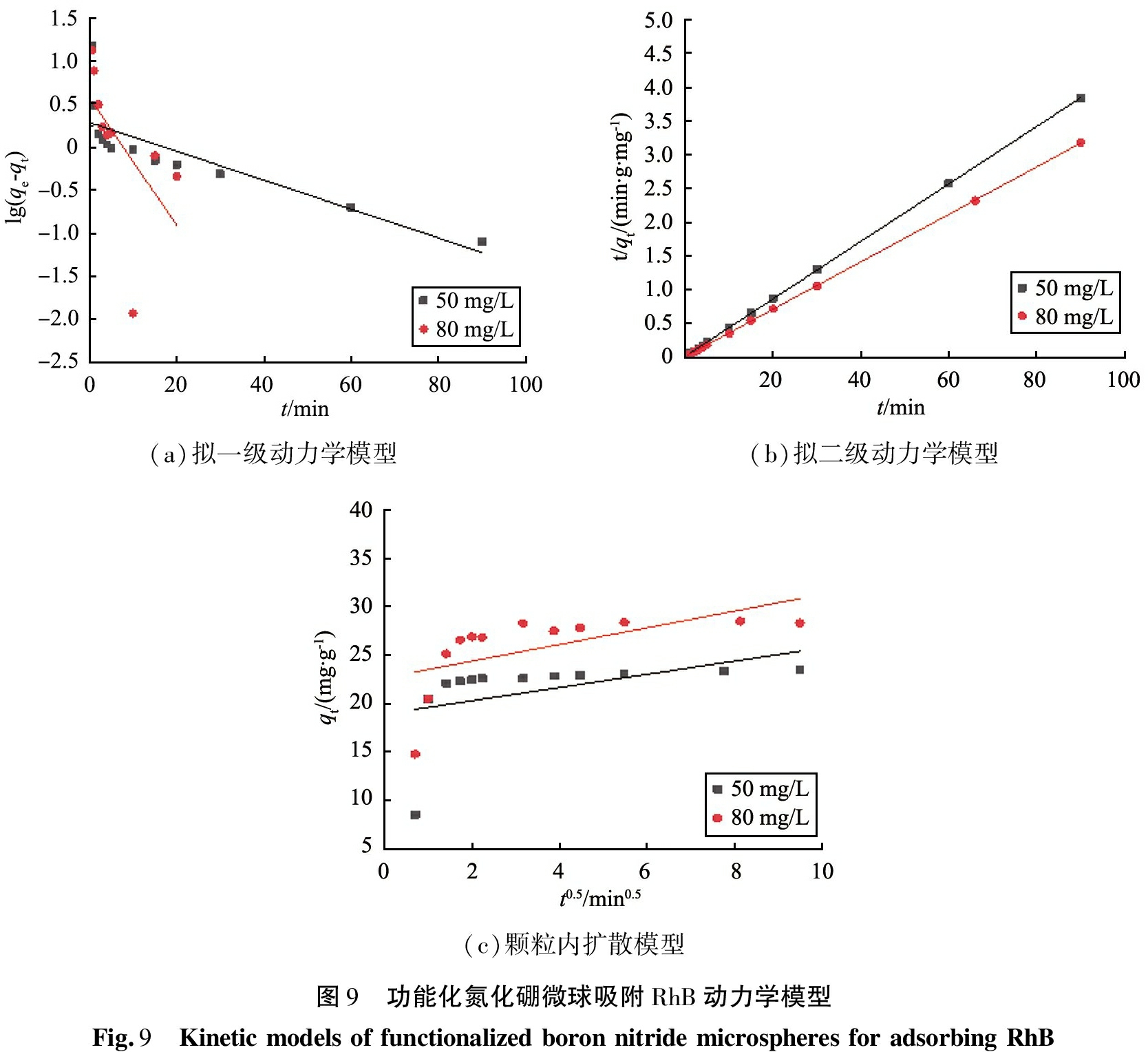
(a)拟一级动力学模型(b)拟二级动力学模型(c)颗粒内扩散模型图9 功能化氮化硼微球吸附RhB动力学模型Fig.9 KineticmodelsoffunctionalizedboronnitridemicrospheresforadsorbingRhB
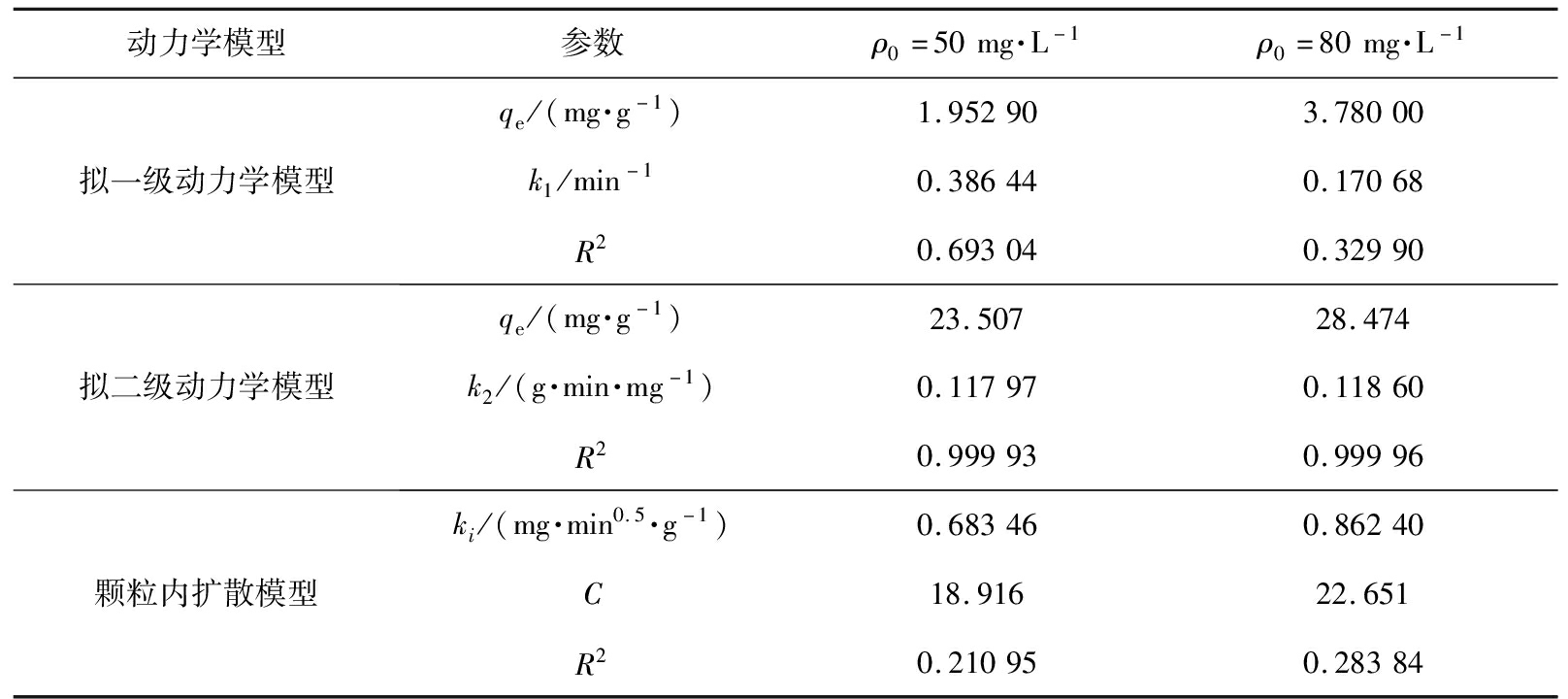
图9所示为分别对初始质量浓度为50、80 mg/L的RhB溶液,利用3种模型拟合的吸附动力学曲线,模型参数数据见表2。其中,二者初始质量浓度下的吸附均是拟二级动力学模型的R2值最高,因此功能化氮化硼微球吸附RhB的过程可以用拟二级动力学模型来解释,即速率限制步骤是化学吸附过程。
表2 功能化氮化硼微球吸附RhB的动力学模型参数
Tab.2 Kinetic model parameters of functionalized boron nitride microspheres for adsorbing RhB
动力学模型参数ρ0=50mg·L-1ρ0=80mg·L-1拟一级动力学模型qe/(mg·g-1)1.952903.78000k1/min-10.386440.17068R20.693040.32990拟二级动力学模型qe/(mg·g-1)23.50728.474k2/(g·min·mg-1)0.117970.11860R20.999930.99996颗粒内扩散模型ki/(mg·min0.5·g-1)0.683460.86240C18.91622.651R20.210950.28384
综上,功能化氮化硼微球吸附RhB为单分子层化学吸附,且结合该过程基本不受pH的影响。本文中合成的功能化氮化硼微球组成结构BNNSs具有由B和N交替环合的六元环结构,该结构中的B原子可以接受π电子。吸附质RhB结构中含3个芳香苯环,富含π电子,因此,认为功能化氮化硼微球吸附RhB主要受到π-π相互作用[19],机理如图10所示。同时,功能化氮化硼微球中接枝的亲水性官能团对于吸附RhB也可能产生积极的影响。
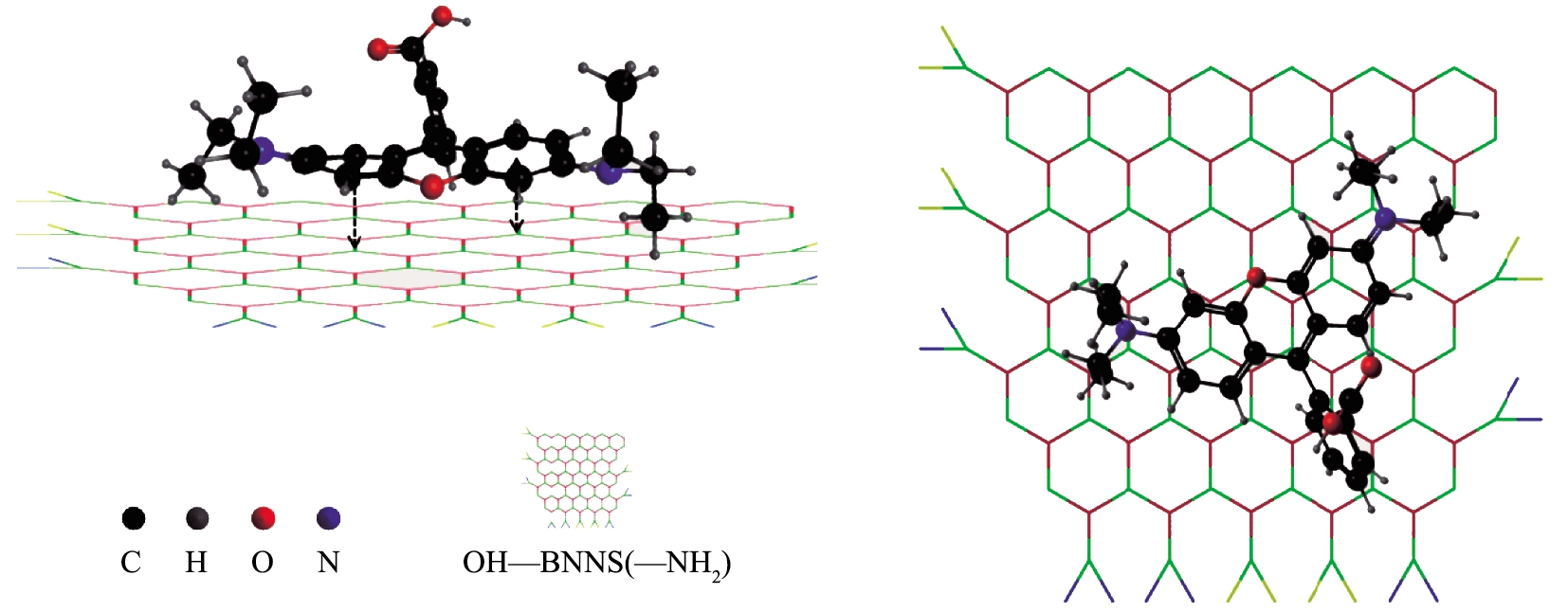
图10 功能化氮化硼微球吸附RhB机理模型示意图
Fig.10 Schematic diagram of mechanism model of functionalized boron nitride microspheres for adsorbing RhB
3 结论
1)以h-BN为原料,通过球磨改性、高速剥离和喷雾干燥成功制备得到了多孔结构的功能化氮化硼微球,其平均直径约为6 μm,分散性良好,成功接枝上氨基和羟基,并有明显的大孔道。
2)以RhB为吸附质,当溶液质量浓度为20 mg/L时,功能化氮化硼微球比BNNSs和煅烧前的样品的吸附性能更好,具体体现为吸附容量大且吸附速率快。
3)当加入的吸附剂量一定时,RhB溶液质量浓度越低,功能化氮化硼微球对RhB的吸附率越高。当RhB溶液质量浓度为50 mg/L时,吸附率可达到94%。同时,该吸附过程不受温度和pH的影响,这对处理RhB染料废水十分有利。
4)功能化氮化硼微球吸附RhB符合Langmuir等温吸附模型和拟二级动力学模型,即该过程为单分子层化学吸附。
[1]MENG J, REN M F, WANG S Y, et al.A smart adsorbent with ability of environmentally friendly regeneration for p-nitrophenol removal in aqueous solution[J].Journal of Inorganic and Organometallic Polymers and Materials, 2021, 31: 2381-2392.
[2]ZHANG J, ZHU M M, JONES I, et al.Performance of activated carbons prepared from spent tyres in the adsorption of rhodamine B in aqueous solutions[J].Environmental Science and Pollution Research International, 2021, 28: 52862-52872.
[3]LIOU T H, TSENG Y K, LIU S M, et al.Green synthesis of mesoporous graphene oxide/silica nanocomposites from rich husk ash: characterization and adsorption performance[J].Environmental Technology & Innovation, 2021, 22: 101424.
[4]LIANG X, NI Z J, ZHAO L, et al.Improving surface areas of covalent organic framework with surfactant assisted solvothermal method and its adsorption properties for rhodamine B[J].Materials Chemistry and Physics, 2021, 270: 124725.
[5]ZHANG Y N, HAN H J, WANG X H, et al.Utilization of NaP zeolite synthesized with different silicon species and NaAlO2 from coal fly ash for the adsorption of rhodamine B[J].Journal of Hazardous Materials, 2021, 415: 125627.
[6]NAZIR M A, BASHIR M S, JAMSHAID M, et al.Synthesis of porous secondary metal-doped MOFs for removal of rhodamine B from water: role of secondary metal on efficiency and kinetics[J].Surfaces and Interfaces, 2021, 25: 101261.
[7]LI Y F, YAN X L, HU X Y, et al.Trace pyrolyzed ZIF-67 loaded active-ted carbon pellets for enhanced adsorption and catalytic degradation of rhodamine B in water[J].Chemical Engineering Journal, 2019, 375: 122003.
[8]ROY S, ZHANG X, ANAND B, et al.Structure, properties and applications of two-dimensional hexagonal boron nitride[J].Advanced Materials, 2021, 33(44): 2101589.
[9]XIONG J, DI J, ZHU W S, et al.Hexagonal boron nitride adsorbent: synthesis, performance tailoring and applications[J].Journal of Energy Chemistry, 2020, 40(1): 99-111.
[10]LIN Y, WILLIAMS T V, CAO W, et al.Defect functionalization of hexagonal boron nitride nanosheets[J].The Journal of Physical Chemistry C, 2010, 114: 17434-17439.
[11]LEI W, MOCHALIN V N, LIU D, et al.Boron nitride colloidal solution, ultralight aerogels and freestanding membranes through one-step exfoliation and functionalization[J].Nature Communications, 2015, 6: 9849.
[12]LI G Y, ZHU M Y, GONG W B, et al.Boron nitride aerogels with super-flexibility ranging from liquid nitrogen temperature to 1000 ℃[J].Advanced Functional Materials, 2019, 29(20): 1900188.
[13]XUE Y M, DAI P C, ZHOU M, et al.Multifunctional superelastic foam-like boron nitride nanotubular cellular-network architectures[J].ACS Nano, 2017, 11(1): 558-568.
[14]WANG J M, LIU D, LI Q X, et al.Lightweight, superelastic yet thermoconductive boron nitride nanocomposite aerogel for thermal energy regulation[J].ACS Nano, 2019, 13(7): 7860-7870.
[15]CAO B X, SHEN F, DAI H.Studies on spray drying[J].Journal of Tsinghua University(Natural Science), 1948(S2): 115-126.
[16]MA J, YU F, ZHOU L, et al.Enhanced adsorptive removal of methyl orange and methylene blue from aqueous solutionby alkali-activated multiwalled carbon nanotubes[J].ACS Applied Materials & Interfaces, 2012, 4(11): 5749-5760.
[17]GHORAI S, SARKAR A, RAOUFI M, et al.Enhanced removal of methylene blue and methyl violet dyes from aqueous solution using a nanocomposite of hydrolyzed polyacrylamide grafted xanthan gum and incorporated nanosilica[J].ACS Applied Materials & Interfaces, 2014, 6(7): 4766-4777.
[18]ZHOU J B, TANG C, CHENG B, et al.Rattle-type carbon-alumina core-shell spheres: synthesis and application for adsorption of organic dyes[J].ACS Applied Materials & Interfaces, 2012, 4(4): 2174-2179.
[19]CHEN X F, JIA S L, DING N, et al.Capture of aromatic organic pollutants by hexagonal boron nitride nanosheets: density functional theoretical and molecular dynamic investigation[J].Environmental Science: Nano, 2016, 3: 1493-1503.