近年来随着工业的迅速发展,环境问题日益严峻,造成环境污染的因素也日益增多。其中,各种工业废气和废水的产生和排放造成的空气污染和水污染已成为亟待解决的问题。硝基酚类化合物通常从合成染料、石化、增塑剂、农药和制药等行业释放到环境中,具有高毒性、致癌性和生物蓄积性等危险特性的污染物[1-2]。
目前已报道的去除环境中对硝基酚污染物的方法有催化法、吸附法、氧化法、萃取法、微生物降解法、生物固定法等[3]。其中,催化法因操作简单、处理效率高、可资源化污染物等优点,成为处理对硝基酚的常用方法。贵金属作为一种常用的催化剂近年来已被广泛报道,它们具有优异的物理和化学性质以及潜在的应用,例如环境污染物降解、化学生产、能量储存等[4]。小尺寸在赋予贵金属纳米颗粒独特优势的同时也带来了一些缺点,例如较低的可回收性和较高的团聚倾向。另外,贵金属价格昂贵而且数量稀少,这也妨碍了其进一步的实际应用。贵金属纳米颗粒可以与多孔材料有效结合,以改善凝聚并同时减小纳米颗粒尺寸[5-7]。作为多孔材料中最有趣的材料之一,金属有机骨架(MOFs)具有高比表面积、可调节的尺寸选择性以及在不同条件下的出色的热稳定性和化学稳定性[8-11]。在过去的研究中,MOFs已被广泛地用于气体的分离和储存,或作为多孔碳材料合成的前体。
在最近的研究中,构建多金属MOFs已成为一个热门的研究方向。构造多金属MOFs最常用的合成策略之一是通过金属交换或浸渍等将另一种金属离子引入单金属MOFs中[12-13]。基于一些MOF具有相似的晶体结构,另一种合成策略是使用单金属MOFs作为种子并在其表面继续生长另一种有相似晶体结构的MOFs[14-15]。
在大多数情况下多金属MOFs能够有效结合2种单金属MOFs的各自优点,表现出显著增强的物理和化学性质[16-20]。沸石咪唑酯骨架-8(ZIF-8)是具有代表性的一种MOFs材料,本文中在制备多金属ZIF-8(Zn-Co)载体基础上,进一步对Ag纳米颗粒进行包封,得到了Ag-ZIF-8(Zn-Co)多金属复合材料。与单金属ZIF-8和ZIF-67催化降解硝基酚类化合物相比,得到的多金属复合材料对于多种硝基酚类化合物都表现出显著增强的催化性能。
1 实验
1.1 试剂与仪器
二水合乙酸锌(纯度为99.0%,质量分数,下同)、四水合乙酸钴(纯度为99.0%)、2-甲基咪唑(纯度为98.0%)、邻硝基苯酚(纯度为98.0%)、对硝基苯胺(纯度为99.0%)(上海阿拉丁工业有限公司);硝酸银(纯度为99.8%,国药集团化学试剂有限公司);硼氢化钠(纯度为97.0%,上海凌峰化学试剂有限公司);无水乙醇、对硝基苯酚(纯度为99.0%)(上海麦克林化学品有限公司);甲醇(纯度为99.5%)和无水正己烷(纯度为97.0%)(成都科隆化学品有限公司)。
Nicolet iS10红外光谱仪(FTIR,美国Thermo Scientific公司);AXS D8 Advance X射线衍射仪(德国Bruker公司);FEI Quanta 250F扫描电子显微镜(SEM,美国FEI公司);Specord 50Plus紫外分光光度计(德国耶拿公司);Tecnai-G20高分辨透射电子显微镜(美国FEI公司)。
1.2 方法
1.2.1 ZIF-8的制备
在40 mL去离子水中溶解1.4 g的二水合乙酸锌,此为A溶液。再在120 mL水中溶解4.2 g的2-甲基咪唑,此为B溶液。充分溶解后将A溶液逐滴滴入B溶液中,边滴边搅拌,滴完之后再搅拌30 min。静置24 h,离心。离心完成后倒掉上清液,用去离子水洗涤,再次离心,重复3~4次。之后放入真空干燥箱,60 ℃下真空干燥12 h。
1.2.2 ZIF-67的制备
在40 ml去离子水中溶解1.59 g的四水合乙酸钴,此为A溶液。再在120 mL水中溶解4.2 g的2-甲基咪唑,此为B溶液。混合、离心、干燥操作同上。
1.2.3 ZIF-8(Zn-Co)制备
在40 mL去离子水中溶解795.5 mg的四水合乙酸钴和701.1 mg的二水合乙酸锌,此为A溶液。再在120 mL水中溶解4.2 g的2-甲基咪唑,此为B溶液。混合、离心、干燥操作同上。
1.2.4 Ag-ZIF制备
取500 mg制备的ZIF材料,超声20 min,使其均匀分散到40 mL无水正己烷中。再用0.11 mL的去离子水溶解15.7 mg的硝酸银,溶解之后逐滴加入上述正己烷溶液中。滴加完成后持续搅拌3h,倒掉上清液,并放入真空干燥箱在60 ℃下干燥6 h。取0.1 g的硼氢化钠溶于5 mL甲醇溶液中,配置成0.6 mol/L的硼氢化钠甲醇溶液,将其逐滴加入干燥后的上述材料中,并搅拌30 min。离心、干燥操作同上。
1.2.5 硝基苯酚催化还原
取对硝基苯酚(1.75 mmol/L)4 mL,邻硝基苯酚(3.5 mmol/L)12 mL,对硝基苯胺(8 mmol/L)12 mL于烧杯中,稀释至60 mL,再加入32 mL水,待用。在16.5 mL水中溶解0.8 g硼氢化钠,溶解完全后,取13.2 mL硼氢化钠溶液加入稀释过的对硝基苯酚溶液中,并开始搅拌,此时取1 mL溶液稀释10倍,测量在400、415、380 nm波长处的吸光度,作为对照。取0.034 6 g的催化剂(ZIF-8、ZIF-67、Ag-ZIF-8(Zn-Co))分散到1 mL乙醇中,充分溶解。取0.1 ml分散液加入正在搅拌的模拟废水中,开始计时,定时取1 mL的待测液,稀释10倍后,分别在400、415、380 nm波长处用紫外分光光度计测量吸光度。
2 结果和讨论
2.1 微观形貌表征
通过扫描电镜对制备的样品进行了表征,ZIF-8、ZIF-67和ZIF-8(Zn-Co)颗粒扫描电镜图像如图1所示。由图可以看出,3种样品大多都为规则的菱形多面体,具有光滑的表面。由图1(a)、1(b)可知,2种单金属ZIF的粒径约为2 μm,形貌没有明显的差异。图1(c)显示,制备的Zn和Co双金属ZIF的尺寸有明显的减小,粒径大约为200 nm。

(a)ZIF-8(b)ZIF-67(c)ZIF-8(Zn-Co)图1 ZIF-8、ZIF-67、ZIF-8(Zn-Co)的颗粒扫描电镜图像Fig.1 SEMimagesofZIF-8,ZIF-67andZIF-8(Zn-Co)particles
图2为制备的Ag-ZIF-8(Zn-Co)复合催化剂在使用前后的SEM图像。由图2(a)可知,在使用双溶剂法将银纳米颗粒包封在ZIF的孔道中后,材料的外观并没有发生明显的变化,在表面也没有看到大面积的团聚。为了探究Ag-ZIF对硝基苯酚的催化机理,对反应后的材料样品也同样进行了SEM测试。Ag-ZIF-8(Zn-Co)材料催化还原硝基苯酚后的SEM图像如图2(b)所示。从图2(b)可以看出,催化后的Ag-ZIF-8(Zn-Co)仍然是均匀的菱形十二面体,直径为500~800 nm。对比图2(a)和图2(b)可以发现,Ag-ZIF-8(Zn-Co)使用前后的微观形貌并没有太大变化,证明所制备的复合材料具有较好的稳定性,在反应过程中结构不会受到明显的破坏。

(a)Ag-ZIF-8(Zn-Co)反应前(b)Ag-ZIF-8(Zn-Co)反应后图2 Ag-ZIF-8(Zn-Co)材料反应前后的SEM图像Fig.2 SEMimagesofAg-ZIF-8(Zn-Co)materialsbeforeandafterreaction
图3为Ag-ZIF-8(Zn-Co)的TEM图像和包封在材料内部的Ag纳米颗粒的高分辨TEM图像。从图3(a)中可以清晰的看到,分布在晶体内部的Ag纳米颗粒,这些纳米颗粒分布均匀且几乎没有发生大面积的团聚,这为催化过程提供了大量的活性位点。其次,可见晶体表面几乎没有Ag纳米粒子的存在,证明双溶剂法成功的将金属前体置入了ZIF材料的孔道中。这些Ag纳米颗粒的直径平均在5 nm左右,通过高分辨TEM图像图3(b)可以观察到晶格条纹间距为0.234 nm,对应了0价银的111晶面。

(a)Ag-ZIF-8(Zn-Co)(b)Ag纳米颗粒图3 Ag-ZIF-8(Zn-Co)及其内包封的银纳米颗粒TEM图像Fig.3 TEMimagesofAg-ZIF-8(Zn-Co)andAgnanoparticlesencapsulatedinit
2.2 XRD表征
XRD光谱被用来验证合成样品的晶体结构。图4为制备2种单金属ZIF-8材料以及Co和Zn双金属ZIF-8在使用双溶剂法包封Ag纳米颗粒前后的XRD谱图。如图4(a)所示,由于ZIF-8和ZIF-67具有相同的拓扑结构和近似的晶胞参数,因此所有合成的ZIF-8和ZIF-67应该具有几乎相同的XRD特征峰,测试结果也显示了类似的结果[21]。混合金属ZIFs的特征峰与ZIF-8和ZIF-67几乎相同,尖锐而高的峰表明了所制备的材料具有较高的结晶度,与其他文献中所制备的单金属ZIF是相同的[22]。
在ZIF材料包封了Ag纳米颗粒之后,其属于ZIF材料的特征峰并没有消失或者降低,这表明所制备的材料具有良好的稳定性。制备过程中高浓度的硼氢化钠并没有破坏材料的结构,保证了在后续催化性能测试中材料不会受硼氢化钠的影响。应该注意的是,由于Ag纳米颗粒的含量较低,仅为2%,且制备的Ag纳米颗粒尺寸较小,因此从图4(b)中找不到明显的属于Ag纳米颗粒的峰,该结果与以前的文献结果相似[23];但是,通过TEM测试可以证明Ag纳米颗粒在ZIF材料内部成功的包封,并且其粒径尺寸仅为5 nm左右,这与XRD得到的结果一致。
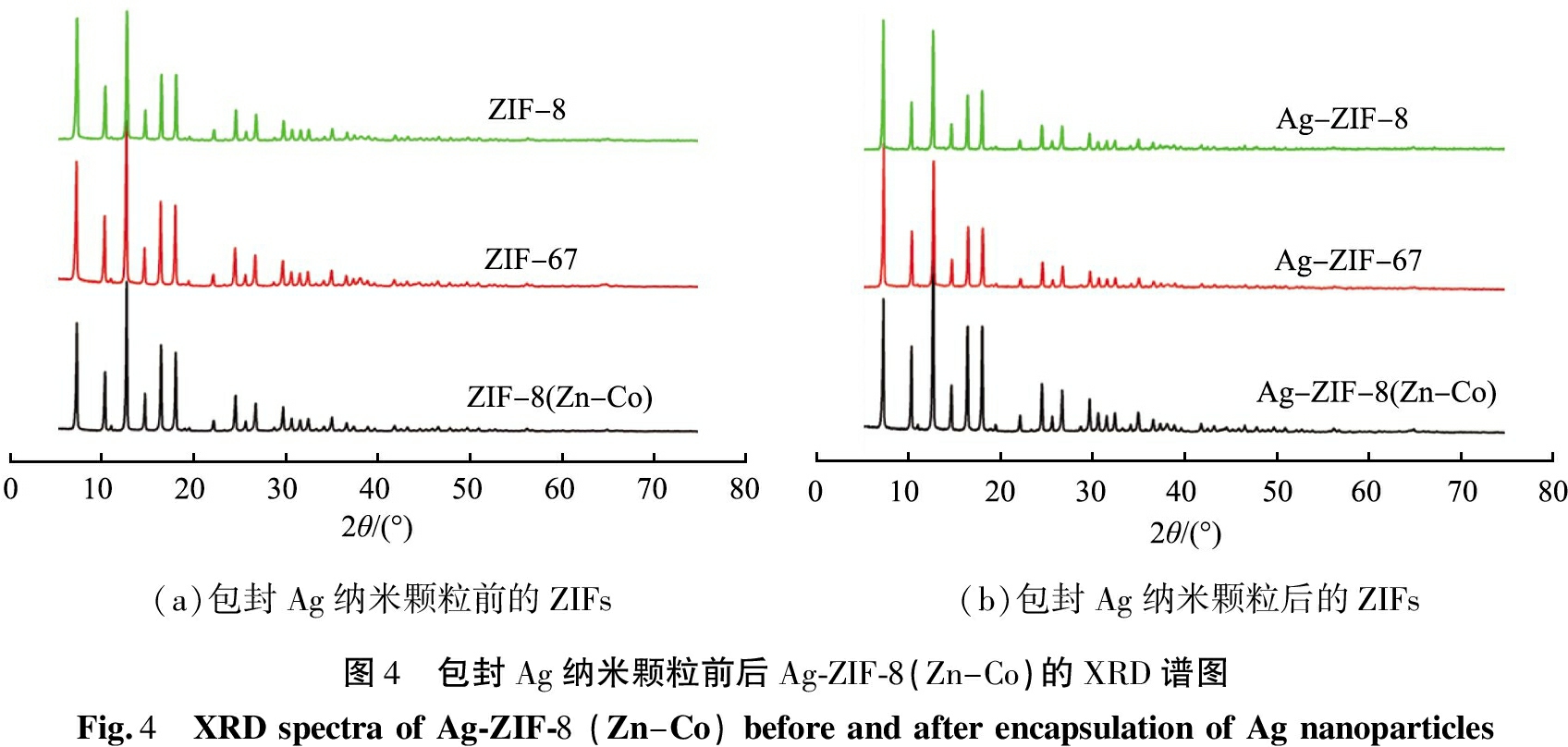
(a)包封Ag纳米颗粒前的ZIFs(b)包封Ag纳米颗粒后的ZIFs图4 包封Ag纳米颗粒前后Ag-ZIF-8(Zn-Co)的XRD谱图Fig.4 XRDspectraofAg-ZIF-8(Zn-Co)beforeandafterencapsulationofAgnanoparticles
2.3 催化性能
为了评价Ag-ZIF的催化活性,将对硝基苯酚、邻硝基苯酚和对硝基苯胺的催化还原反应作为应模型。在这些反应期间,用过量的NaBH4水溶液用作还原剂,以保证在反应过程中其浓度保持不变,并利用紫外-可见光谱法监测反应过程。其中,在检测对硝基苯酚时,由于在加入NaBH4后形成了对硝基苯酚离子,所以溶液中的对硝基苯酚的吸收峰移至400 nm处,颜色也变为黄绿色。在加入催化剂之后还原反应开始,并且每隔一段时间,通过紫外吸收光谱同时检测在300和400 nm处的吸收峰变化。图5为Ag-ZIF-8(Zn-Co)降解对硝基苯酚随时间变化的紫外吸收光谱图。如图所示,400 nm处的特征峰属于对硝基苯酚,而300 nm处为对氨基苯酚。在7 min内,400 nm处的峰迅速减小,而300 nm处的峰增加,说明对硝基苯酚在Ag-ZIF和NaBH4的存在下迅速还原。
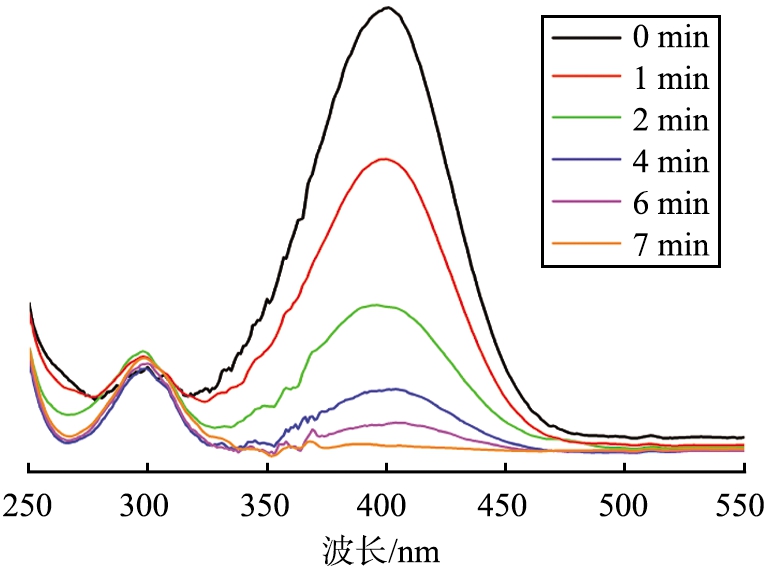
图5 Ag-ZIF-8(Zn-Co)降解对硝基苯酚随时间的紫外吸收光谱
Fig.5 Time-dependent UV absorption spectra of 4-nitrophenol solution
图6为对硝基苯酚在制备的3种复合催化剂上的反应动力学图。如图6(a)所示,Ag-ZIF-8的催化活性最弱,需要30min以上才能够还原所有的污染物,而Ag-ZIF-8(Zn-Co)仅在8 min内即可完成反应。图6(b)中ln(ct/c0)和时间显示出良好的线性相关性,其中c0和ct分别表示在初始时间的污染物浓度和不同时间的污染物浓度。表观速率常数(Kapp)是ln(ct/c0)与时间关系图的斜率绝对值,通过计算表观速率常数我们可以更加直观的比较不同材料的催化活性。经过计算,Ag-ZIF-8的表观速率常数为0.15×10-4 s-1,Ag-ZIF-67的表观速率常数为0.31×10-4 s-1。与Ag-ZIF-8和Ag-ZIF-67相比,制备的多金属Ag-ZIF-8(Zn-Co)表现出显著增强的催化能力,其Kapp为1.08×10-4 s-1。此时,在400 nm处的吸收峰在7 min内消失,而300 nm处的峰逐渐增强。相反,Ag-ZIF-8用了40 min使400 nm处的峰消失,而Ag-ZIF-67用了20 min。显然,通过构建多金属ZIF作为载体来包封Ag纳米颗粒可以显著提升复合材料的催化性能。
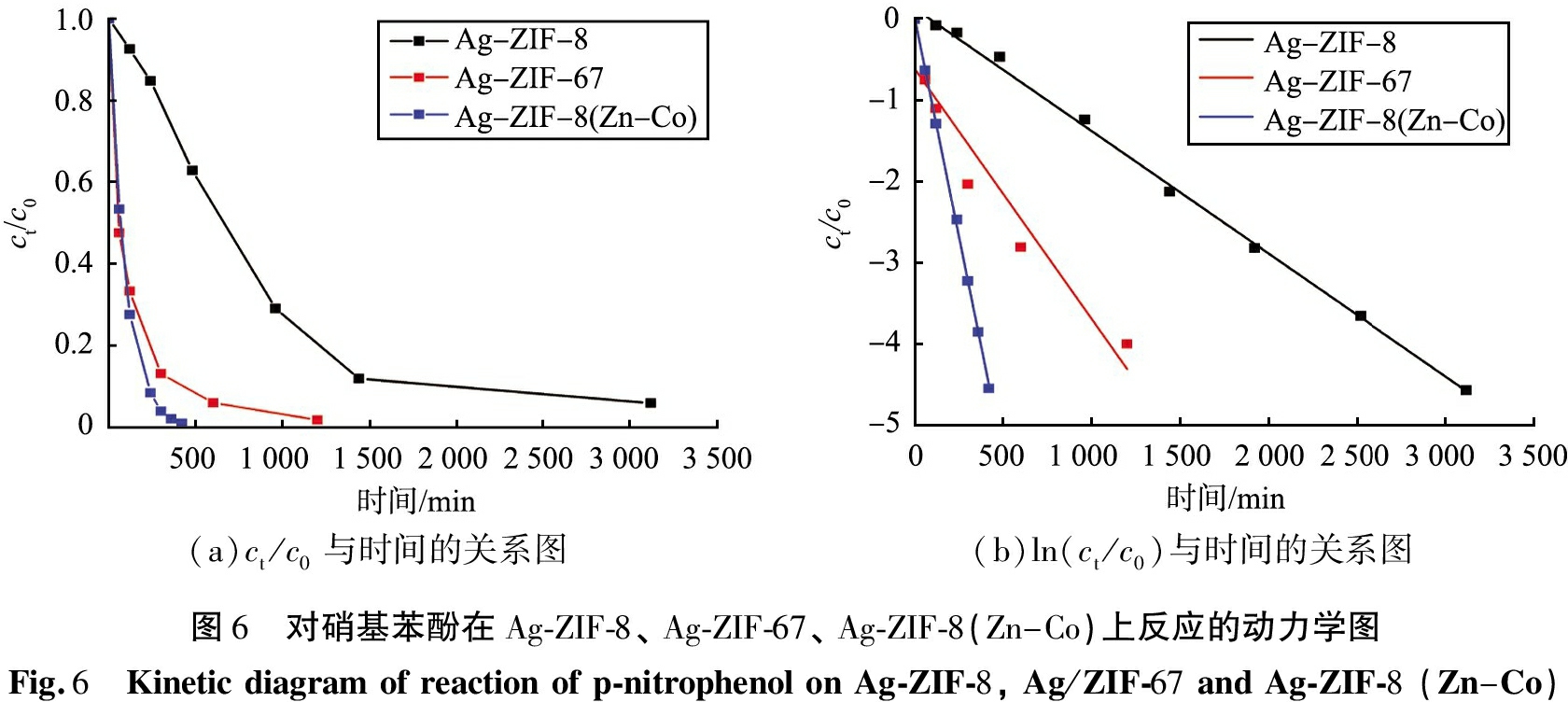
(a)ct/c0与时间的关系图(b)ln(ct/c0)与时间的关系图图6 对硝基苯酚在Ag-ZIF-8、Ag-ZIF-67、Ag-ZIF-8(Zn-Co)上反应的动力学图Fig.6 Kineticdiagramofreactionofp-nitrophenolonAg-ZIF-8,Ag/ZIF-67andAg-ZIF-8(Zn-Co)
Ag-ZIF-8(Zn-Co)不仅对对硝基苯酚的催化还原具有良好的活性,对其他2种典型的硝基酚类化合物也具有相似的作用。在测试复合材料对邻硝基苯酚和对硝基苯胺还原反应的催化活性时![]() 在所有反应中均是过量的。图7和图8分别是制备的复合材料去除邻硝基苯酚和对硝基苯胺的反应动力学图。反应过程中的ln(ct/c0)同样与时间之间的线性关系良好,这证明2个硝基酚类化合物的催化反应符合伪一级动力学,并显示出与催化还原对硝基苯酚时相同的趋势。实验表明,对于3种硝基酚类化合物,多金属Ag-ZIF-8(Zn-Co)的催化活性最强。
在所有反应中均是过量的。图7和图8分别是制备的复合材料去除邻硝基苯酚和对硝基苯胺的反应动力学图。反应过程中的ln(ct/c0)同样与时间之间的线性关系良好,这证明2个硝基酚类化合物的催化反应符合伪一级动力学,并显示出与催化还原对硝基苯酚时相同的趋势。实验表明,对于3种硝基酚类化合物,多金属Ag-ZIF-8(Zn-Co)的催化活性最强。
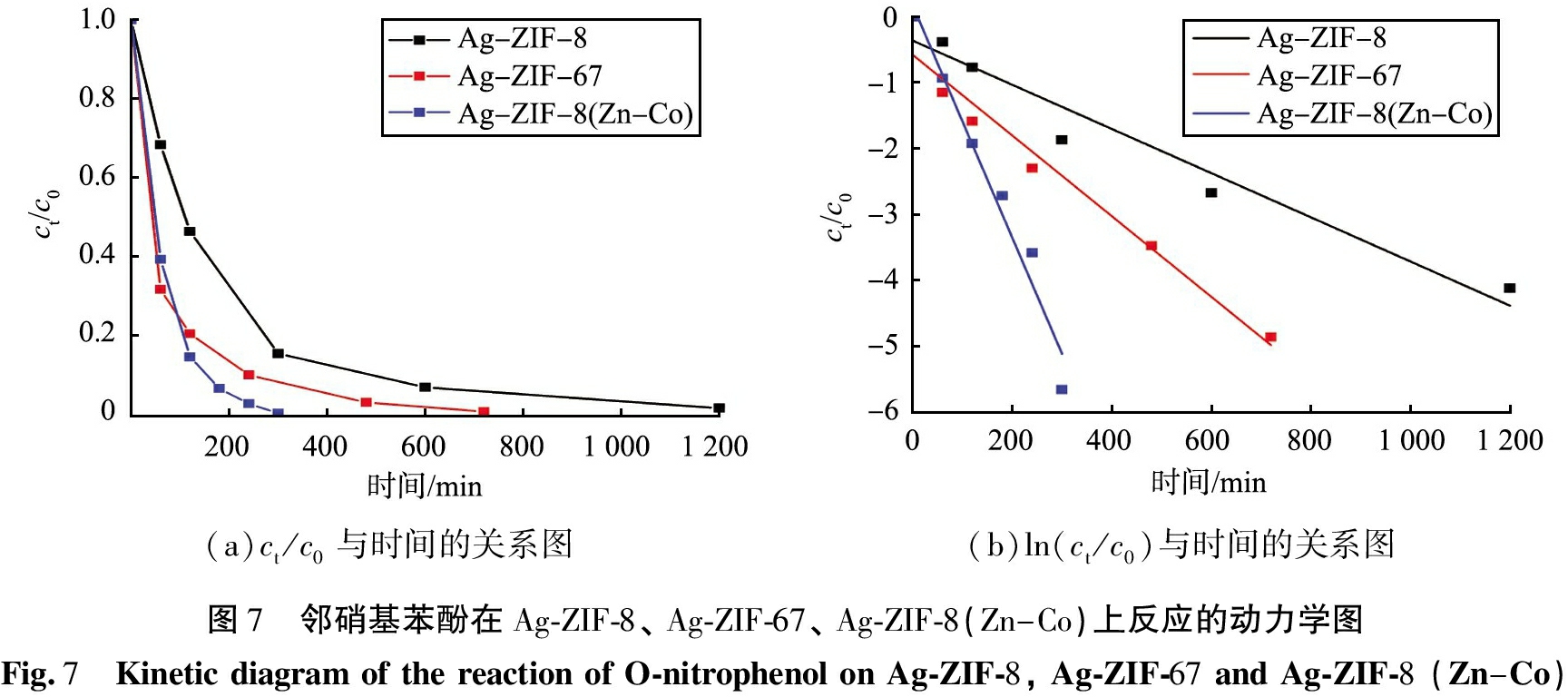
(a)ct/c0与时间的关系图(b)ln(ct/c0)与时间的关系图图7 邻硝基苯酚在Ag-ZIF-8、Ag-ZIF-67、Ag-ZIF-8(Zn-Co)上反应的动力学图Fig.7 KineticdiagramofthereactionofO-nitrophenolonAg-ZIF-8,Ag-ZIF-67andAg-ZIF-8(Zn-Co)
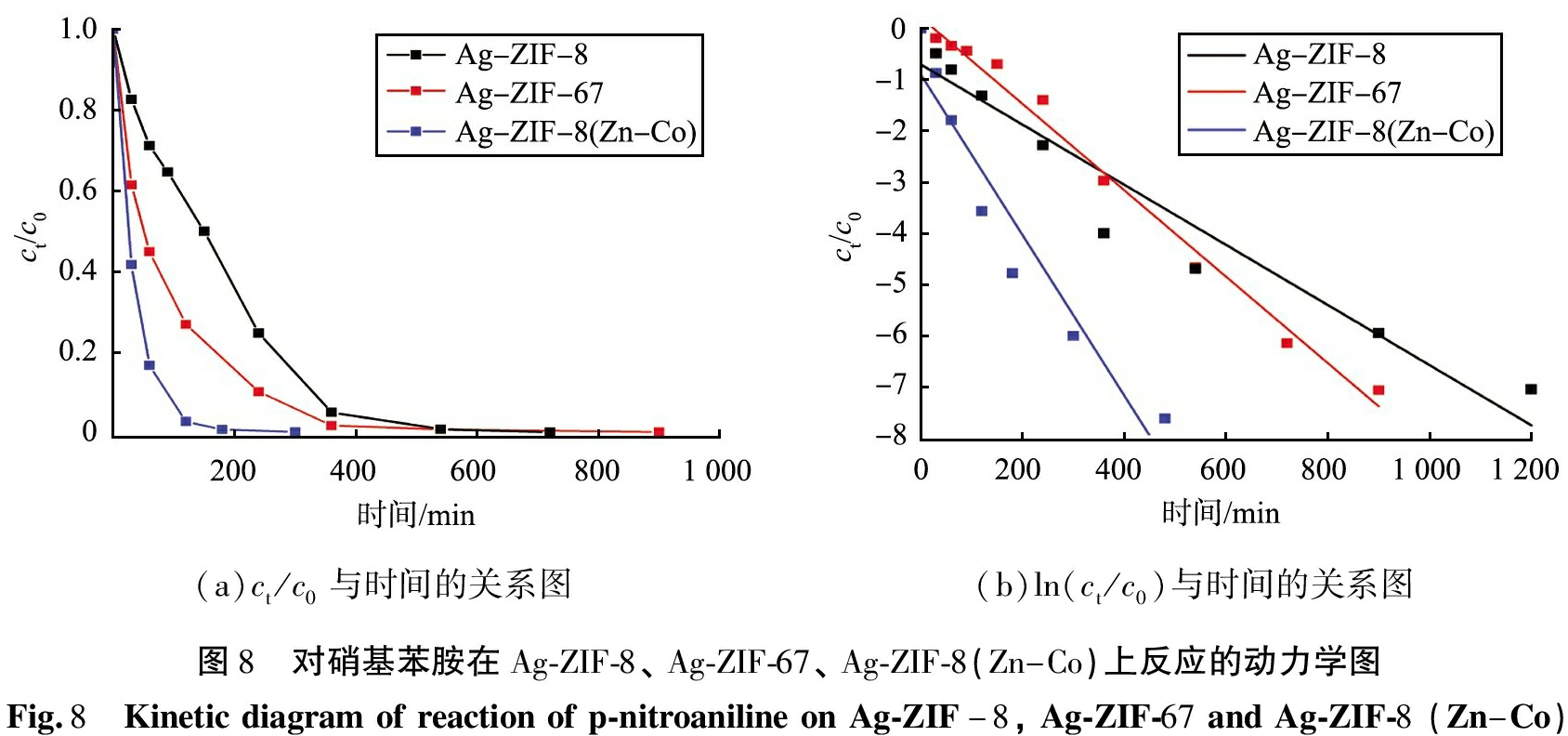
(a)ct/c0与时间的关系图(b)ln(ct/c0)与时间的关系图图8 对硝基苯胺在Ag-ZIF-8、Ag-ZIF-67、Ag-ZIF-8(Zn-Co)上反应的动力学图Fig.8 Kineticdiagramofreactionofp-nitroanilineonAg-ZIF-8,Ag-ZIF-67andAg-ZIF-8(Zn-Co)
不难看出,每一组污染物催化降解过程中均是Ag-ZIF-8(Zn-Co)表现最好,用于催化降解对硝基苯酚的Ag-ZIF-8(Zn-Co)的Kapp为1.08×10-4 s-1,而母体Ag-ZIF-8的仅为1.50×10-3 s-1。显然,Ag-ZIF-8(Zn-Co)显示出比Ag-ZIF-8和Ag-ZIF-67大得多的反应速率。其他研究者的研究与本项工作的对比如表1所示。
计算和比较转化频率(Tof)有助于进一步评估Ag-ZIF的催化性能。在所有制备的催化剂中,Ag-ZIF-8(Zn-Co)的最高的为2.056 min-1,而Ag-ZIF-8的仅为0.283 min-1,表明Zn和Co的协同作用可以显著提高Ag-ZIF-8的催化活性。与其他研究者报告银基催化剂相比,本次研究催化剂的Tof值也是理想的,如表1所示。
表1 各种典型MOF基吸附剂的吸附容量
Tab.1 Adsorption capacity of various typical MOF-based adsorbents
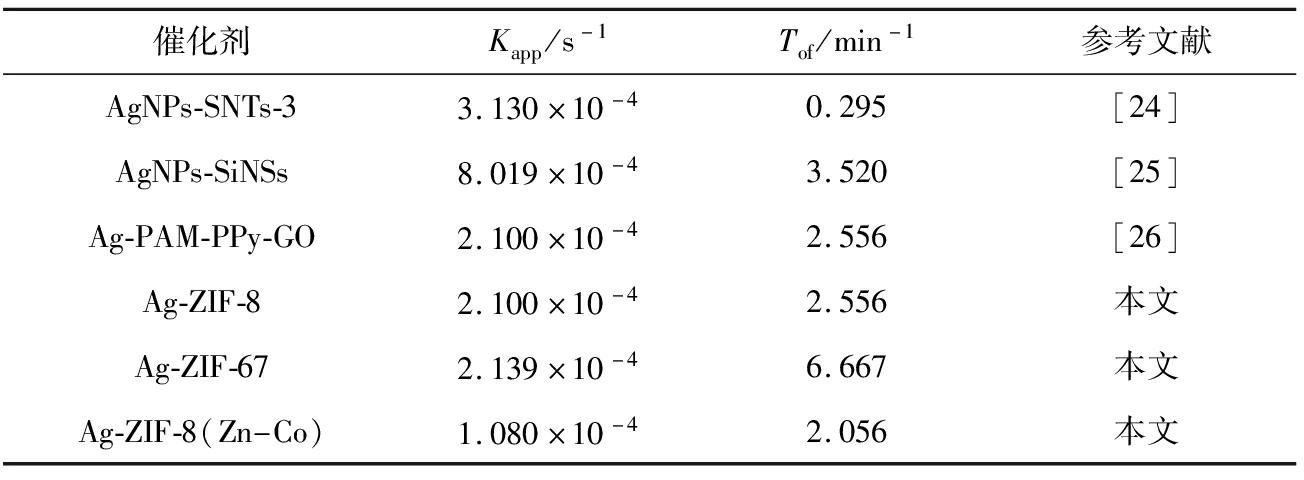
催化剂Kapp/s-1Tof/min-1参考文献AgNPs-SNTs-33.130×10-40.295[24]AgNPs-SiNSs8.019×10-43.520[25]Ag-PAM-PPy-GO2.100×10-42.556[26]Ag-ZIF-82.100×10-42.556本文Ag-ZIF-672.139×10-46.667本文Ag-ZIF-8(Zn-Co)1.080×10-42.056本文
2.4 催化剂重复使用性能
在Ag-ZIF-8(Zn-Co)可重复使用能力的测试中,采用相同的操作测量对硝基苯酚、邻硝基苯酚、对硝基苯胺3种不同的污染物加入催化剂后的去除率,一次测量完成后通过离心、洗涤回收催化剂,然后进入下一次实验,经过5次试验后,对去除率和重复使用次数作图,得到复合材料的重复使用性能,结果如图9所示。从图可以看出,在重复使用5次后,Ag-ZIF-8(Zn-Co)的催化能力略有降低,但Ag-ZIF-8(Zn-Co)仍然可以还原95%左右的对硝基苯酚,邻硝基苯酚和对硝基苯胺,仅降低了3%左右。结合图2(b)可得知,Ag-ZIF-8(Zn-Co)在使用过后,结构没有产生明显的破坏,有较好的稳定性。这说明ZIF-8(Zn-Co)是贵金属颗粒的极佳载体,与Ag纳米颗粒结合后可有效催化还原水中的硝基苯酚。
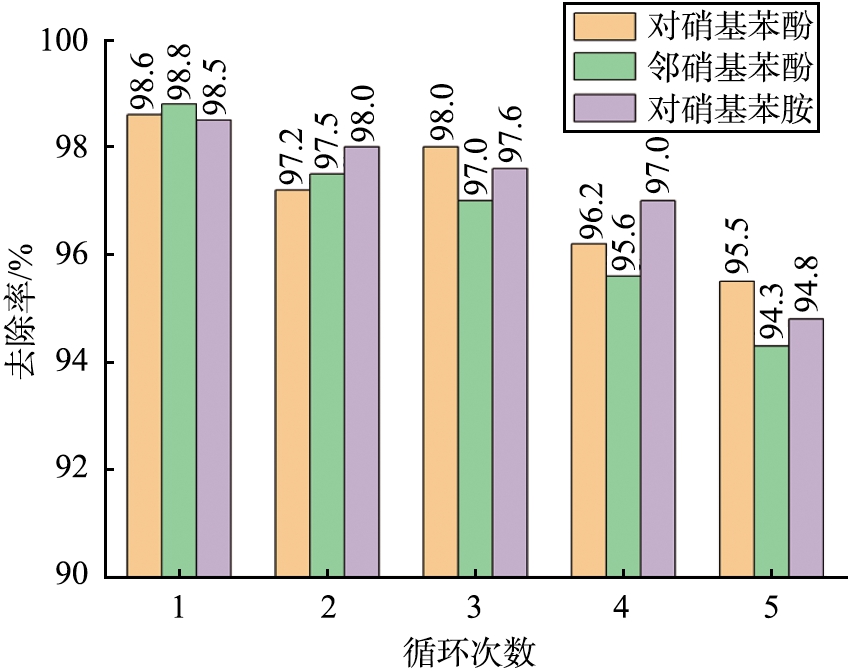
图9 Ag-ZIF-8(Zn-Co)催化还原的重复使用性能
Fig.9 Reusability of Ag-ZIF-8(Zn-Co)for catalytic reduction
2.5 催化反应机理分析
Ag-ZIF-8(Zn-Co)催化还原对硝基苯酚机理如下:在还原反应开始时,![]() 和对硝基苯酚被吸附在催化剂表面,此时ZIF材料的大表面积有利于加快吸附速率。然后,包封在ZIF孔道中的银纳米颗粒会将
和对硝基苯酚被吸附在催化剂表面,此时ZIF材料的大表面积有利于加快吸附速率。然后,包封在ZIF孔道中的银纳米颗粒会将![]() 的电子转移至对硝基苯酚离子上,然后在催化剂表面将对硝基苯酚还原为对氨基苯酚。在这个过程中,电子转移的过程是决定整个反应速率的关键步骤,我们认为多金属ZIF中2种金属离子的协同作用可以有效的提升电子转移速率,而小尺寸的Ag纳米颗粒也为催化剂提供了更多的活性位点,显著提升了复合材料的催化性能。
的电子转移至对硝基苯酚离子上,然后在催化剂表面将对硝基苯酚还原为对氨基苯酚。在这个过程中,电子转移的过程是决定整个反应速率的关键步骤,我们认为多金属ZIF中2种金属离子的协同作用可以有效的提升电子转移速率,而小尺寸的Ag纳米颗粒也为催化剂提供了更多的活性位点,显著提升了复合材料的催化性能。
3 结论
1)运用简单水热法结合双溶剂法制备的Ag-ZIF(Zn-Co)粒径约500~800 nm之间,略小于单金属的ZIF-8和ZIF-67。形貌规整均匀,在包封Ag纳米颗粒后外观没有明显的变化。小尺寸的Ag纳米颗粒均匀地包封在晶体内部,并且仅发生少量的团聚。
2)催化降解实验表明,所制备的Ag-ZIF-8(Zn-Co)具有优异的催化活性和可重复使用性,可高效的降解对硝基苯酚、邻硝基苯酚和对硝基苯胺废水。
3)在Ag-ZIF-8(Zn-Co)催化降解对硝基苯酚实验中,其转化频率和表观速率常数分别为2.056 min-1和1.080×10-4 s-1,与其现有研究所报道的银基催化剂相比,其催化性能也较好。与Ag-ZIF-8、Ag-ZIF-67的催化活性相比显著增强,Zn和Co独特的双金属协同作用可能是产生此结果的主要因素。
[1]SHEN X, ZHU L, WANG N, et al.Selective photocatalytic degradation of nitrobenzene facilitated by molecular imprinting with a transition state analog[J].Catalysis Today, 2014, 225: 164-170.
[2]WU X Y, QI H X, NING J J, et al.One silver(I)/tetraphosphine coordination polymer showing good catalytic performance in the photodegradation of nitroaromatics in aqueous solution[J].Applied Catalysis B: Environmental, 2015, 168/169: 98-104.
[3]DIN M I, KHALID R, HUSSAIN Z, et al.Nanocatalytic assemblies for catalytic reduction of nitrophenols: a critical review[J].Critical Reviews In Analytical Chemistry, 2020, 50(4): 322-338.
[4]PRADHAN N, PAL A and PAL T Silver nanoparticle catalyzed reduction of aromatic nitro compounds[J].Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2002, 196(2): 247-257.
[5]AIJAZ A, KARKAMKAR A, CHOI Y J, et al.Immobilizing highly catalytically active Pt nanoparticles inside the pores of metal-organic framework: a double solvents approach[J].Journal of the American Chemical Society, 2012, 134(34): 13926-13929.
[6]JIANG H L, LIU B, AKITA T, et al.Au@ZIF-8: CO oxidation over gold nanoparticles deposited to metal organic framework[J].Journal of the American Chemical Society, 2009,131(32): 11302-11303.
[7]LU G, LI S, GUO Z, et al.Imparting functionality to a metal-organic framework material by controlled nanoparticle encapsulation[J].Nature Chemistry, 2012, 4: 310.
[8]GARCíA BLANCO A A, VALLONE A F, GIL A, et al.A comparative study of various microporous materials to store hydrogen by physical adsorption[J].International Journal of Hydrogen Energy, 2012, 37(19): 14870-14880.
[9]NANDI S, DE LUNA P, DAFF T D, et al.A single-ligand ultra-microporous MOF for precombustion CO2 capture and hydrogen purification[J].Science Advances, 2015, 1(11): e1500421.
[10]SOMAYAJULU RALLAPALLI P B, RAJ M C, PATIL D V, et al.Activated carbon@MIL-101(Cr): a potential metal-organic framework composite material for hydrogen storage[J].International Journal of Energy Research, 2013, 37(7): 746-753.
[11]ZHOU H-C, LONG J R, YAGHI O M.Introduction to metal-organic frameworks[J].Chemical Reviews, 2012, 112(2): 673-674.
[12]LI Y W, HE K H, BU X H.Bottom-up assembly of a porous MOF based on nanosized nonanuclear zinc precursors for highly selective gas adsorption[J].Journal of Materials Chemistry A, 2013, 1(13): 4186-4189.
[13]LALONDE M, BURY W, KARAGIARIDI O, et al.Transmetalation: routes to metal exchange within metal-organic frameworks[J].Journal of Materials Chemistry A, 2013, 1(18): 5453-5468.
[14]LI T, SULLIVAN J E, ROSI N L.Design and preparation of a core-shell metal-organic framework for selective CO2 capture[J].Journal of the American Chemical Society, 2013, 135(27): 9984-9987.
[15]REN J, MUSYOKA N M, LANGMI H W, et al.Fabrication of core-shell MIL-101(Cr)@UiO-66(Zr)nanocrystals for hydrogen storage[J].International Journal of Hydrogen Energy, 2014, 39(27): 14912-14917.
[16]KAUR G, RAI R K, TYAGI D, et al.Room-temperature synthesis of bimetallic Co-Zn based zeolitic imidazolate frameworks in water for enhanced CO2 and H2 uptakes[J].Journal of Materials Chemistry A, 2016, 4(39): 14932-14938.
[17]PANCHARIYA D K, RAI R K, ANIL KUMAR E, et al.Core-shell zeolitic imidazolate frameworks for enhanced hydrogen storage[J].ACS Omega, 2018, 3(1): 167-175.
[18]TANG J, SALUNKHE R R, LIU J, et al.Thermal conversion of core-shell metal-organic frameworks: a new method for selectively functionalized nanoporous hybrid carbon[J].Journal of the American Chemical Society, 2015, 137(4): 1572-1580.
[19]YANG J, ZHANG F, LU H, et al.Hollow Zn/Co ZIF particles derived from core-shell ZIF-67@ZIF-8 as selective catalyst for the semi-hydrogenation of acetylene[J].Angewandte Chemie International Edition, 2015, 54(37): 10889-10893.
[20]PAN Y, SUN K, LIU S, et al.Core-Shell ZIF-8@ZIF-67-Derived CoP nanoparticle-embedded N-doped carbon nanotube hollow polyhedron for efficient overall water splitting[J].Journal of the American Chemical Society, 2018, 140(7): 2610-2618.
[21]ZHANG J, ZHANG T, XIAO K, et al.Novel and facile strategy for controllable synthesis of multilayered core-shell zeolitic imidazolate frameworks[J].Crystal Growth and Design, 2016, 16(11): 6494-6498.
[22]ZHOU K, MOUSAVI B, LUO Z, et al.Characterization and properties of Zn/Co zeolitic imidazolate frameworks vs.ZIF-8 and ZIF-67[J].Journal of Materials Chemistry A, 2017, 5(3): 952-957.
[23]JIANG H L, AKITA T, ISHIDA T, et al.Synergistic catalysis of Au@Ag core shell nanoparticles stabilized on metal organic framework[J].Journal of the American Chemical Society, 2011, 133(5): 1304-1306.
[24]ZHANG Z, SHAO C, SUN Y, et al.Tubular nanocomposite catalysts based on size-controlled and highly dispersed silver nanoparticles assembled on electrospun silica nanotubes for catalytic reduction of 4-nitrophenol[J].Journal of Materials Chemistry, 2012, 22(4): 1387-1395.
[25]WANG R L, LI D P, WANG L J, et al.The preparation of new covalent organic framework embedded with silver nanoparticles and its applications in degradation of organic pollutants from waste water[J].Dalton Transactions, 2019, 48(3): 1051-1059.
[26]MAO H, JI C, LIU M, et al.Enhanced catalytic activity of Ag nanoparticles supported on polyacrylamide/polypyrrole/graphene oxide nanosheets for the reduction of 4-nitrophenol[J].Applied Surface Science, 2018, 434: 522-533.