氨氮是水体中主要的氮污染源[1],氨氮由非离子态氨(NH3—N)和离子态氨![]() 组成,其存在形式主要取决于废水的pH值和温度[2],过量积累的氨氮易造成水体富营养化,减少溶解氧,对水生生物产生毒性,最终危及水生生态系统[3]。当水体中
组成,其存在形式主要取决于废水的pH值和温度[2],过量积累的氨氮易造成水体富营养化,减少溶解氧,对水生生物产生毒性,最终危及水生生态系统[3]。当水体中![]() 的质量浓度大于1 mg/L时,会使生物体中血液结合氧的能力下降; 当水体中
的质量浓度大于1 mg/L时,会使生物体中血液结合氧的能力下降; 当水体中![]() 的质量浓度大于3 mg/L时,在 24~96 h内,金鱼和鳊鱼等大部分鱼类和水中生物就会死亡[4]。硫化物主要以H2S、 HS-和S2-形式存在[5],具有一定毒性,导致水体出现黑臭现象,研究表明,水体中H2S的质量浓度大于13 mg/L时,会对人类健康造成极大伤害[6]。
的质量浓度大于3 mg/L时,在 24~96 h内,金鱼和鳊鱼等大部分鱼类和水中生物就会死亡[4]。硫化物主要以H2S、 HS-和S2-形式存在[5],具有一定毒性,导致水体出现黑臭现象,研究表明,水体中H2S的质量浓度大于13 mg/L时,会对人类健康造成极大伤害[6]。
目前,废水中![]() 硫化物主要的去除方法包括:光电催化法、 厌氧氨氧化法、 气提法、 化学沉淀法、 吸附法及生物处理法等,其中生化法是去除氨氮、 硫化物较为有效的传统方法。上述方法去除氨氮存在一个共同特点,即均需要一定的动力源,而对于一些没有动力来源的河、 湖、 沟、 渠等大流域水体,氨氮、 硫污染物的去除,这些方法存在很大的局限性。大流域水体污染的特点是水量大、污染程度低,野外没动力源,且以微溶或不溶的悬浮性污染物为主,要求低成本处理和不阻碍(或少阻碍)水体流动,故此,采用具有一定吸附性能(或离子交换功能)的天然矿物颗粒、 再造颗粒,处理大流域水体低污染物是一个不错的选择。天然矿物具有无毒、 来源广泛、 价格低廉及良好的物理化学性质(高比表面积和离子交换容量、 强吸附和催化性能等)等诸多优点,作为吸附材料已经较为广泛地应用于水处理当中。矿物颗粒对于流域水体污染物处理,在要求其本身吸附功能的同时,还要求材料具有较好的水流通量。蛭石具有独特的层片状结构,表现出良好的吸附和离子交换性能,且对氨氮污染物较敏感,在污水处理中有着非常广阔的应用前景,但蛭石颗粒粒径较小,通量较低,且吸附容量也有待提高。火山岩作为大通量的多孔吸附过滤材料,在河道水体治理也有应用,且富含吸附去除硫化物敏感的铁元素。
硫化物主要的去除方法包括:光电催化法、 厌氧氨氧化法、 气提法、 化学沉淀法、 吸附法及生物处理法等,其中生化法是去除氨氮、 硫化物较为有效的传统方法。上述方法去除氨氮存在一个共同特点,即均需要一定的动力源,而对于一些没有动力来源的河、 湖、 沟、 渠等大流域水体,氨氮、 硫污染物的去除,这些方法存在很大的局限性。大流域水体污染的特点是水量大、污染程度低,野外没动力源,且以微溶或不溶的悬浮性污染物为主,要求低成本处理和不阻碍(或少阻碍)水体流动,故此,采用具有一定吸附性能(或离子交换功能)的天然矿物颗粒、 再造颗粒,处理大流域水体低污染物是一个不错的选择。天然矿物具有无毒、 来源广泛、 价格低廉及良好的物理化学性质(高比表面积和离子交换容量、 强吸附和催化性能等)等诸多优点,作为吸附材料已经较为广泛地应用于水处理当中。矿物颗粒对于流域水体污染物处理,在要求其本身吸附功能的同时,还要求材料具有较好的水流通量。蛭石具有独特的层片状结构,表现出良好的吸附和离子交换性能,且对氨氮污染物较敏感,在污水处理中有着非常广阔的应用前景,但蛭石颗粒粒径较小,通量较低,且吸附容量也有待提高。火山岩作为大通量的多孔吸附过滤材料,在河道水体治理也有应用,且富含吸附去除硫化物敏感的铁元素。
本文中以蛭石、 火山岩为吸附材料,通过进行层间或表面修饰,制备可吸附水体中氨氮、硫等污染物,且粒径分别为8~12 mm、 20~35 mm的蛭石和火山岩矿物颗粒;采用2种矿物颗粒粒级组配,制得可用于流域水体净化的复合矿物颗粒;研究样品对氨氮、硫的吸附性能,并探讨蛭石对氨氮、 火山岩对硫化物的吸附机理。
1 实验
1.1 原料与试剂
蛭石(河北省灵寿县泽洋公司),化学组分(w/%)为:SiO2,54.197; Al2O3,13.106; Fe2O3,9.94;CaO,8.088;MgO,4.297;Co3O4,4.048;K2O,2.998;TiO2,2.349;BaO,0.483;Na2O,0.082;火山岩(吉林嘉鹏公司),化学组分(w/%)为:SiO2,52.031;Al2O3,17.526;Fe2O3,9.876;CaO,7.987;Na2O,3.576;MgO,3.444;K2O,2.204;TiO2,1.921;P2O5,1.019;MnO,0.161。氯化钠(NaCl)、氯化铁(FeCl3)、 氯化铵(NH4Cl)(均为分析纯,北京化工厂)。
1.2 方法
1.2.1 制备
在烧杯中配置浓度为1.4 mol/L的NaCl溶液200 mL,加入20 g蛭石,磁力搅拌16 h后,抽滤、干燥,得到Na化蛭石;在烧杯中配置0.15 mol/L的 FeCl3溶液200 mL,加入40 g火山岩,磁力搅拌2 h,抽滤、干燥,得到改性火山岩。蛭石用水清洗2次,去除细粒烘干待用;火山岩用水清洗2次,去除粉末杂质烘干待用。
1.2.2 分析与测试
利用扫描电子显微镜(SEM, 电压为10 kV)、 D8 Advance型X射线衍射仪(XRD, Cu靶Kα辐射,工作电压为50 kV,电流为50 mA,2θ值为5°~90°)、 Bruker Vertex 70型傅里叶红外光谱(FTIR,波数为4 000~400 cm-1,分辨率为4 cm-1)、 X射线光电子能谱分析(XPS,以Al靶Kα辐射,光子能量为1 486.6 eV的X射线为辐射源)、 激光显微共聚焦拉曼光谱仪对样品进行表征,溶液中离子浓度采用电感耦合等离子体原子发射光谱法(ICP-AES)测试。
1.2.3 矿物颗粒粒级组配
根据吸附效果与水流流速,将Na化蛭石颗粒与改性火山岩颗粒进行组配(蛭石颗粒粒径为8~12 mm,火山岩颗粒粒径为20~35 mm),将批量复合矿物颗料进行网袋式模块化组装,采用复合矿物颗粒对实际流域水体进行现场应用研究,以探究Na化蛭石颗粒与改性火山岩颗粒最佳质量配比。
1.2.4 吸附研究
以NH4Cl为水体中氨氮来源,将3.819 g的NH4Cl溶于蒸馏水中并定容至1 L,得到1 g/L的NH4Cl溶液。取10 mL溶液至1 L容量瓶中,定容至1 L,可得到10 mg/L的NH4Cl溶液,即质量浓度为10 mg/L的含氨氮模拟废水(使用此方法可配置不同浓度的氨氮模拟废水)。模拟废水初始pH值使用稀HCl与NaOH溶液进行调节。量取50 mL实验室配置的已知浓度氨氮废水于100 mL烧杯中,称取2 g Na化蛭石加入烧杯中,磁力搅拌4 h,水样离心处理,采用分光光度法测定上清液氨氮浓度,计算样品对氨氮的去除率及吸附量。
以Na2S为水体中硫的来源,配置质量浓度为200 mg/L的含硫废水,用质量分数为8%的稀HCl和10%的NaOH溶液调节溶液初始pH值。量取50 mL已知浓度的含硫废水于烧杯中,称取0.5 g火山岩(改性火山岩)加入烧杯中,磁力搅拌4 h,抽滤得到吸附硫后的火山岩,采用元素分析仪测定吸附前后火山岩中硫的含量。计算吸附剂的吸附量qe和吸附率R,
qe=(ρ0-ρe)V/m
(1)
R=(ρ0-ρe)/ρ0
(2)
式中: qe为平衡吸附容量,mg/g; ρ0为初始质量浓度,mg/L; ρe为平衡质量浓度,mg/L; V为溶液体积,L; m为吸附剂质量,g。
2 结果与讨论
2.1 样品微观形貌分析
实验室研究和现场流域水体应用研究所采用的复合矿物颗粒中,火山岩颗粒以骨架支撑作用、吸附去除硫化物为主,对不溶性污染物(悬浮物)有过滤功能;蛭石颗粒以吸附或离子交换功能为主。火山岩与蛭石的SEM图像如图1所示,从图1 a)和1 b)可以看出,火山岩表面粗糙凹凸不平,具有天然多孔结构,孔径较大;从图1 c)和1 d)可以看到,蛭石的层片状结构,结构紧密,层间距较小。

a)火山岩原土(2.2×103倍)b)火山岩原土(9×103倍)c)蛭石原土(9×103倍)d)蛭石原土(9×103倍)图1 火山岩和蛭石样品的SEM图像Fig.1 SEM images of volcanic rock and vermiculite samples
2.2 样品结构表征分析
蛭石吸附氨氮前、后的XRD图谱如图2所示。由图可知,蛭石特征衍射峰出现在7.3°附近,所对应的晶面为(001)。7.8°、 8.7°处的衍射峰位表明蛭石中含有一些云母杂质[7]。吸附氨氮后,蛭石特征衍射峰强度降低,表明蛭石在吸附氨氮过程中结构受到影响。分析其原因是由于离子半径和离子水合能不同,离子交换会导致蛭石夹层崩塌[8]。
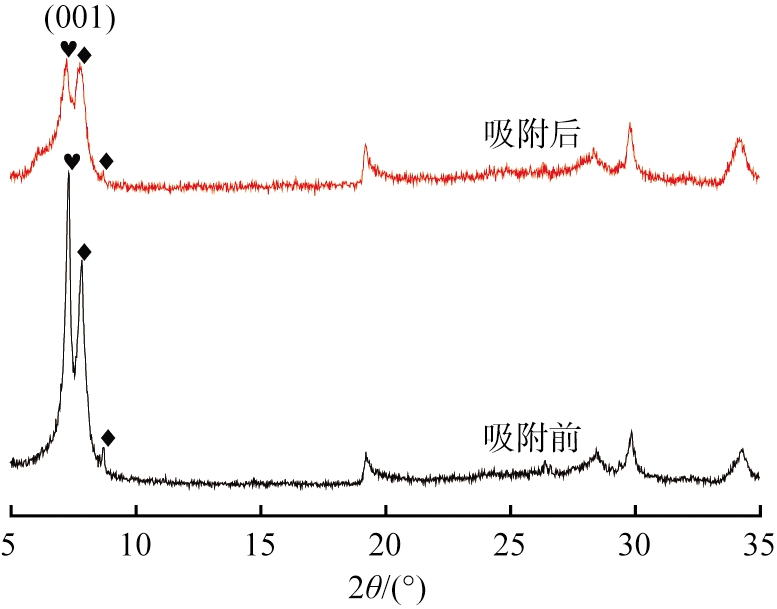
图2 吸附氨氮前、 后蛭石的XRD图谱
Fig.2 XRD patterns of vermiculite before and after adsorption of ammonia nitrogen
火山岩修饰前、 后的XRD图谱如图3所示。由图可看出,火山岩在24.128°、 33.117°、 40.828°、 49.417°、 54.002°、 62.385°、 63.962°处的特征衍射峰与Fe2O3标准卡片(JCPDS PDF#72-0469)高度吻合,对应晶面分别为(012)、(104)、(113)、(024)、(116)、(214)、(300),判定为Fe2O3特征衍射峰。在29.855°(-221)和35.666 °(221)处的特征衍射峰与(Mg0.962Fe0.038)(Ca0.999Mg0.04)(Si2O6)标准卡片(JCPDS PDF#83-0104)高度吻合,判定为(Mg0.962Fe0.038)(Ca0.999Mg0.04)(Si2O6)的特征衍射峰。在21.962°(-202)、 23.629°(112)和27.836°(-204)处的特征衍射峰与Ca(Al2Si2O8) 的标准卡片(JCPDS PDF#76-0948)高度吻合,判定为Ca(Al2Si2O8)的特征衍射峰。处理后火山岩在14.347°、 15.979°、 17.811°处新出现3个高强度特征衍射峰,与Fe(SO4)(OH)(H2O)2标准卡片(JCPDS PDF#71-2397)高度吻合,判定为Fe(SO4)(OH)(H2O)2的特征衍射峰,改性火山岩中铁离子含量有所提高。
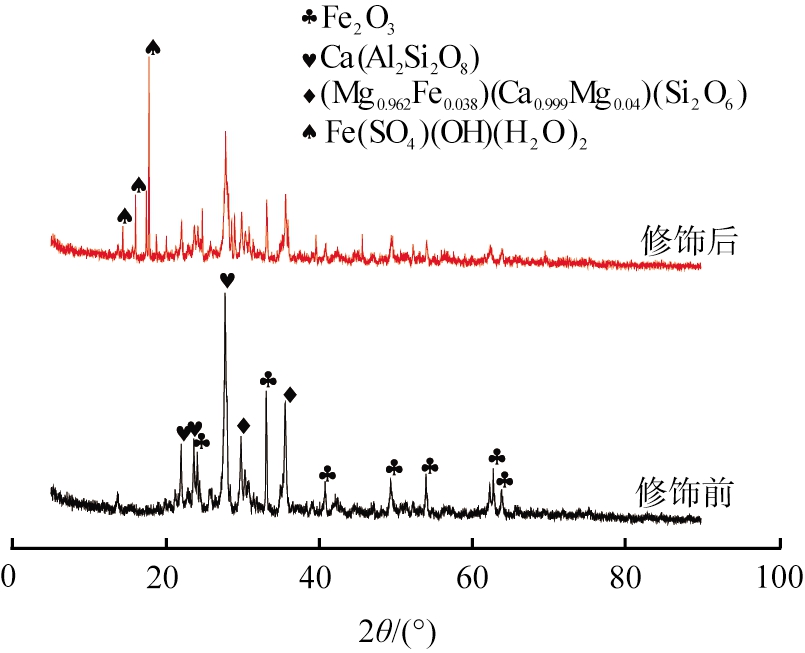
图3 修饰前、 后火山岩的XRD图谱
Fig.3 XRD patterns of volcanic rocks before and after modification
2.3 样品吸附性能研究
在不同条件下处理前、 后蛭石对氨氮吸附性能,以及处理前、后火山岩对硫化物吸附性能的影响如图4所示。反应时间对单位吸附量的影响如图4 a)所示。在50 mL质量浓度为10 mg/L的氨氮模拟废水中加入1 g原蛭石(Na化蛭石),模拟废水pH值为7的条件下,不同反应时间(0.5、 1、 1.5、 2、 3、 4、 5、 6、 7 h)对单位吸附量的影响。从图中可以看出,2种蛭石早期对氨氮均可实现快速吸附,吸附量增加较快;后期吸附量增加缓慢,表明已到达吸附平衡。吸附反应时间为1 h后,原蛭石与Na化蛭石对氨氮均有较好去除效果,最高吸附量分别为:73.8%、 86.4%。
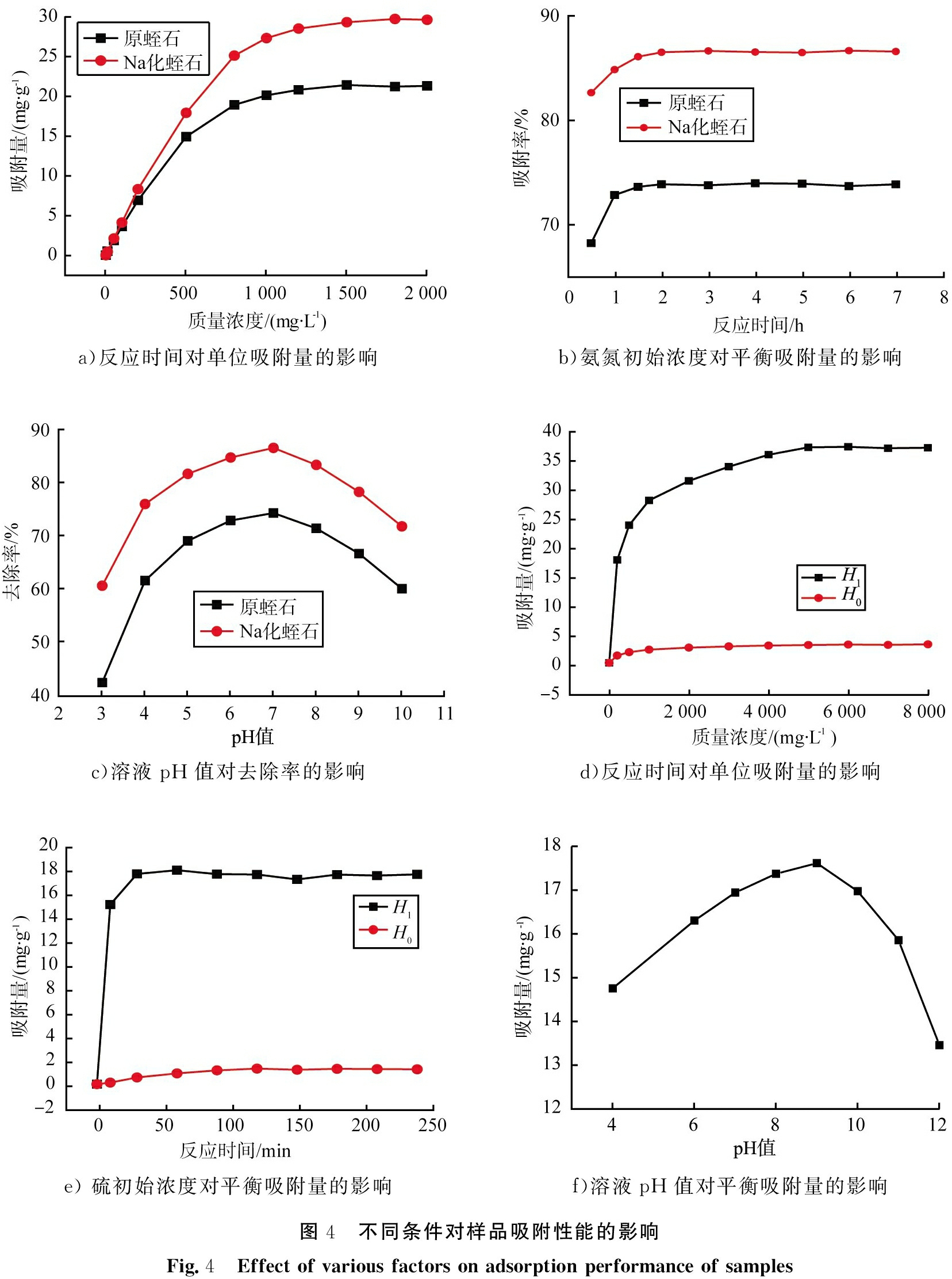
a)反应时间对单位吸附量的影响b)氨氮初始浓度对平衡吸附量的影响c)溶液pH值对去除率的影响d)反应时间对单位吸附量的影响e) 硫初始浓度对平衡吸附量的影响f)溶液pH值对平衡吸附量的影响图4 不同条件对样品吸附性能的影响Fig.4 Effect of various factors on adsorption performance of samples
氨氮初始浓度对平衡吸附量的影响如图4 b)所示。在50 mL氨氮模拟废水中加入1 g原蛭石(Na化蛭石),模拟废水pH值为7、 反应时间为2 h的条件下,氨氮初始浓度对平衡吸附量的影响。氨氮初始浓度分别设置为10、 50、 100、 200、 500、 800、 1 000、 1 200、 1 500、 1 800、 2 000 mg/L。从图中可以看出,随着氨氮初始浓度的增大,蛭石对氨氮的平衡吸附量均呈现出先增加并逐渐趋于稳定的趋势,当氨氮初始浓度为1 500 mg/L时,原蛭石与Na化蛭石的平衡吸附量分别为: 21.4、 29.3 mg/g。
溶液pH值对去除率的影响如图4 c)所示。在50 mL质量浓度为 10 mg/L的氨氮模拟废水中加入1 g原蛭石(Na化蛭石),反应时间为2 h的条件下,氨氮模拟废水初始pH值对去除率的影响。氨氮模拟废水初始pH值分别设置为: 3、 4、 5、 6、 7、 8、 9、 10。从图中可以看出,两种蛭石均在pH=7时表现出最佳的吸附性能,对氨氮的去除率最高,分别为:74.1%、 86.4%,在酸性及碱性条件下原蛭石及Na化蛭石的吸附性能均有不同程度的下降。分析其原因,在酸性环境中,溶液中H+含量增多,H+与![]() 存在竞争吸附现象,使得原蛭石及Na化蛭石对氨氮的吸附性能降低;在碱性环境中,
存在竞争吸附现象,使得原蛭石及Na化蛭石对氨氮的吸附性能降低;在碱性环境中,![]() 会与OH-结合生成氨水,使得溶液中的
会与OH-结合生成氨水,使得溶液中的![]() 浓度减少,氨氮去除率降低。
浓度减少,氨氮去除率降低。
反应时间对单位吸附量的影响如图4 d)所示。在50 mL质量浓度为200 mg/L的含硫模拟废水中加入0.5 g火山岩(改性火山岩)、模拟废水pH值为9的条件下,不同反应时间(10、 30、 60、 90、 120、 150、 180、 210、 240 min)对单位吸附量的影响。从图中可以看出,原火山岩对硫吸附效率较低,随着反应时间增加,平衡吸附量缓慢升高,吸附容量约为1.3 mg/g。改性后火山岩对硫化物有较好的吸附能力,并可实现快速吸附,反应10 min吸附容量可达到15.1 mg/g,吸附30 min可达到平衡,吸附容量为17.6 mg/g。其中H0、 H1分别代表原火山岩、改性后火山岩的吸附曲线。
硫初始浓度对平衡吸附量的影响如图4 e)所示。在50 mL 200 mg/L含硫模拟废水中加入0.5 g火山岩(改性火山岩)、模拟废水pH值为9、 反应时间为120 min的条件下,硫初始浓度对平衡吸附量的影响。硫初始浓度分别设置为200、 500、 1 000、 2 000、 3 000、 4 000、 5 000、 6 000、 7 000、 8 000 mg/L。从图中可以看出,随氨氮初始浓度增大,两种火山岩对硫化物平衡吸附量均呈现出先增加后逐渐趋于稳定的趋势,改性后火山岩增加幅度提升明显。初始浓度为5 000 mg/L时,可达吸附平衡,火山岩改性前后的最大吸附容量分别为:3.1、 36.9 mg/g。
溶液pH值对平衡吸附量的影响如图4 f)所示。在50 mL质量浓度为200 mg/L的含硫模拟废水中加入0.5 g改性火山岩,反应时间为30 min的条件下,含硫模拟废水初始pH值对平衡吸附量的影响。含硫模拟废水初始pH值分别设置为:4、 5、 6、 7、 8、 9、 10、 11、 12。从图中可以看出,改性火山岩在pH=9时表现出最佳吸附性能,平衡吸附量为17.58 mg/g,在pH<9或者pH>9时吸附效率均有下降。分析其原因,当pH<9时,溶液中增多的H+会与溶液中的HS-结合生成H2S气体逸出溶液进入空气中,使得溶液中硫的浓度减少,随着pH的不断减小,溶液中硫的浓度会相应的不断减少,导致改性火山岩对硫的平衡吸附量不断减小。当pH>9时,溶液中增多的OH-会抑制溶液中![]() 的水解反应,造成溶液中HS-浓度的减少,进而影响与改性火山岩吸附硫有关化学反应的发生,从而使得改性火山岩对硫的平衡吸附量降低。
的水解反应,造成溶液中HS-浓度的减少,进而影响与改性火山岩吸附硫有关化学反应的发生,从而使得改性火山岩对硫的平衡吸附量降低。
2.4 吸附机理分析
2.4.1 蛭石对氨氮的吸附机理
吸附氨氮前、 后蛭石的FTIR谱图如图5所示。由图可知,457、 683、 1 002 cm-1处的吸收峰分别为蛭石晶体片层中Si—O的伸缩振动、M—O—Si的振动(其中M代表金属)以及Si—O—Si弯曲振动引起的。1 648 cm-1处的吸收峰代表蛭石层间吸附水O—H的弯曲振动峰,3 410、 3 715 cm-1处的吸收峰分别为四面体片层中—OH的伸缩振动峰和Si—OH基团中O—H的拉伸振动峰[7,9]。
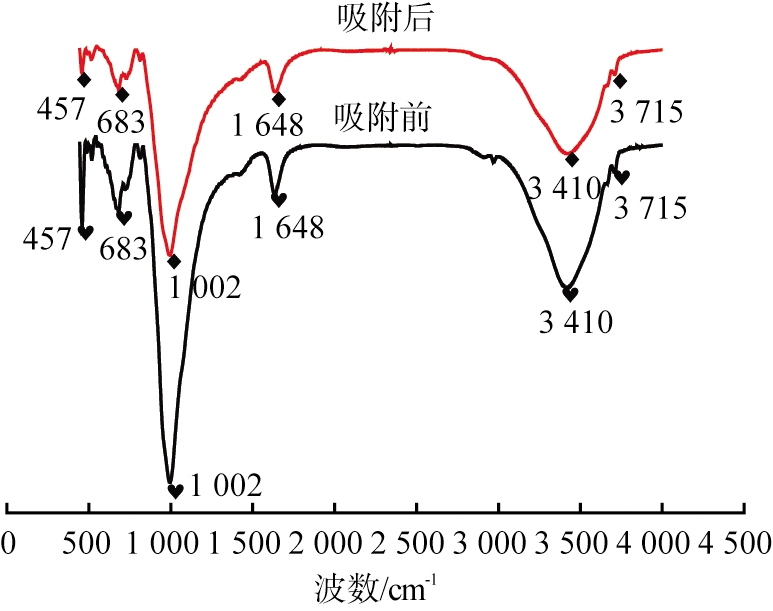
图5 吸附氨氮前、后蛭石的FTIR图像
Fig.5 FTIR images of vermiculite before and after adsorption of ammonia nitrogen
对比吸附前和吸附后曲线可以发现,吸附氨氮前后蛭石的特征吸收峰的位置没有发生变化,说明![]() 进入蛭石层间后,没有形成新的化学键。
进入蛭石层间后,没有形成新的化学键。
在100 mL烧杯中分别加入50 mL含氨氮废水和蒸馏水(对比实验),加入1 g蛭石样品,吸附搅拌0.5 h,2个水样进行离心处理得上清液。采用ICP-AES测定上清液中Na+、 K+、 Ca2+、 Mg2+的浓度;分光光度法测试含氨氮废水处理前后氨氮浓度。
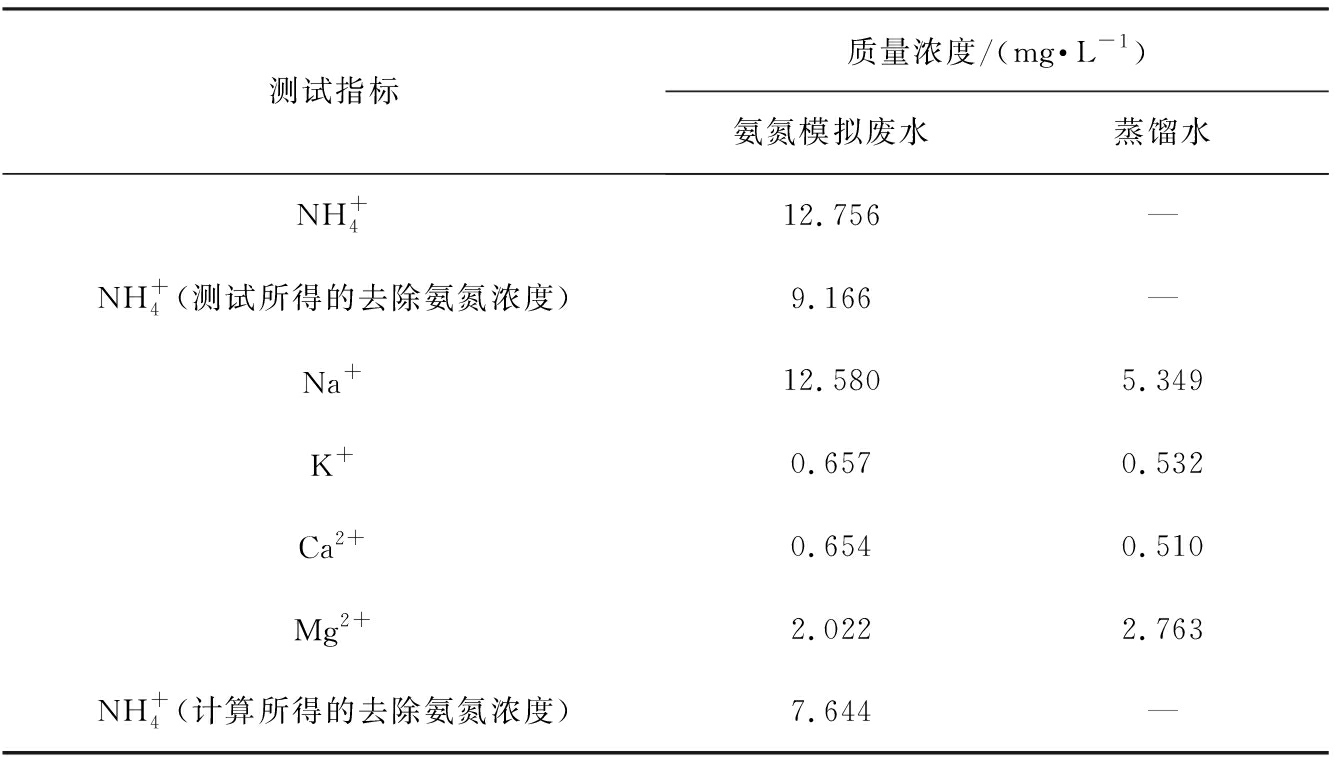
表1列出了水样中Na+、 K+、 Ca2+、 Mg2+的质量浓度。采用分光光度法测定的氨氮浓度,为了获得样品与含氨氮废水中![]() 交换的Na+、 K+、 Ca2+、 Mg2+离子的浓度,先测定样品处理废水后水样中Na+、 K+、Ca2+、 Mg2+离子的总浓度,从中扣除蛭石样品在蒸馏水中释放的Na+、 K+、 Ca2+、 Mg2+的浓度。Na+、 K+、 Ca2+、 Mg2+离子会与等量的
交换的Na+、 K+、 Ca2+、 Mg2+离子的浓度,先测定样品处理废水后水样中Na+、 K+、Ca2+、 Mg2+离子的总浓度,从中扣除蛭石样品在蒸馏水中释放的Na+、 K+、 Ca2+、 Mg2+的浓度。Na+、 K+、 Ca2+、 Mg2+离子会与等量的![]() 交换,即1个Na+与1个
交换,即1个Na+与1个![]() 交换,1个Ca2+与2个
交换,1个Ca2+与2个![]() 交换。这样可通过表1的结果,计算出蛭石在废水中与
交换。这样可通过表1的结果,计算出蛭石在废水中与![]() 发生离子交换后去除的
发生离子交换后去除的![]() 的理论浓度。对比计算与实验测试数据,得到去除的
的理论浓度。对比计算与实验测试数据,得到去除的![]() 浓度。发现实验测试所得去除
浓度。发现实验测试所得去除![]() 浓度略大于计算的,由此可以推断,离子交换是蛭石吸附氨氮的主要机理,另外还存在一定的物理吸附。
浓度略大于计算的,由此可以推断,离子交换是蛭石吸附氨氮的主要机理,另外还存在一定的物理吸附。
进行蛭石解吸实验,将吸附氨氮后蛭石样品,加入100 mL蒸馏水中搅拌3 h,离心处理取上清液,检测氨氮浓度,通过计算所得的数据作为蛭石样品通过物理吸附的氨氮量。通过测试得到蛭石解吸的氨氮的质量浓度为1.505 mg/L。结合表1结果可以看出,1.505 mg/L(物理吸附)+7.644 mg/L(离子交换)=9.149 mg/L,与实际测得蛭石样品处理去除的氨氮浓度(9.166 mg/L)非常接近,因此,样品吸附氨氮机理主要为离子交换作用,其次还包括蛭石对氨氮的物理吸附作用。
表1 相关离子浓度测试结果
Tab.1 Relevant ion concentration test results
测试指标质量浓度/(mg·L-1)氨氮模拟废水蒸馏水NH+412.756—NH+4(测试所得的去除氨氮浓度)9.166—Na+12.5805.349K+0.6570.532Ca2+0.6540.510Mg2+2.0222.763NH+4(计算所得的去除氨氮浓度)7.644—
2.4.2 火山岩对硫化物的吸附机理
火山岩吸附硫前、后样品的红外光谱图如图6 a)所示,局部放大图如图6 b)所示。由图6 a)可知,467、 1 034 cm-1处为火山岩中Si—O—Si弯曲振动,540 cm-1处为Si—O—Al振动,1 640、 3 430 cm-1处代表火山岩吸附水—OH的弯曲和拉伸振动,3620 cm-1处为火山岩内部—OH拉伸振动[10],样品强特征吸收峰的位置没有发生明显变化。由图6 b)可知,吸附后样品在451 cm-1增加了一处特征吸收峰,归因于Fe2+—[S2]2-的伸缩振动峰[11]。可见,样品在吸附硫的过程中有FeS2的生成。
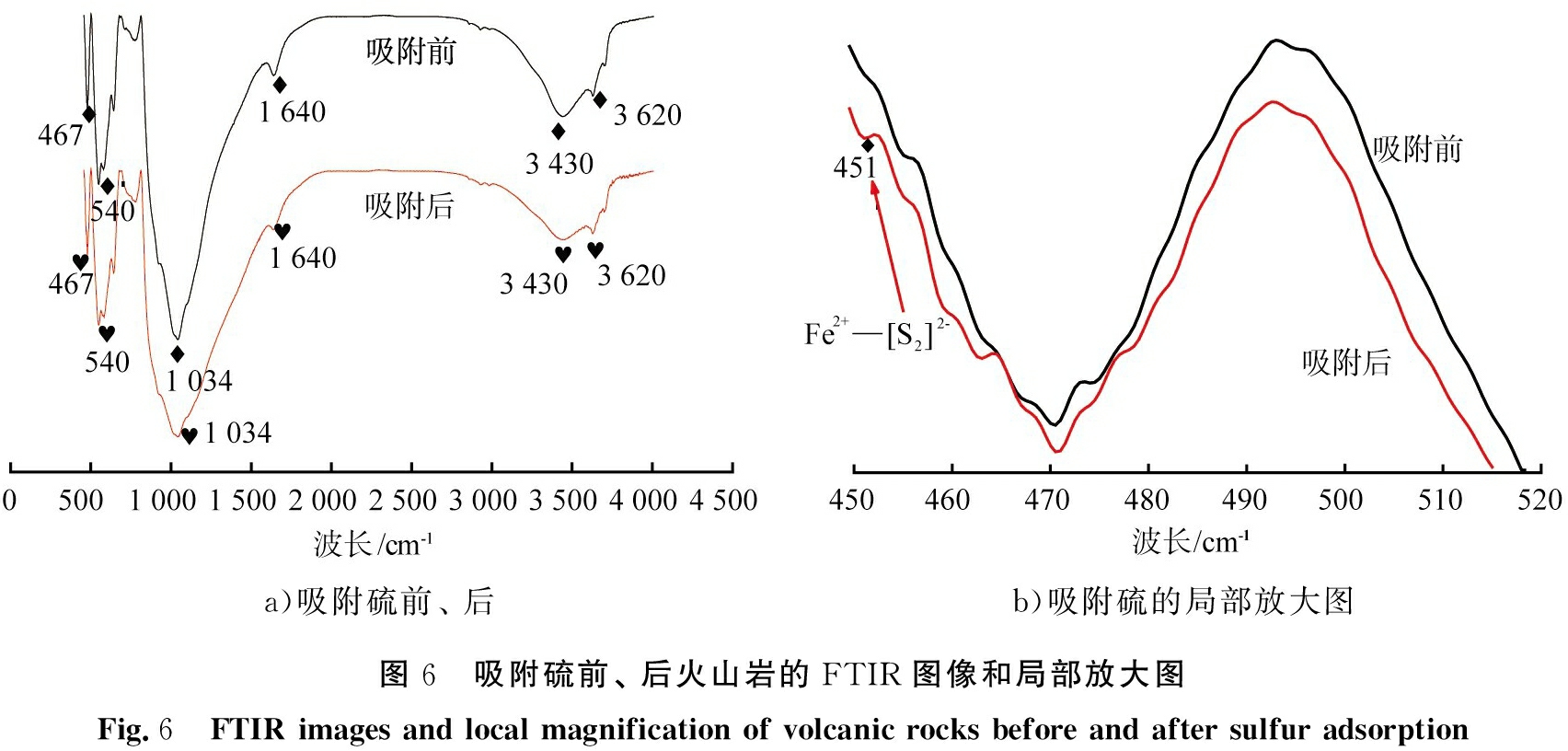
a)吸附硫前、 后b)吸附硫的局部放大图图6 吸附硫前、 后火山岩的FTIR图像和局部放大图Fig.6 FTIR images and local magnification of volcanic rocks before and after sulfur adsorption
火山岩吸附硫前、 后样品的XPS图谱如图7所示。其中图7 a)为全谱图,图7 b)为S 2p轨道图。由图7 a)可以看出,吸附后样品增加了S的特征信号峰。由图7 b)样品的S 2p高分辨谱图可知,162.9、 161.8 eV处分别代表S 2p1/2和S 2p3/2的信号峰,这与文献中所报道的FeS2中S的结合能相一致[12]。另外,由图7 b)可以看出,吸附后样品的S 2p高分辨谱图中在167.97 eV处还存在一个特征信号峰,此处的信号峰代表S—O信号峰[13]。分析其原因为含S2-废水暴露在空气中被氧化成硫酸根、亚硫酸根、硫代硫酸根等所致。可见样品在吸附硫的过程中有FeS2的生成。
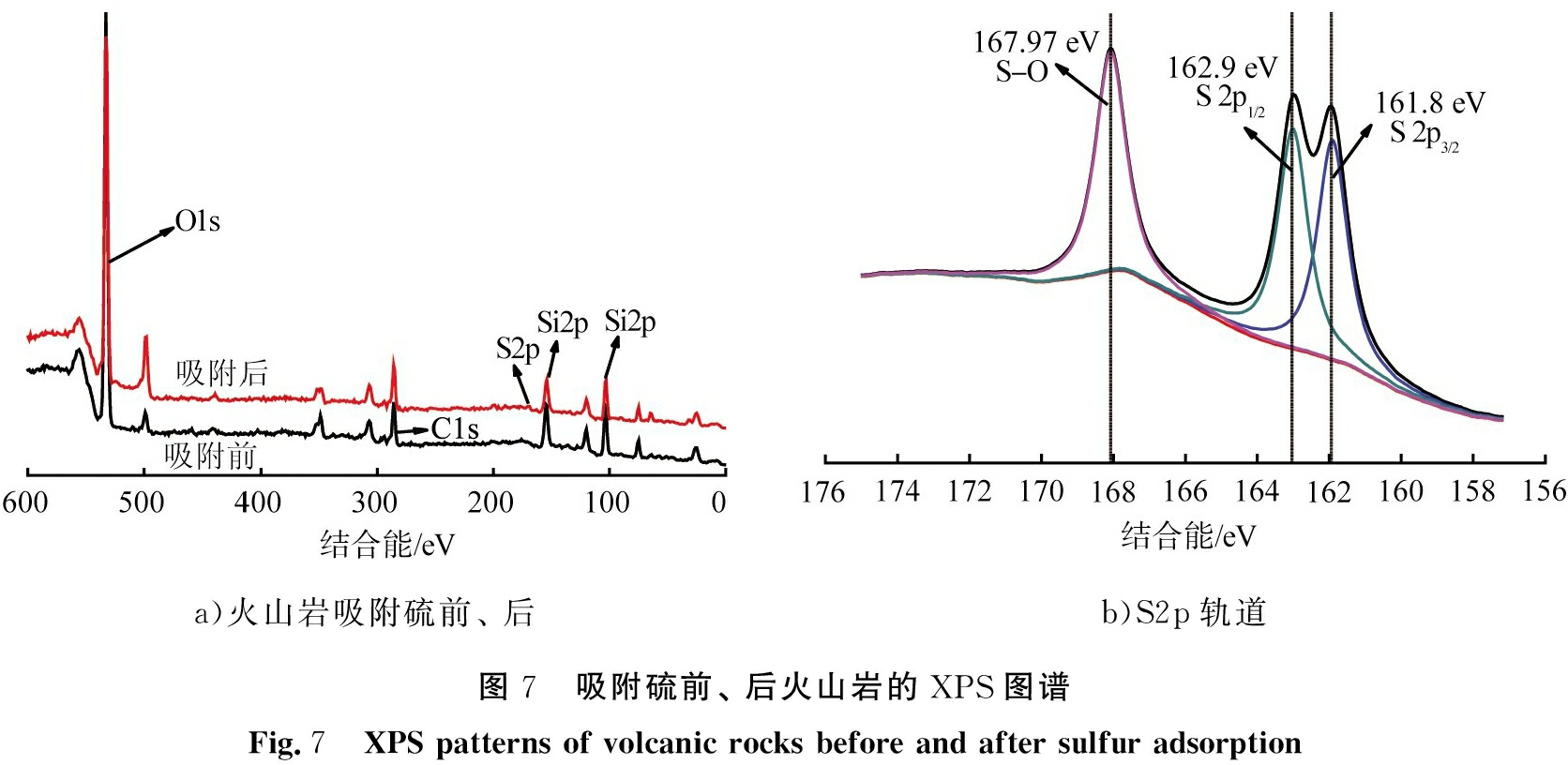
a)火山岩吸附硫前、 后b)S2p轨道图7 吸附硫前、 后火山岩的XPS图谱Fig.7 XPS patterns of volcanic rocks before and after sulfur adsorption
火山岩吸附硫化物前、 后样品的拉曼光谱图如图8所示。由图可以看出,吸附前后火山岩在287、 475 cm-1处均存在特征拉曼峰,但吸附后火山岩在475 cm-1处的拉曼峰发生宽化,在400 cm-1处的拉曼峰消失了。吸附后火山岩在339、 377以及504 cm-1处出现了新的拉曼峰,与文献报道的FeS2(黄铁矿)结构非常匹配[14]。339、 377以及504 cm-1处的拉曼峰分别归因于FeS2的S2振动、 S—S的同相拉伸以及S—S的耦合振动和拉伸。可见,火山岩在吸附硫的过程中有FeS2的生成。
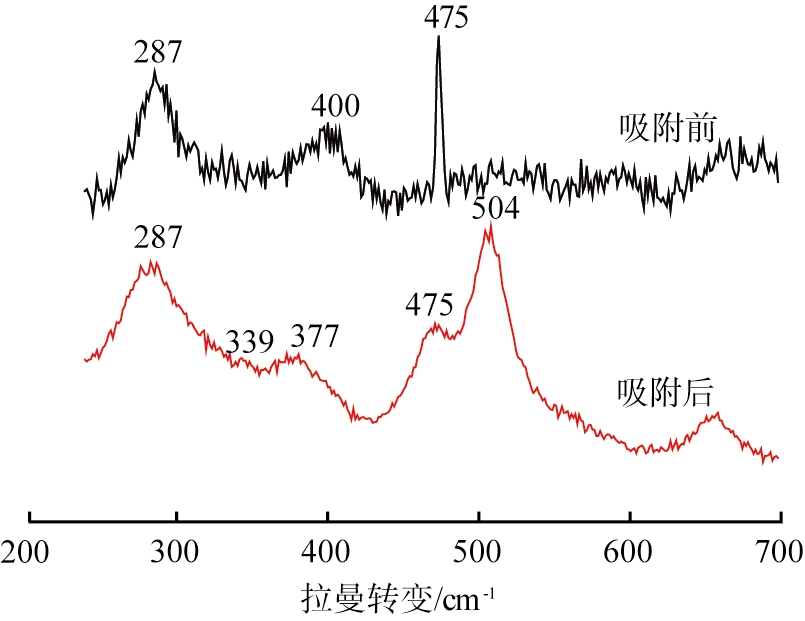
图8 吸附硫前、后火山岩的拉曼光谱图
Fig.8 Raman spectra of volcanic rocks before and after sulfur adsorption
综上所述,由吸附硫前后火山岩的XPS、 拉曼光谱以及FTIR分析,可以推断火山岩对硫化物的吸附与其含有的铁离子有关系很大,含有的铁离子在吸附硫过程中发生系列反应生成FeS2,铁离子在含硫水体中发生反应可归纳如下[15]:
2Fe3++HS-![]() 2Fe2++S+H+ ,
2Fe2++S+H+ ,
Fe2++ HS-![]() FeS+H+ ,
FeS+H+ ,
FeS+H2S![]() FeS2+H2。
FeS2+H2。
2.5 应用研究
采用复合矿物颗粒(蛭石颗粒与火山岩颗粒质量比为4∶1,粒径分别为:8~12 mm、 20~35 mm)对实际流域水体进行了现场应用研究。样品的制备:将批量复合矿物颗料(粒径为8~35 mm)进行网袋式模块化组装。流域水体水样:永宁干沟(入黄排水沟),位于宁夏银川市永宁县。装置为U型亚克力板流槽,其截面积为0.16 m2、 长为50 m,水流量为50 kg/h。通过粒料吸附过滤方式对该流域水体进行氨氮去除应用研究。该水体原水氨氮质量浓度为2.74 mg/L,属于劣Ⅴ类水质。
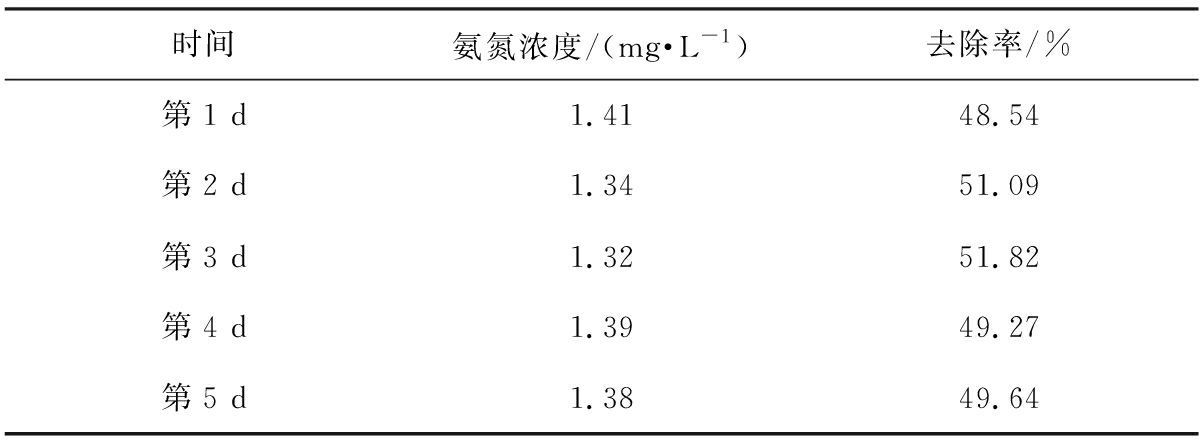
经一次吸附过滤净化后,水体氨氮浓度连续5d测试结果如表2所示。从表可以看出,复合矿物颗料对流域水体中低浓度氨氮的去除效果较显著,水体经粒料吸附过滤净化后,氨氮浓度可降低至符合地表水环境质量Ⅳ类水质标准(不超过1.5 mg/L),去除率维持在50%左右,最高时可达51.82%。
表2 水体经蛭石吸附净化后氨氮测试结果
Tab.2 Test results of ammonia nitrogen after water
purification by vermiculite adsorption
时间氨氮浓度/(mg·L-1)去除率/%第1 d1.4148.54第2 d1.3451.09第3 d1.3251.82第4 d1.3949.27第5 d1.3849.64
3 结论
1)通过对蛭石颗粒(8~12 mm)进行NaCl层间处理,制备了可吸附水体中氨氮等污染物的Na化蛭石矿物颗粒。处理前、 后蛭石样品对氨氮的吸附容量分别为21.4、 29.3 mg/g,最佳条件下对水体中氨氮的去除率分别为86.7%、 93.4%。
2)通过对火山岩颗粒(20~35 mm)进行FeCl3表面处理,制备可吸附水体中硫化污染物的矿物颗粒。处理前后火山岩颗粒对硫化物吸附容量分别为3.1、 36.9 mg/g。
3)采用2种矿物颗粒进行粒级组配制得复合矿物颗粒,当蛭石与火山岩颗粒质量比为4∶1时,去除入黄排水沟(永宁干沟)实际流域水体中氨氮,可由劣Ⅴ类水质(氨氮浓度为2.74 mg/L)降低至符合地表水环境质量Ⅳ类水质标准(氨氮浓度为1.35 mg/L)。
[1]ZHONG M F,TING S. A novel selective hybrid cation exchanger for low-concentration ammonia nitrogen removal from natural water and secondary wastewater[J]. Chemical Engineering Journal, 2015, 281: 295-302.
[2]FAN J W,WU H X,LIU R Y,et al. Non-thermal plasma combined with zeolites to remove ammonia nitrogen from wastewater[J]. Journal of Hazardous Materials, 2021, 401: 123627-123635.
[3]ZHOU Q,YIN H B,WANG A L,et al. Preparation of hollow B-SiO2@TiO2 composites and their photocatalytic performances for degradation of ammonia-nitrogen and green algae in aqueous solution[J]. Chinese Journal of Chemical Engineering, 2019, 27(10): 2535-2543.
[4]刘富龙. 氨氮浓度对硝化反应影响的研究[D]. 晋中: 太原理工大学, 2009.
[5]李丛丛. 废水中硫化物的生成、硫化物对生化系统的影响及其处理技术的研究[D]. 青岛: 青岛科技大学, 2014.
[6]LBTISSEM B, HÉDI B A, HASSEN C, et al. Hydrogen sulphide removal from the effluents of a phosphoric acid production unit by absorption into chlorinated seawater under alkaline conditions[J]. Comptesrendus-Chimie, 2016, 19(4): 517-524.
[7]陈理想, 吴平霄, 杨林, 等. 有机改性蛭石的特性及其对Hg2+吸附性能的研究[J]. 环境科学学报, 2015, 35(4): 1054-1060.
[8]BRI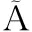 O G D V, SILVA M G C D, VIEIRA M G R A. Neodymium recovery from aqueous solution through adsorption/desorption onto expanded vermiculite[J]. Applied Clay Science, 2020, 198: 105825-105837.
O G D V, SILVA M G C D, VIEIRA M G R A. Neodymium recovery from aqueous solution through adsorption/desorption onto expanded vermiculite[J]. Applied Clay Science, 2020, 198: 105825-105837.
[9]陈理想,吴平霄, 杨林,等. 巯基乙胺改性蛭石对水体中Ag(I)的吸附性能研究[J]. 中国环境科学, 2015, 35(4): 1109-1115.
[10]MITSIS I, GODELITSAS A, GOETTLICHER J, et al. Chromium-bearing clays in altered ophiolitic rocks fromcrommyonia(Soussaki) volcanic area, Attica, Greece[J]. Applied Clay Science, 2018, 162: 362-374.
[11]XIAO S T, LU Y, FENG M, et al. Multifunctional FeS2 the ranostic nanoparticles for photothermal-enhanced chemodynamic/photodynamic cancer therapy and photoacoustic imaging[J]. Chemical Engineering Journal, 2020, 396: 125294-125307.
[12]IKKURTHI K D S S, REDDY M N K. Facile synthesis of FeS2/PVP composite as high-performance electrodes for supercapacitors[J]. Journal of Energy Storage, 2020, 28: 101216-101224.
[13]FENG D M, ZHANG X, SUN Y, et al. Surface-defective FeS2 for electrochemical NH3 production under ambient conditions[J]. Nano Materials Science, 2020, 2(2): 132-139.
[14]REHMAN U, JACOB J, MAHMOOD K, et al. Improving the thermoelectric performance of hydrothermally synthesized FeS2 nanoparticles by post sulfurization[J]. Ceramics International, 2020, 46(12): 20496-20499.
[15]MA S F, ABIGAIL N, DEREK B, et al. Removal of H2S via an iron catalytic cycle and iron sulfide precipitation in the water column ofdeadend tributaries[J]. Estuarine, Coastal and Shelf Science, 2006, 70(3): 461-472.