γ-氧化铝具有良好的机械性能、优良的化学稳定性和可控的表面酸碱性,作为催化剂[1]或催化剂载体被广泛应用于化工和石油催化工业领域[2-3]。介孔γ-Al2O3具有高比表面积、可调控的孔道结构和良好的热稳定性,可用于吸附与分离[4-5]、催化[6-7]、复合材料[8]、功能材料[9]和陶瓷[10]等领域;然而,由于存在原油质量降低、重油组分在催化剂孔道内的扩散阻力较大、重金属杂质沉积、结焦导致催化剂活性下降或失活等问题,因此需开发出具备大孔容孔径的γ-氧化铝载体材料[11-12]。
在纳米材料合成过程中,晶体成核与生长过程直接决定其尺寸分布和形貌结构,而反应器混合程度的强弱又直接影响着晶体成核与生长过程[13]。其中微反应器具有大的内比表面积、温度控制好、传热传质效率高、流体间混合强度高、转化率和收率高等优越性。微反应器为纳米材料合成提供了均匀、稳定和可控的反应环境[14]。将微反应器与传统纳米材料合成工艺相结合,可精确控制反应条件,并开发出高产率、低能耗的合成工艺[15]。
膜分散微反应器采用微孔膜作为分散介质,让分散相流体被连续相剪切成微滴进入连续相。这种方法使得两相流体间界面面积足够大,极大地提升了微观混合效率和传质性能[16-18]。Nisisako 等[19]开发出能生产单分散液滴的微通道集成芯片,该集成芯片有16~256个液滴形成单元。Pan等[20]采用膜分散微混合器对党参进行乙醇沉淀,可使半边莲素的回收率达到95%以上。Wan等[21]采用膜分散微反应器成功制备出窄孔径分布的大孔纤维状γ-氧化铝。虽然膜分散微反应器常被用于制备纳米材料,但是工业化应用的研究很少有被报道。
在不损失微反应器特性的前提下,将其尺寸放大到工业应用规模仍然是一项具有挑战性的关键技术。并联放大方法要求各个反应器的通道结构相同且反应器入口流体分布均匀,增加了工艺操作难度和能耗[22]。串联多个微反应器放大方法的优势在于流量易控和成本较低,但不能无限制地增大流量,并且通道延长后会导致流体停留时间不同,因此具有较大的局限性[23]。
而适当放大微反应器通道尺寸增大流体通量,在保证流体动力学和传输特性的同时,可大大提高防堵塞性能和生产率。Sotowa等[24]通过扩展深微通道反应器的z-维度或深度,保持质量通量不变以提高产量;Liu等[25]通过改变狭缝微通道反应器的一个维度来提高产量,但是较大的纵横比会导致流量分配不均,混合性能下降,反而使生产率降低。
本文中,参考Wan等[21]采用的膜分散微反应器,并将其微通道尺寸进行放大,探究千克级γ-氧化铝的制备工艺。研究不同操作条件对γ-氧化铝的比表面积、孔容、平均孔径和最可几孔径的影响,同时研究了干燥温度对拟薄水铝石的胶溶指数的影响。通过TEM和XRD的表征方法比较其与实验室制备的γ-氧化铝是否具有相同的性质和微观结构,对制备工艺进行优化,确定千克级放大制备工艺的最佳参数,制备出大比表面积、大孔容和平均孔径的介孔γ-氧化铝。
1 实验
1.1 试剂材料
物质的量浓度为2.85 mol/L的偏铝酸钠溶液(以Al2O3计质量浓度为150 g/L),纯度为99%的NaOH(内蒙古渤海化工有限公司),Al(OH)3(淄博福如海工贸有限公司);物质的量浓度为0.17~0.35 mol/L的硫酸铝溶液(以Al2O3计质量浓度为17~35 g/L),Al2(SO4)3(卢龙县双益磷化有限责任公司);物质的量浓度为1 mol/L的 NaOH溶液(AR,国药集团化学试剂有限公司);碳酸钠(Na2CO3,AR,天津欧博凯化工有限公司);磷酸(H3PO4,AR,天津欧博凯化工有限公司)。
1.2 表征与分析
采用D8 ADVANCE型多晶 X 射线衍射仪(Bruker,德国)对样品进行X 射线衍射(XRD)分析,实验参数为:Cu Kα射线 (λ=0.154 06 nm),40 kV的加速电压和40 mA的电流,5 (°)/min的扫描速度和10 °~80 °扫描范围。
采用 JEM-2010(JEOL,Japan)型透射电子显微镜(TEM)对样品的微观形貌与结构进行观测分析。
采用3H-2000PS2型比表面积及孔径分析仪(贝士德仪器科技有限公司,北京)测定样品的比表面积和孔参数。在77.3 K温度条件下进行氮气吸、脱附分析,测定相对压力p/p0为0.01~0.99的N2吸附-脱附等温线。由Brunauer-Emmett-Teller(BET)法计算样品的比表面积,通过相对压力p/p0为0.99时氮气的吸附量计算总孔容。由Barrett-Joyner-Halenda(BJH)法利用氮气脱附等温线数据计算孔径分布。
1.3 千克级放大工艺流程
采用偏铝酸钠和硫酸铝作为反应物的共沉淀法,通过放大膜分散微反应器制备γ-氧化铝。膜分散结构示意图如图1所示,千克级工艺放大流程图如图2所示。
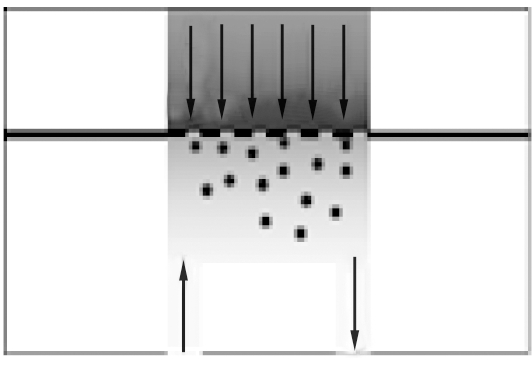
图1 膜分散结构示意图
Fig.1 Schematic diagram of membrane dispersion structure
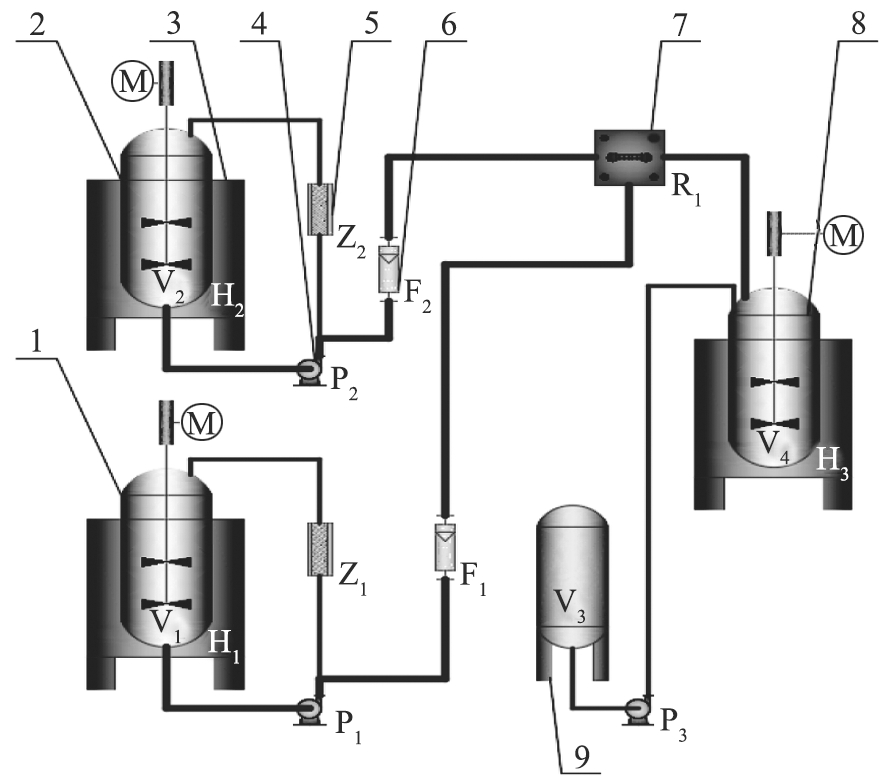
1—偏铝酸钠原料罐V1; 2—硫酸铝原料罐V2; 3—加热釜(H1,H2,H3); 4—离心泵(P1,P2,P3);5—过滤器(Z1,Z2); 6—转子流量计(F1,F2); 7—膜分散微反应器R1; 8—产物容量罐V4; 9—碱液罐V3。
图2 千克级工艺放大流程图
Fig.2 Flow chart of kilogram-scale process amplification
由图1和图2可知,所采用的膜分散微反应器反应室的半径和高度分别为8 mm,分散膜规格为15 μm。首先,开启油浴加热釜H1、H2、H3,偏铝酸钠溶液和硫酸铝溶液在带有搅拌器的原料罐V1和V2内油浴升温至60 ℃,在产物容量罐V4中添加35%(约为63 L)去离子水并油浴升温至60℃。开启进料离心泵P1、P2和原料循环回流阀门,原料通过过滤器Z1和Z2循环过滤,该方式使得工艺过程中的压强为0; 随后,开启分散相偏铝酸钠溶液的阀门调节进料流量,再开启连续相硫酸铝溶液阀门控制流量为100 L/h,反应器出口浆料流入产物容量罐V4内,通过调节流量控制产物罐内pH值稳定在8.0~8.3左右,1 h后产物罐内接料达到180 L; 浆液以一定搅拌速度老化,此时开启离心泵P3,将碱液罐V3中的氢氧化钠溶液泵入产物罐V4中,调节浆液pH值为8.8,老化完成后用65 ℃去离子水洗涤浆液至其电导率小于500 μS/cm; 经过干燥、研磨、过200 μm筛网后,600 ℃焙烧3 h得到γ-Al2O3。千克级工艺放大装置产出拟薄水铝石产量约为10 kg/h,γ-氧化铝产量约为6.8 kg/h。
2 结果与讨论
2.1 膜分散微反应器尺寸的影响
为探究不同尺寸的膜分散微反应器对制备的氧化铝性能的影响,不同尺寸的膜分散微反应器制备的氧化铝性质如表1所示。保持其他条件不变,控制反应过程pH值为8.0~8.3。
表1 不同尺寸微反应器制备的氧化铝性质
Tab.1 Properties of Al2O3 prepared with different microreactor sizes
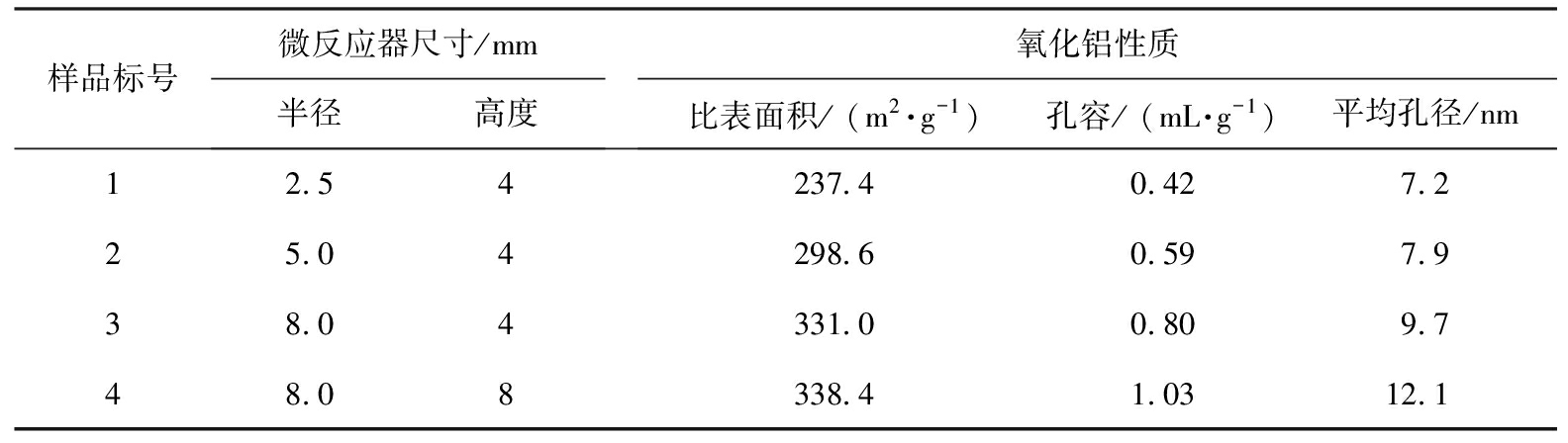
样品标号微反应器尺寸/mm半径高度氧化铝性质比表面积/ (m2·g-1)孔容/ (mL·g-1)平均孔径/nm12.54237.40.427.225.04298.60.597.938.04331.00.809.748.08338.41.0312.1
从表1可以看出,4种尺寸的膜分散微反应器所制备的氧化铝的比表面积和孔性能差别很大。随着膜分散微反应器尺寸参数的增大,氧化铝的比表面积、孔容和平均孔径都随之增大,比表面积从237.4 m2/g增大到338.4 m2/g,孔容从0.42 mL/g增加到1.03 mL/g,平均孔径从7.2 nm增大到12.1 nm。
由此,为保证制备的氧化铝具有优异的性质,同时满足大规模生产条件,确定膜分散微反应器最优半径和高度分别为8 mm。
2.2 偏铝酸钠流量的影响
在保持其他条件不变的情况下,不同偏铝酸钠流量所制备的氧化铝性质如表2所示。由表2可以看出,随偏铝酸钠流量增大,比表面积和孔容呈现下降趋势,偏铝酸钠流量为36 L/h时的孔容为最大值1.05 mL/g,因此,偏铝酸钠的最佳流量为36 L/h。
表2 不同偏铝酸钠流量下制备的氧化铝性质
Tab.2 Properties of Al2O3 prepared with different NaAlO2 flow rates
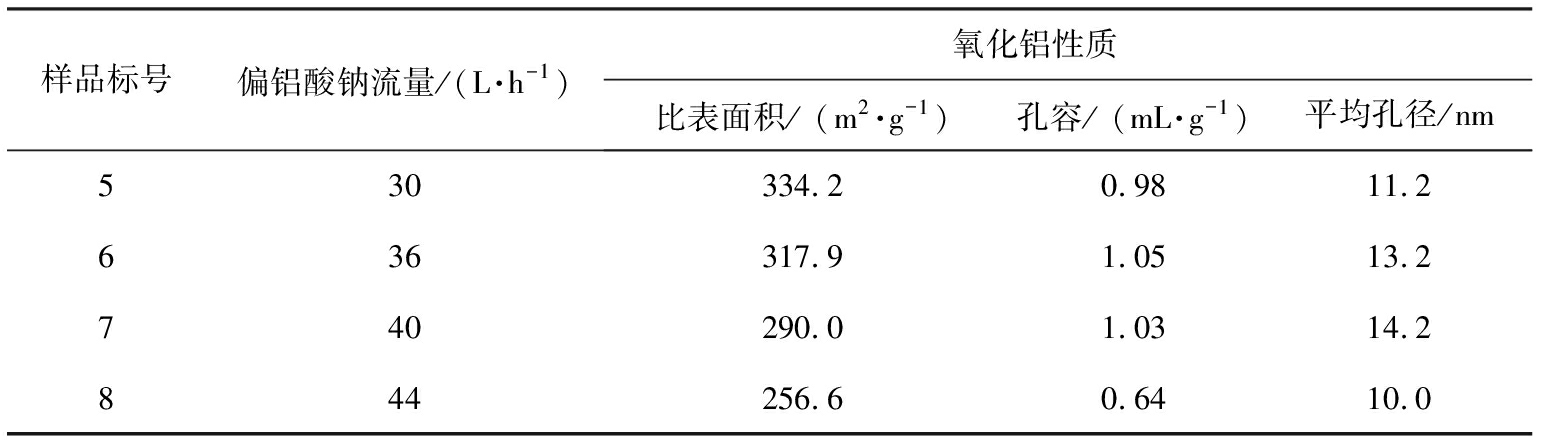
样品标号偏铝酸钠流量/(L·h-1)氧化铝性质比表面积/ (m2·g-1)孔容/ (mL·g-1)平均孔径/nm530334.20.9811.2636317.91.0513.2740290.01.0314.2844256.60.6410.0
2.3 硫酸铝质量浓度的影响
为提高反应效率和生产效率,提高偏铝酸钠溶液物质的量浓度至2.85 mol/L(以Al2O3计质量浓度为150 g/L),改变硫酸铝溶液的质量浓度,控制反应过程pH值在8.0~8.3之间,在不同硫酸铝质量浓度下考察样品的孔结构、物相组成、晶体类型和微观结构。不同质量浓度的硫酸铝制得的干燥样品XRD谱图如图3所示,出现在2θ为14.4 °、28.2 °、38.4 °、49.3 °、65.2 °附近的特征衍射峰分别对应拟薄水铝石(PDF No.74-1895)的(020)、(021)、(130)、(002)、(200)晶面,由此表明,在反应pH值在8.0~8.3之间,不同反应物质量浓度制备出的样品前驱体皆为拟薄水铝石。
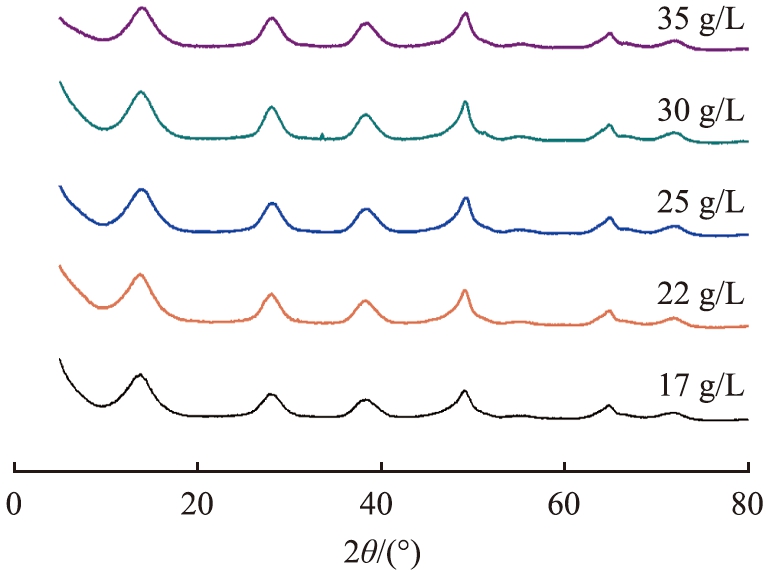
图3 不同质量浓度硫酸铝制得的氢氧化铝XRD图谱
Fig.3 XRD patterns of aluminum hydroxide prepared with different Al2(SO4)3 concentrations
不同质量浓度硫酸铝制备的γ-氧化铝性质如表3所示。
表3 不同质量浓度硫酸铝制备的γ-氧化铝性质
Tab.3 Properties of γ-Al2O3 prepared with different Al2(SO4)3 concentrations
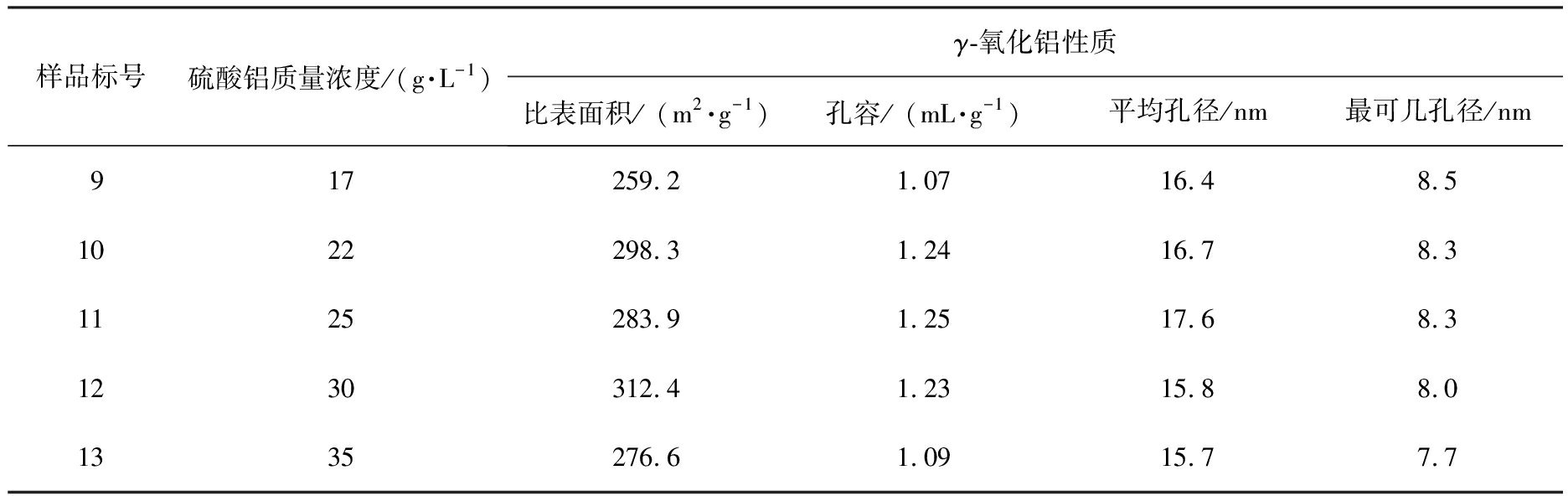
样品标号硫酸铝质量浓度/(g·L-1)γ-氧化铝性质比表面积/ (m2·g-1)孔容/ (mL·g-1)平均孔径/nm最可几孔径/nm917259.21.0716.48.51022298.31.2416.78.31125283.91.2517.68.31230312.41.2315.88.01335276.61.0915.77.7
由表3可以看出,当硫酸铝质量浓度较低时,过低的饱和度导致成核少,进一步造成较低的比表面积。当硫酸铝质量浓度增加到25 g/L时,γ-氧化铝的孔容和平均孔径达到最大值,分别为1.25 mL/g和17.6 nm。随着硫酸铝质量浓度的进一步升高,孔容和平均孔径都出现减小的趋势,γ-氧化铝的最可几孔径逐渐减小。
不同质量浓度的硫酸铝制备的γ-Al2O3的孔径分布图如图4所示。
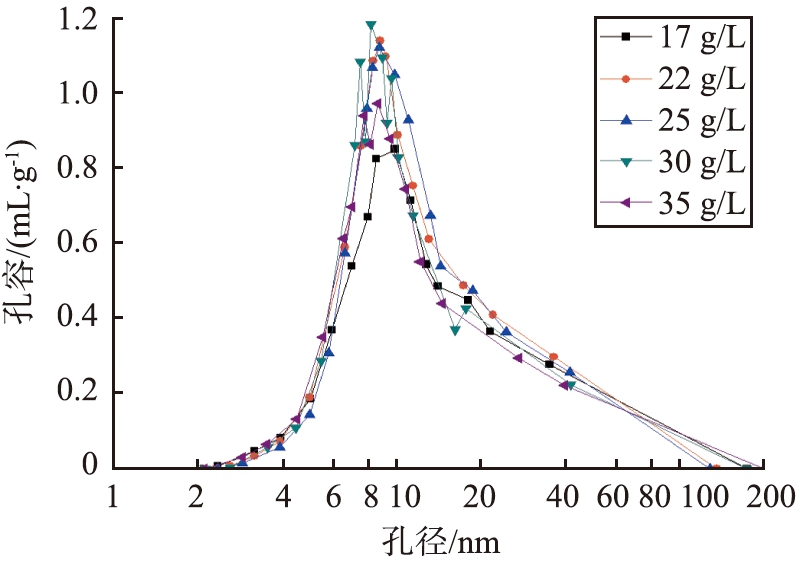
图4 不同硫酸铝质量浓度制备的γ-Al2O3的孔径分布图
Fig.4 Pore size distribution diagrams of γ-Al2O3 prepared with different Al2(SO4)3 concentrations
由图4可以看出,孔径分布范围较宽,介孔的存在提供了更多内表面积和孔体积。当硫酸铝质量浓度为30 g/L时,孔径分布峰高且较为集中,其比表面积为最大值312.4 m2/g,孔容为1.23 mL/g,平均孔径为15.8 nm。
不同硫酸铝质量浓度制备的γ-Al2O3的N2吸附-脱附等温线如图5所示。由图5可看出,吸附-脱附存在迟滞现象,等温线类型为IV型等温线,表明样品为介孔材料。在相对压力p/p0为0.7~1.0时的滞后环为H3型,其孔道是由片状结构堆叠产生的狭缝孔所致,高压区吸附量大,说明样品具有较大的总孔容。为得到较大比表面积的γ-氧化铝,研究硫酸铝质量浓度为30 g/L时其他影响因素。本文中所采用的高质量浓度偏铝酸钠溶液制得优异性质γ-氧化铝的方法此前少有报道。
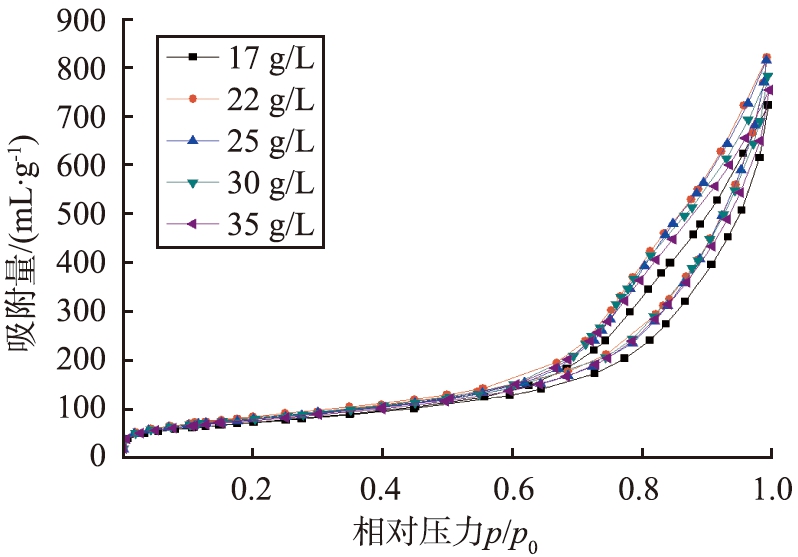
图5 不同硫酸铝质量浓度制备的γ-Al2O3的N2吸附-脱附等温线
Fig.5 N2 adsorption-desorption isotherms of γ-Al2O3 prepared with different Al2(SO4)3 concentrations
不同质量浓度硫酸铝制备的γ-氧化铝的TEM图像如图6所示。由图6可以看出,不同质量浓度下制备的γ-氧化铝均呈现纳米纤维状,纤维长度约为60 nm,直径约为4 nm; 当硫酸铝质量浓度增大到35 g/L,纳米纤维长度变短且出现团聚现象。这些纳米纤维相互交织堆叠构成不同尺寸的间隙孔,从TEM图像可见,样品γ-氧化铝结构内充满各种孔隙,也证明了大孔容γ-氧化铝的存在。

a)17 g/L

b)22 g/L

c)25 g/L
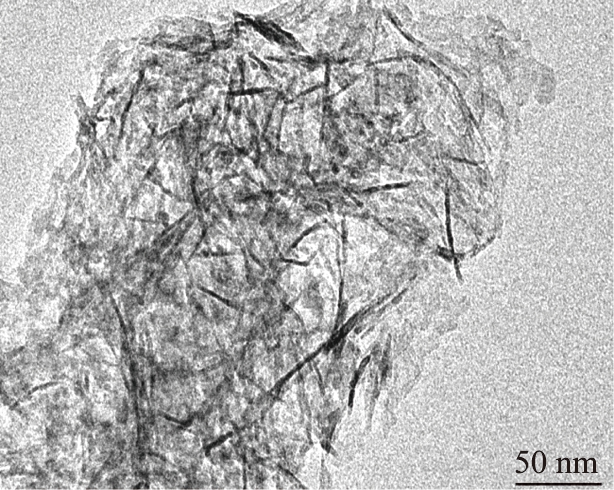
d)30 g/L
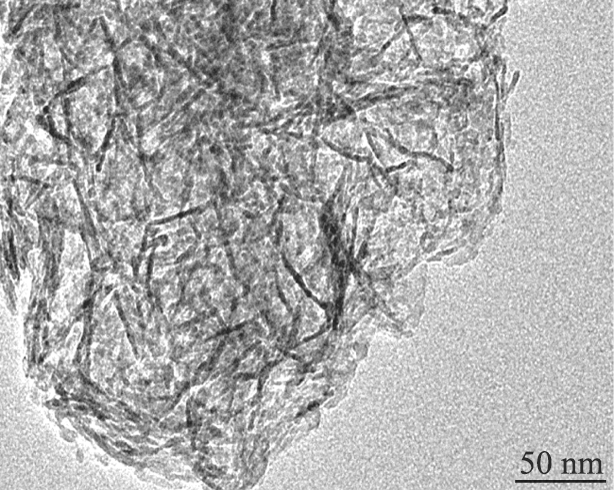
e)35 g/L
图6 不同质量浓度硫酸铝制备γ-Al2O3的TEM图像
Fig.6 TEM images of γ-Al2O3 prepared with different Al2(SO4)3 concentrations
2.4 不同反应时间的影响
采用硫酸铝质量浓度为30 g/L,保持反应过程pH值为8.0~8.3,不同反应时间时制得γ-氧化铝的性质如表4所示。随着反应时间从10 min增加到30 min,样品的比表面积、孔容和平均孔径均有所增加,当比表面积从256.5 m2/g增大到305.7 m2/g; 反应时间为20 min时,孔容和平均孔径达到最大值,分别为1.19 mL/g和17.1 nm; 当反应时间从30 min延长到60 min,比表面积和孔容均有所减小,孔容从1.15 mL/g减小到1.02 mL/g; 随着反应时间从10 min延长到60 min,γ-氧化铝固含量从15.6%增加到38.0%,反应时间为40 min后增长缓慢并趋于稳定。
表4 不同反应时间制备的γ-氧化铝的性质
Tab.4 Properties of γ-Al2O3 prepared with different reaction time
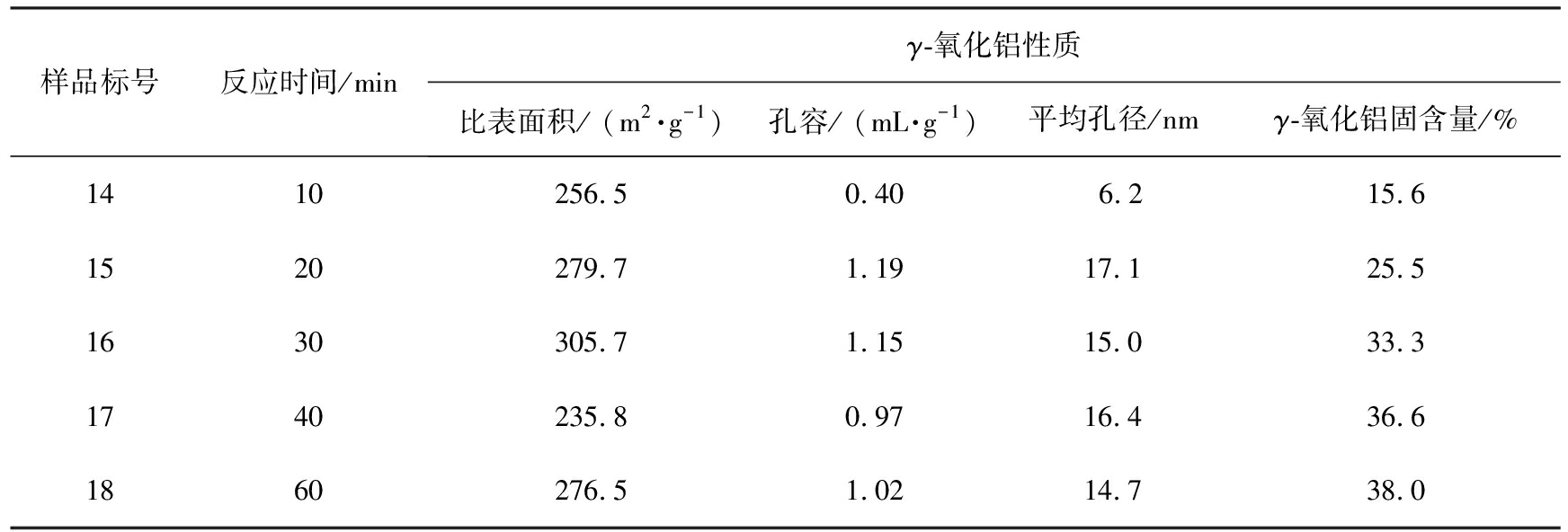
样品标号反应时间/minγ-氧化铝性质比表面积/ (m2·g-1)孔容/ (mL·g-1)平均孔径/nmγ-氧化铝固含量/%1410256.50.406.215.61520279.71.1917.125.51630305.71.1515.033.31740235.80.9716.436.61860276.51.0214.738.0
由表4可知,反应最开始时,产物浆液中饱和度低且没有充足时间让颗粒团聚物生长为纳米纤维的片状堆叠结构,因此得到γ-氧化铝的孔容和平均孔径很小;随着反应时间延长,浆液饱和度进一步提高,此时以供晶体生长的物质和能量同时得到满足,晶体沿着某一特定方向生长为纤维状结构。
不同反应时间制备的γ-氧化铝的XRD图谱如图7所示。尽管不同反应时间得到样品的孔性质不同,但XRD衍射谱图表明煅烧后的样品晶型几乎完全相同,所有氧化铝样品都在 37.7 °、45.8 °及66.8 °附近出现了特征衍射峰,这3个强衍射峰分别对应γ-Al2O3(PDF No.74-2206)的(311)、(400)和(440)晶面,说明所得氧化铝样品均为γ-氧化铝。为满足制备的γ-氧化铝的高固含量,且放大工艺的产量达到一定要求,确定反应时间为1 h。
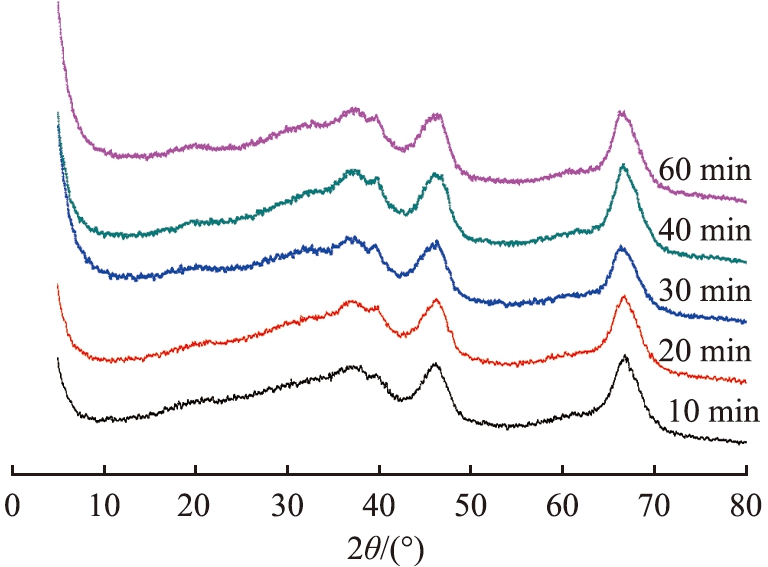
图7 不同反应时间制备的γ-Al2O3的XRD图谱
Fig.7 XRD patterns of γ-Al2O3 prepared with different reaction time
2.5 老化时间以及洗涤方式的影响
保持pH值为8.0~8.3,通过改变老化时间来探究老化时间和洗涤方式对氧化铝前驱体晶型的影响。不同的老化时间和洗涤方式制备的γ-氧化铝性质如表5所示。
表5 不同老化时间和洗涤方式制备的γ-氧化铝性质
Tab.5 Properties of γ-Al2O3 prepared with different aging time and washing methods
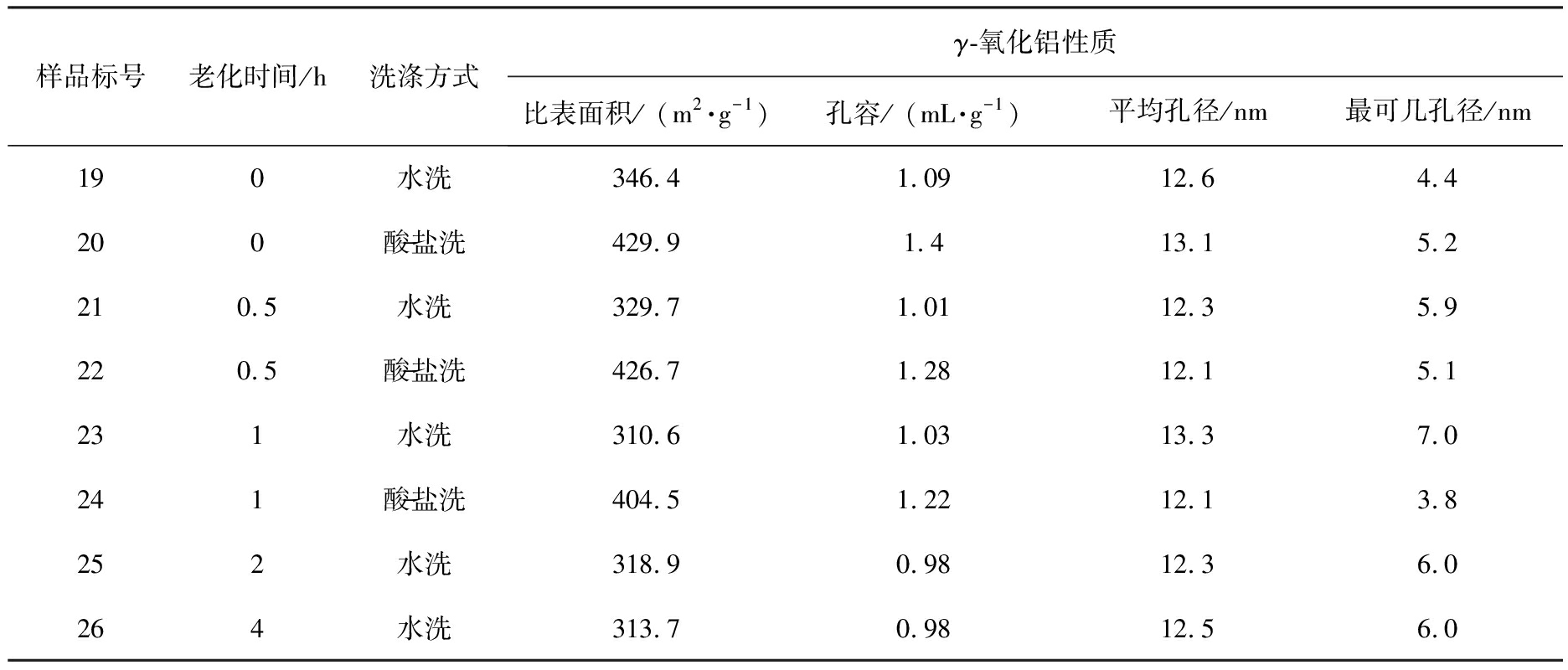
样品标号老化时间/h洗涤方式γ-氧化铝性质比表面积/ (m2·g-1)孔容/ (mL·g-1)平均孔径/nm最可几孔径/nm190水洗346.41.0912.64.4200酸-盐洗429.91.413.15.2210.5水洗329.71.0112.35.9220.5酸-盐洗426.71.2812.15.1231水洗310.61.0313.37.0241酸-盐洗404.51.2212.13.8252水洗318.90.9812.36.0264水洗313.70.9812.56.0
由表5可看出,当老化时间从初始时间增加到4 h时,γ-氧化铝的比表面积从346.4 m2/g减小到313.7 m2/g,孔容也有所减小,最可几孔径呈现先增大后减小的趋势,其中,当平均孔径和最可几孔径在老化时间为1 h时分别达到最大值13.3 nm和7 nm。
同时,在第3、4次洗涤样品时分别加入碳酸钠和磷酸溶液洗涤样品,其添加量分别为γ-氧化铝固含量的20%,通过酸-盐洗涤之后的γ-氧化铝比表面积和孔容明显增大,但是平均孔径变化不大; 随着老化时间从初始时间增加到1 h,酸-盐洗涤方式对比表面积和孔容提升效果有所减弱。
由表5可以看出,老化时间为0 h时,通过酸-盐洗涤方式制备的γ-氧化铝样品的比表面积达到最大值429.9 m2/g,孔容为1.40 mL/g,孔径为13.1 nm,这与课题组前期报导制备的氧化铝数据[21](比表面积为403.8 m2/g,孔容为1.52 mL/g,平均孔径为14.5 nm)差异不大,表明膜分散微反应器制备γ-氧化铝的放大工艺是成功的。
对上述现象的解释为,偏铝酸钠溶液和硫酸铝溶液在微反应器中发生快速的化学反应形成过饱和溶液,过饱和度不断累积,过饱和溶液中发生成核和晶体生长,溶液中的构晶离子向晶核表面扩散并且进入晶格,逐渐形成大颗粒沉淀物。沉淀最初聚集速度大于定向速度,生成的拟薄水铝石[26]呈现介稳的无定形相态,晶粒小且结晶度低,随着老化时间延长,定向速度大于聚集速度,形成沉淀微粒时有足够时间进行定向排列,通过相转移的老化过程转变为结晶度高的一水软铝石[27];老化时间为0 h时,样品母液中存在堆积松散的拟薄水铝石沉淀,拟薄水铝石是由较小的晶粒团聚成较大的颗粒聚集体,其大颗粒随着焙烧形成较小的颗粒,故此时比表面积和孔容最大;随着老化时间延长,母液中拟薄水铝石结晶度提高,其进一步转化形成一水软铝石晶体,随着焙烧导致晶体结构破坏烧结成大颗粒,形成更大孔径,所以此时制得γ-氧化铝的比表面积和孔容减小,最可几孔径增大。
不同老化时间和洗涤方式制备的γ-氧化铝的孔径分布如图8所示,SP-W表示碳酸钠-磷酸洗涤方式。由图8 a)看出,当老化时间为1 h时介孔数最多,故此时平均孔径最大;图8 b)表明了经过酸-盐洗涤之后介孔数量明显增多,孔容有了明显提升,这与表5中反映出的γ-氧化铝的孔容数据相对应。
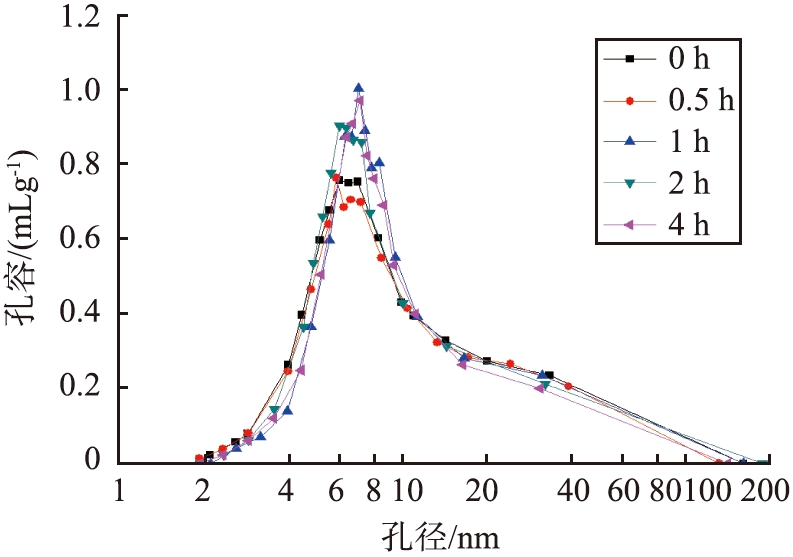
a)不同老化时间
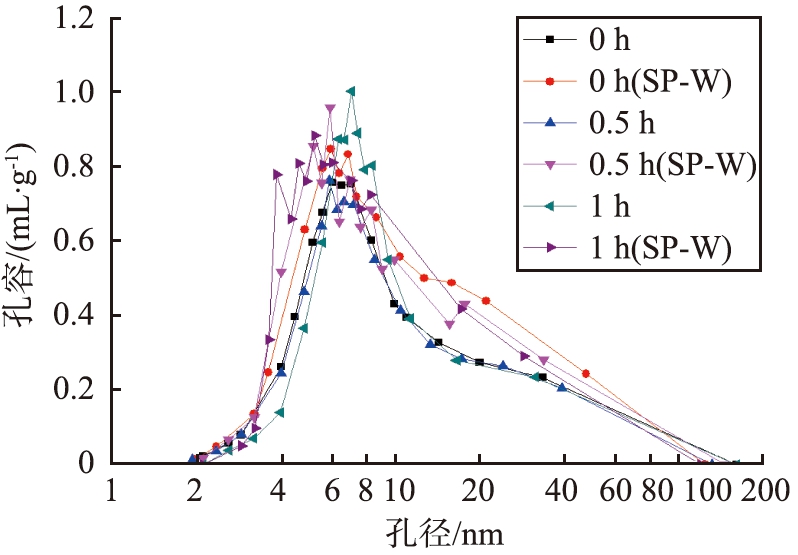
b)不同洗涤方式
图8 不同老化时间和洗涤方式制备的γ-氧化铝孔径分布图
Fig.8 Pore size distribution diagrams of γ-Al2O3 prepared by different aging time and washing methods
不同老化时间和洗涤方式制备的γ-氧化铝TEM图像如图9所示。由图9可知,虽然老化时间不同,γ-氧化铝的形貌均呈现纳米纤维状,但是纳米纤维长度和直径随着老化时间延长变短变窄。当老化时间为0 h时,纤维长度大约为70 nm,直径约为4.5 nm,老化时间2 h时,纤维长度大约为40 nm,直径约为2.5 nm。对比图9 a)—9 d)可以看出,经过酸-盐洗涤过后纤维交叠松散,这可能是导致大比表面积、大孔容的原因。因此工业制备中可选择老化时间范围为0~1 h,以碳酸钠-磷酸洗涤方式来制备大孔容γ-氧化铝。

a)老化时间0 h,水洗

b)老化时间0 h,酸-盐洗

c)老化时间0.5 h,水洗

d)老化时间0.5 h,酸-盐洗

e)老化时间1 h,水洗
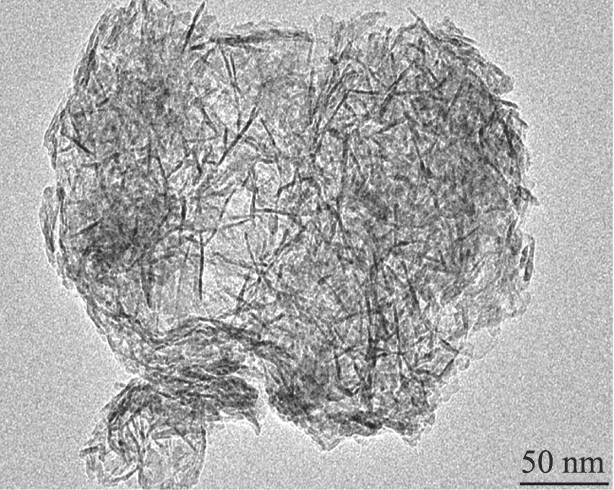
f)老化时间2 h,水洗
图9 不同老化时间和洗涤方式制备的γ-氧化铝TEM图像
Fig.9 TEM images of γ-Al2O3 prepared by different aging time and washing methods
2.6 干燥温度的影响
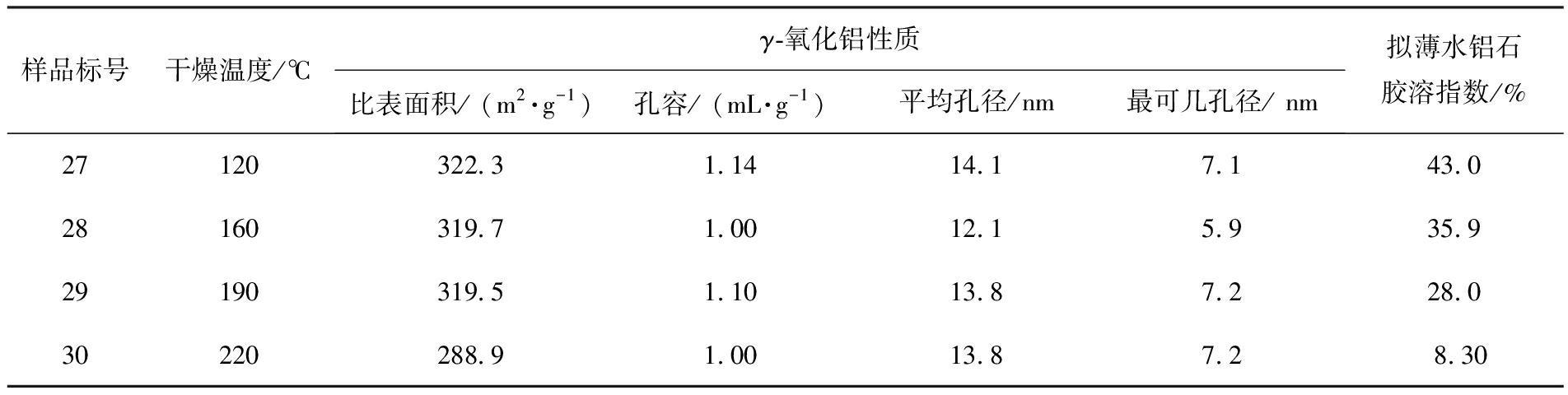
拟薄水铝石的胶溶性能与其表面铝-羟基层间水有关[28],不同干燥温度对γ-氧化铝性质和拟薄水铝石胶溶指数的影响见表6。干燥温度为120 ℃时拟薄水铝石不能完全胶溶,说明在此温度下拟薄水铝石已经开始失去表面铝-羟基层间水,使其胶溶性能变差,胶溶指数随着干燥温度升高不断减小; 当干燥温度达到220 ℃,胶溶指数从43%急剧减小到8.3%,根据产品的应用要求改变干燥温度来调节拟薄水铝石的胶溶指数。在干燥温度为120~190 ℃时,可看出干燥温度对γ-氧化铝的比表面积影响不明显,γ-氧化铝样品的比表面积基本保持不变,在120 ℃时γ-氧化铝的比表面积为322.3 m2/g、孔容为1.14 mL/g、平均孔径为14.1 nm;当干燥温度为220 ℃时比表面积明显降低为288.9 m2/g。
表6 不同干燥温度制备的γ-氧化铝性质以及拟薄水铝石的胶溶指数
Tab.6 Properties of γ-Al2O3 and peptization index of pseudo boehmite prepared with different drying temperatures
样品标号干燥温度/℃γ-氧化铝性质比表面积/ (m2·g-1)孔容/ (mL·g-1)平均孔径/nm最可几孔径/ nm拟薄水铝石胶溶指数/%27120322.31.1414.17.143.028160319.71.0012.15.935.929190319.51.1013.87.228.030220288.91.0013.87.28.30
由表6可知,随着干燥温度的升高,孔容和平均孔径有所减小,说明在干燥过程中由于表面铝-羟基层间水的脱除,较大的表面张力会使得样品颗粒逐渐聚集,使得孔道结构发生改变甚至孔结构塌陷导致孔容和孔径减小,而且干燥温度越高水分脱除速率越快,孔结构越容易被破坏[29]。选择120 ℃为干燥温度,不但能保持γ-氧化铝的性质,还能减小因干燥温度高造成的能量损失。
3 结论
以偏铝酸钠为分散相、硫酸铝为连续相,采用共沉淀方法在膜分散微反应器中进行了纤维状γ-氧化铝制备工艺的放大试验。通过放大膜分散微反应器的尺寸,成功制备出大比表面积、大孔容和平均孔径的介孔γ-氧化铝。通过TEM和XRD的表征方法表明其与实验室制备的γ-氧化铝具有相同的性质和微观结构,说明该工艺放大效应不明显,具有优良的重复性。通过探究不同条件参数对介孔γ-氧化铝的性质和微观形貌的影响,得出以下结论:
1)适当增大反应物质量浓度可以增大γ-氧化铝平均孔径和最可几孔径,合适的反应时间能达到稳定的γ-氧化铝固含量,改变老化时间和洗涤方式能够显著提升γ-氧化铝的比表面积和孔容,升高干燥温度会导致γ-氧化铝的胶溶指数减小。
2)千克级放大制备工艺的最佳参数为:膜分散微反应器的半径和高度均为8 mm,偏铝酸钠流量为36 L/h,硫酸铝的质量浓度为30 g/L,反应时间为1 h,老化时间为0~1 h,洗涤方式为碳酸钠-磷酸洗涤方式,干燥温度为120 ℃。
3)通过膜分散微反应器千克级放大制备工艺制备出的纤维状介孔γ-氧化铝的比表面积为429.9 m2/g、孔容为 1.4 mL/g、平均孔径为13.1 nm。
[1]BAI P,WU P P,YAN Z F,et al.Cation-anion double hydrolysis derived mesoporous γ-Al2O3 as an environmentally friendly and efficient aldol reaction catalyst[J].J Mater Chem,2009,19(11):1554-1563.
[2]HICKS W H,CASTAGNOLA N B,ZHANG Z R,et al.Lathlike mesostructured γ-alumina as a hydridesulfurization catalyst support[J].Applied Catalysis A,General,2003,254(2):311-317.
[3]ZHANG Z R,THOMAS J P.Mesostructured γ-Al2O3 with a lathlike framework morphology[J].Journal of the American Chemical Society,2012,124(41):12294-12301.
[4]POURSANI S A,NILCHI A,HASSANI A H,et al.A novel method for synthesis of nano-γ-Al2O3:study of adsorption behavior of chromium,nickel,cadmium and lead ions[J].International Journal of Environmental Science and Technology,2015,12(6):2003-2014.
[5]TIAN J Y,TIAN P,PANG H C,et al.Fabrication synthesis of porous Al2O3 hollow microspheres and its superior adsorption performance for organic dye[J].Microporous and Mesoporous Materiails,2016,223:27-34.
[6]POURKHALIL M,IZAD I N,RASHIDI A,et al.Synthesis of CeOx/γ-Al2O3 catalyst for the NH3-SCR of NOx[J].Materials Research Bulletin,2017,97:1-5.
[7]PAN,ZHANG W Q,ZHENG G S,et al.Degradation of p-nitrophenol using CuO/Al2O3 as a Fenton-like catalyst under microwave irradiation[J].Rsc Advances,2015,5(34):27043-27051.
[8]TISHKEVICH D I,VOROBJOVA A I,SHIMANOVICH D L,et al.Formation and corrosion properties of Ni-based composite material in the anodic alumina porous matrix[J].J Alloys Compd,2019,804:139-146.
[9]ZHEIVOT V I,PARKHOMCHUK E V,SASHKINA K A,et al.Silica and alumina based functional materials:substructures,adsorption and gas chromatographic properties[J].Microporous and Mesoporous Materials,2015,202:57-67.
[10]ZANG W J,GUO F,LIU J C,et al.Lightweight alumina based fibrous ceramics with different high temperature binder[J].Ceramics International,2016,42(8):10310-10316.
[11]BOKHIMI X,TOLEDO-ANTONIO A J,GUZM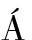 N-CASTILLO M L,et al.Relationship between crystallite size and bond lengths in boehmite[J].J Solid State Chem,2001,159(1):32-40.
N-CASTILLO M L,et al.Relationship between crystallite size and bond lengths in boehmite[J].J Solid State Chem,2001,159(1):32-40.
[12]BOKHIMI X,S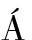 NCHEZ-VALENTE J,PEDRAZA F.Crystallization of sol-gel boehmite via hydrothermal annealing[J].J Solid State Chem,2002,166(1):182-190.
NCHEZ-VALENTE J,PEDRAZA F.Crystallization of sol-gel boehmite via hydrothermal annealing[J].J Solid State Chem,2002,166(1):182-190.
[13]BA DYGA J,POHORECKI R.Turbulent micromixing in chemical reactors:a review[J].The Chemical Engineering Journal and The Biochemical Engineering Journal,1995,58(2):183-195.
[14]GONG X Q,WANG Y W,IHLI J,et al.The crystal hotel:a microfluidic approach to biomimetic crystallization[J].Advanced Materials,2015,27(45):7395-7400.
[15]ABOU-HASSAN A,NEVEN S,DUPUIS V,et al.Synthesis of cobalt ferrite nanoparticles in continuous-flow microreac-tors[J].Rsc Advances,2012,2(30):11263-11266.
[16]JIA Z Q,LIU Z Z.Membrane-dispersion reactor in homogeneous liquid process[J].Journal of Chemical Technology and Biotechnology,2013,88(2):163-168.
[17]GÜNTHER A,JENSEN K F.Multiphase microfluidics:from flow characteristics to chemical and materials synthesis[J].Lab on A Chip,2006,6(12):1487-1503.
[18]DU L,TAN J,WANG K,et al.Controllable preparation of SiO2 nanoparticles using a microfiltration membrane dispersion microreactor[J].Industrial and Engineering Chemistry Research,2011,50(14):8536-8541.
[19]NISISAKO T,TORII T.Microfluidic large-scale integration on a chip for mass production of monodisperse droplets and particles[J].Lab on a Chip,2008,8(2):287-293.
[20]PAN J J,SHAO J Y,QU H B,et al.Ethanol precipitation of codonopsis radix concentrate with a membrane dispersion micromixer[J].J Clean Prod,2020,251.
[21]WAN Y C,LIU Y B,WANG Y J,et al.Preparation of large-pore-volume γ-alumina nanofibers with a narrow pore size distribution in a membrane dispersion microreactor[J].Industrial &Engineering Chemistry Research,2017,56(31):8888-8894.
[22]Al-RAWASHDEH M,ZALUCKU J,MÜLLER C,et al.Phenylacetylene hydrogenation over[Rh(NBD)(PPh3)2]BF4 catalyst in a numbered-up microchannels reactor[J].Industrial and Engineering Chemistry Research,2013,52:11516-11526.
[23]ZHANG J S,WANG K,TEIXEIRA A R,et al.Design and scaling up of microchemical systems:a review[J].Annual Review of Chemical and Biomolecular Engineering,2017,8:285-305.
[24]SOTOWA K-I,SUGITAMA S,NAKAGAWA K,et al.Flow uniformity in deep microchannel reactor under high throughput conditions[J].Organic Process Research and Development,2009,13(5):1026-1031.
[25]LIU G T,WANG K,LU Y C,et al.Liquid-liquid microflows and mass transfer performance in slit-like microchan-nels[J].Chemical Engineering Journal,2014,258:34-42.
[26]徐登清.大孔拟薄水铝石制备及加氢脱氧的研究[D].曲阜:曲阜师范大学,2011.
[27]MULLIN J W.Crystallization[M].4th ed.Massachusetts:Reed Educational and Professional Publishing Ltd,2001:536-575.
[28]苗壮,史建公,郝建薇,等.拟薄水铝石的胶溶性与结构的关系[J].石油学报(石油加工),2016,32(3):493-500.
[29]尹衍升,张景德.氧化铝陶瓷及其复合材料[M].北京:化学工业出版社,2001:69-85.