水滑石(hydrotalcite,HT)又称为层状双氢氧化物,是一类具有层状结构的阴离子黏土,与类水滑石、插层水滑石统称为水滑石类材料(layered double hydroxides,LDHs)[1]。
LDHs的组成通式为![]() 其中An-表示
其中An-表示![]() 等层间阴离子[2],Mg2+、Al3+可被Ca2+、Cu2+或Cr3+、Fe3+等半径与其相似的二价或三价阳离子同晶替代,从而形成大量的不同元素组成的LDHs材料[3]。
等层间阴离子[2],Mg2+、Al3+可被Ca2+、Cu2+或Cr3+、Fe3+等半径与其相似的二价或三价阳离子同晶替代,从而形成大量的不同元素组成的LDHs材料[3]。
LDHs的典型结构如图1所示。以M代表Mg2+、Zn2+、Ni2+、Al3+、Fe3+等金属阳离子,LDHs结构层是由以M2+—OH或M3+—OH八面体结构形成的正电荷层板、层间阴离子及水分子组成的。
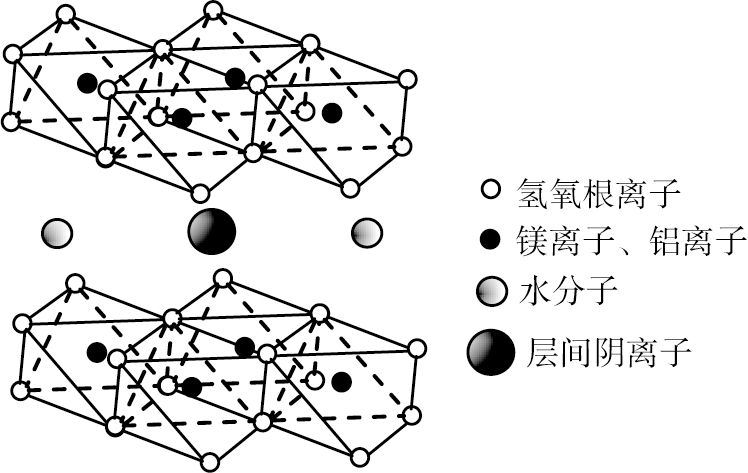
图1 LDHs典型结构
Fig.1 Typical structure of LDHs
LDHs种类繁多,具有层间距大、化学组成丰富、离子交换能力强[4-5]、生物相容性和化学稳定性良好[4,6]等特性,其阴离子交换量与阴离子交换树脂相当[6-7],因此,被广泛应用于催化、吸附、医药、阻燃、离子交换等领域[5,7]。
由于LDHs为片状结构,其表面和活性位点的暴露程度比较低[8],在水处理领域中,仅用LDHs单一材料难以达到较好的处理效果[9]。因此,需要对LDHs进行改性处理,提高改性LDHs对废水中重金属和有机污染物等的吸附能力。本文中综述了改性LDHs的制备方法及其在废水处理中的应用进展。
1 改性LDHs的制备与性质
LDHs的制备和改性方法主要有共沉淀法、水热法、离子交换法、焙烧复原法、尿素法、溶剂热法等[10-12]。
1.1 共沉淀法
共沉淀法是最为典型的LDHs制备方法。共沉淀法是在一定温度条件下,将含有一定比例金属阳离子的混合溶液加入到碱性溶液中,控制反应过程中溶液的pH达到目标值,搅拌溶液至发生共沉淀现象后,将产物继续老化一定时间,最后过滤、清洗和干燥后得到LDHs[8]。金属阳离子的种类和比例、混合溶液目标pH、碱性溶液的性质和浓度等均影响LDHs的生成[13],通过改变这些条件可以实现对LDHs的改性处理。
闫良国课题组通过改变金属盐的种类、碱溶液的组成以及加入Fe3O4、生物炭等基体,采用共沉淀法制备了系列LDHs及其复合材料[14-24]。LDHs及其复合材料制备的基本流程为:将M(NO3)2(M=Mg2+或Zn2+)与Al(NO3)3溶液以及NaOH、Na2CO3混合溶液逐滴加入到装有60 ℃蒸馏水的烧杯中,控制滴加速度以保证混合溶液的pH值达到10左右,搅拌12 h,待反应完全后,继续静置晶化6 h即可得到MAl-LDHs。X射线衍射(XRD)、红外光谱(FTIR)、扫描电镜(SEM)等表征结果表明该方法制备的LDHs晶型良好,为典型的六边形层状结构[14,16-18]。若在碱溶液中溶解EDTA、L-半胱氨酸等插层剂,再按照上述步骤操作则可制得插层LDHs,不仅保留了LDHs的晶体结构,还带入了插层剂的氨基等官能团,更有利于提高插层LDHs去除水中污染物的能力[22-24]。而以Fe3O4为基质,采用共沉淀法合成具有磁性的核壳结构的Fe3O4@MAl-LDHs(M=Mg2+、Zn2+、Ni2+),在保持LDHs晶体结构和性质的基础上,还具备了超顺磁性,使得材料在使用完成后能够快速地固液分离,有利于材料的回收[15-17,19]。
夏燕等[25]以阴离子表面活性剂十二烷基硫酸钠(SDS)为改性剂,采用共沉淀法制备了有机改性的LDH-DS。XRD表征显示样品底面间距显著增大,FTIR图谱结果表明十二烷基硫酸根已部分取代![]() 成功进入层间。
成功进入层间。
陈航等[26]利用共沉淀法合成苯甲酸根插层镁铝水滑石(MgAl-B-LDH),并在800 ℃温度下对其进行焙烧得到样品MgAl-LDO。对比焙烧前、后样品的结构,透射电子显微镜图像可以看出:MgAl-B-LDH具有良好的结晶度和有序的层状结构;MgAl-LDO晶粒出现中间宽、两头尖的孔状结构,孔径均匀分布,比表面积显著增大。
衷水平等[27]采用共沉淀法将乙二胺四乙酸根插入MgAl-LDH层间,使插层LDHs能够迅速、有效地吸附Cu2+。
Hassani等[28]采用稀碱液共沉淀法合成了具有花状纳米结构的NiAl-LDH,与常规共沉淀法合成的LDH相比,比表面积显著增大,孔隙体积达到0.562 cm3/g,在去除甲基橙染料(MO)时具有更好的吸附效果。
1.2 水热及溶剂热法
水热及溶剂热法能够控制产品晶形,一般无需高温烧结。通常在60~200 ℃的温度条件下加热高压釜,混合物在水热条件下维持的时间从数小时到数天不等。高温水热处理使得LDHs微晶形状规则地生长,通过控制反应温度和反应时间可以实现不同形态和尺寸的LDHs的可控制备[10]。
衡惠敏等[29]以Mg(NO3)2、Al(NO3)3和氨水为原料,采用水热法合成纳米级MgAl-LDH,并通过正交试验研讨了诸因素对合成材料粒径尺寸及分布的影响,发现在原料浓度为0.03 mol/L、成核反应时间为35 min、水热反应温度为80 ℃、反应时间为17 h的条件下制得的纳米级LDH为晶型完整且单一的Mg2Al-NO3-LDH。
Zhao等[30]通过水热法合成了MgAl-LDH-石墨烯纳米复合材料。经过水热反应,去除了大部分羟基、羧基等含氧基,复合材料内的层间距缩小,所获得的杂化纳米结构材料具有优异的阻燃、导电和导热性质,可以用作阻燃剂或电、热的导体。
溶剂热法是以水热法为前驱体发展起来的方法,与水热法的不同之处在于其使用的溶剂并非水而是有机物或其它非水溶媒。
闫良国课题组采用溶剂热法在制备Fe3O4的过程中加入LDH或LDH-氧化石墨烯合成了具有磁性的LDH复合材料,用于吸附水溶液中的污染物[31-33]。
磁性氧化石墨烯-LDH纳米复合材料(MGL)制备过程示意图如图2所示。由图2可知,采用一步溶剂热法制备MGL的具体步骤为:首先将2 g FeCl3·6H2O和6 g NaAc·3H2O溶于10 mL乙二胺与20 mL乙二醇的有机溶剂中做备用,再将0.8 g MgAl-LDH和0.05 g GO分别采用超声法溶解于15 mL乙二醇中,最后将其溶于先前制备好的有机溶剂中,混合均匀后转移至100 mL反应釜中,在200 ℃下反应8 h,将得到的黑色固体洗涤、烘干、研磨、过筛。利用XRD、FTIR、BET、SEM、TEM、EDS、XPS、VSM进行一系列表征后发现,制备的MGL不仅具有较强的磁性,而且有完整的晶型结构和粗糙的表面,比表面积达到78.07 m2/g[31]。
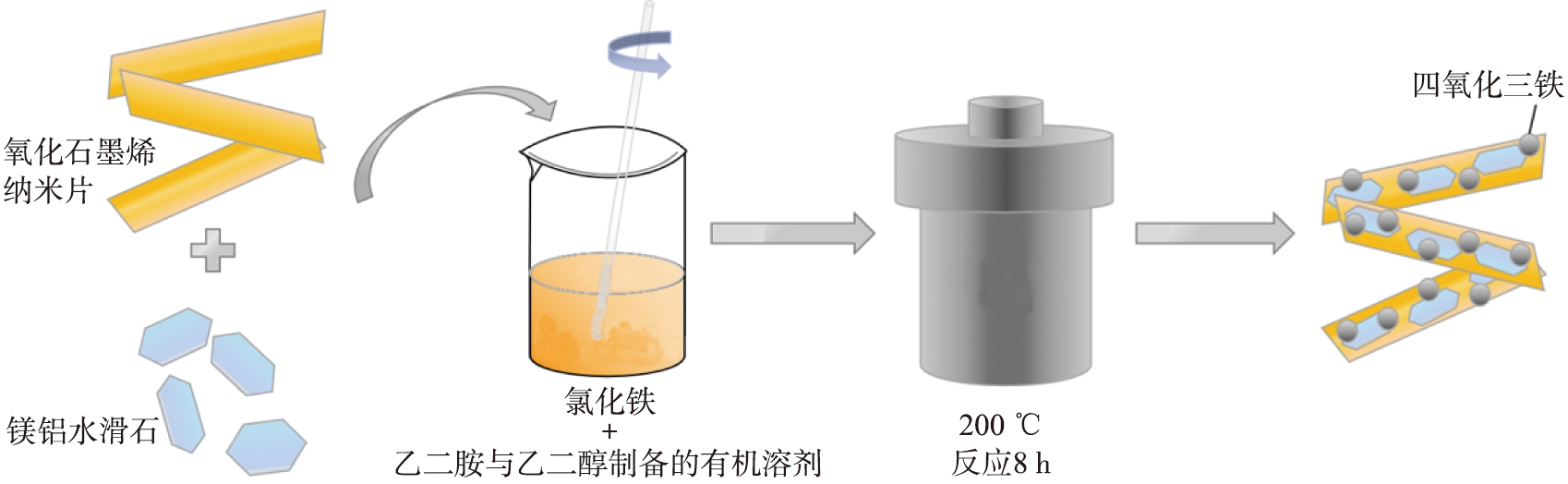
图2 MGL制备过程示意图
Fig.2 Schematic diagram of MGL preparation process
制备复合材料时用其他材料的优势弥补LDHs自身的缺陷,实现互补的同时也使得LDHs的优势被发挥出来。例如,坡缕石的比表面积大,有适度的阳离子交换能力,且其表面具有许多反应性羟基,已被证实是良好的吸附剂或吸附剂载体。Yang等[34]结合坡缕石和MgAl-LDH的优势,采用原位水热结晶法合成MgAl-LDH改性坡缕石高效黏土吸附剂,对Pb2+、Cu2+、Ni2+ 3种金属阳离子的吸附能力均高于单一坡缕石和MgAl-LDH。Zou等[35]采用一步水热法制备了具有良好化学稳定性的类水滑石复合材料g-C3N4@NiMgAl-LDH,g-C3N4与LDH中丰富的金属-氧配位结构结合,使得LDH具有良好的吸附能力和稳定的理化性质。
1.3 离子交换法
LDHs最主要的特征之一,是可以通过在层间中容纳不同的阴离子来调整其性能,因而可采用离子交换法制备具有不同层间阴离子的LDHs。离子交换法反应时间短,在对层间阴离子的数量和种类进行组装的同时保持LDHs原有的层状结构
Wei等[36]通过离子交换法对结晶良好的L-半胱氨酸插层MgAl-LDH的结构进行研究,发现具有不同层间距(1.03、1.44 nm)的一价或二价L-半胱氨酸阴离子插入到了LDH层间,这归因于它们在精确控制反应条件下在层间空间中表现出了不同取向。González等[37]先采用共沉淀法合成以Cl-作层间阴离子的MgAl-LDH-Cl,而后加入腐植酸(HA),通过离子交换合成LDH-HA吸附剂,其表现出对Cu2+、Pb2+、Cd2+良好的去除性能。
苏继新等[38]以采用共沉淀法合成的层间阴离子为![]() 的MgAl-LDH为主体,以十二烷基磺酸钠(SDS)为客体制备了复合LDH,再分别用一步改性法、离子交换法和焙烧复原法对其进行改性,根据XRD及FTIR图谱可可以确定DS-部分取代了
的MgAl-LDH为主体,以十二烷基磺酸钠(SDS)为客体制备了复合LDH,再分别用一步改性法、离子交换法和焙烧复原法对其进行改性,根据XRD及FTIR图谱可可以确定DS-部分取代了![]() 进入层间,且DS-均为单层垂直排列。
进入层间,且DS-均为单层垂直排列。
李燕等[39]用离子交换法成功制备了十二烷基苯磺酸根(DBS-)和柠檬根(Cit3-)复合改性LDHs,样品的XRD图谱基本一致,说明LDHs的晶体结构没有发生改变,Cit-LDHs和DBS-LDHs的层间距均有所增加,表明Cit3-和DBS-分别取代了![]()
1.4 焙烧复原法
焙烧复原法又称煅烧重建法,可消除与有机阴离子竞争插层的金属盐无机阴离子,利用“记忆效应”实现LDHs重复利用。在300~500 ℃条件下煅烧后,LDHs转化为层状双金属氧化物(LDO),当其与水或含有适当阴离子的溶液接触时,能够重构层状结构,重新形成LDHs[28]。焙烧过程通常分为脱水、脱羟基化、阴离子分解和氧化物重整4个过程[10]。Yao等[40]经焙烧复原法成功制备了甘油改性纳米MgAl-LDO,能够有效去除水溶液中的MO染料。
磁性LDHs可高效吸附水中的腐殖酸类物质,为充分利用这一废弃物吸附剂,Hou等[41]采用煅烧重建法得到磁性纳米复合材料Mag-LDO/C,对水中Cd2+、Pb2+、Cu2+的最大吸附量分别达到386.1、359.7、192.7 mg/g,实际水样中重金属的去除实验也表明了该材料具有很好的吸附能力和重复利用性。马明海等[42]采用焙烧法对LDHs做改性处理,能较好去除渗滤液中的氮、磷,极大减少了当地河流中氮、磷营养盐的输入,且此法能够显著提高吸附剂的使用率,减少二次污染。
2 改性LDHs的应用进展
2.1 吸附去除重金属离子
在冶金、采矿、核能等行业领域中,有毒重金属离子释放到自然环境中会对人类及其他物种造成极大危害。改性LDHs吸附重金属离子的机制主要有沉淀反应、络合作用、同晶置换、静电作用等,可被用来去除工业废水中的重金属离子,如Zn2+、Cu2+、Pb2+、Cd2+、Ni2+等。LDHs吸附去除重金属离子情况如表1所示。
表1 LDHs吸附去除重金属离子情况
Tab.1 Adsorptive removal of heavy metal ions by LDHs
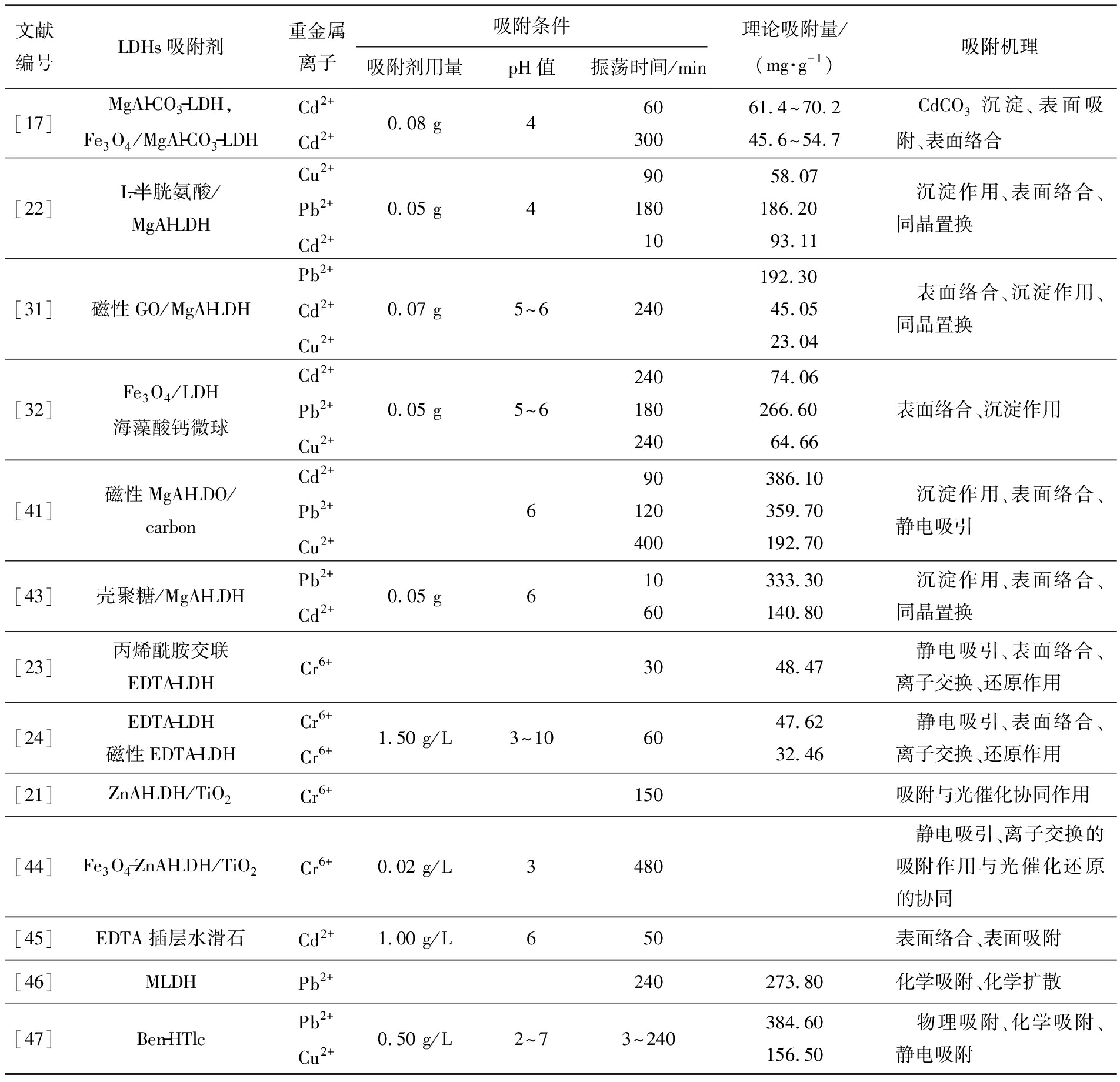
文献编号LDHs吸附剂重金属离子吸附条件吸附剂用量pH值振荡时间/min理论吸附量/(mg·g-1)吸附机理[17]MgAl-CO3-LDH,Fe3O4/MgAl-CO3-LDHCd2+Cd2+0.08 g46030061.4^70.245.6^54.7 CdCO3沉淀、表面吸附、表面络合[22]L-半胱氨酸/MgAl-LDHCu2+Pb2+Cd2+0.05 g4901801058.07186.20 93.11 沉淀作用、表面络合、同晶置换[31]磁性GO/MgAl-LDHPb2+Cd2+Cu2+0.07 g5^6240192.30 45.0523.04 表面络合、沉淀作用、同晶置换[32]Fe3O4/LDH海藻酸钙微球Cd2+Pb2+Cu2+0.05 g5^624018024074.06266.60 64.66表面络合、沉淀作用[41]磁性MgAl-LDO/carbonCd2+Pb2+Cu2+690120400386.10359.70192.70 沉淀作用、表面络合、静电吸引[43]壳聚糖/MgAl-LDHPb2+Cd2+0.05 g61060333.30140.80 沉淀作用、表面络合、同晶置换[23]丙烯酰胺交联EDTA-LDHCr6+3048.47 静电吸引、表面络合、离子交换、还原作用[24]EDTA-LDH磁性EDTA-LDHCr6+Cr6+1.50 g/L3^106047.6232.46 静电吸引、表面络合、离子交换、还原作用[21]ZnAl-LDH/TiO2Cr6+150吸附与光催化协同作用[44]Fe3O4-ZnAl-LDH/TiO2Cr6+0.02 g/L3480 静电吸引、离子交换的吸附作用与光催化还原的协同[45]EDTA插层水滑石Cd2+1.00 g/L650表面络合、表面吸附[46]MLDHPb2+240273.80化学吸附、化学扩散[47]Ben-HTlcPb2+Cu2+0.50 g/L2^73^240384.60156.50 物理吸附、化学吸附、静电吸附
由表1可知,闫良国课题组[17,21-24,31-32,41,43-44]将制备的系列LDHs功能材料用于去除水中的Cd2+、Pb2+、Cu2+和Cr6+。将磁性MgAl-LDH吸附腐殖酸后进行高温煅烧得到磁性Mag-LDO/C复合材料,该材料对Cd2+、Pb2+、Cu2+的吸附量分别达到386.1、359.7、192.7 mg/g[41]。通过优化吸附剂用量、振荡时间、溶液pH影响等实验条件,并研究系列LDHs吸附重金属的动力学、等温线和回收利用性能,综合运用谱学表征和溶液化学手段详细研究了吸附重金属离子的作用机理。
XRD、FTIR、XPS、zeta电位等表征结果表明:LDHs对于在水溶液中以阳离子存在的二价重金属的吸附功能主要通过形成表面沉淀、与官能团的络合、层板元素的同晶置换以及与表面电荷的静电作用等方式进行[17,22,31-32,41,43]。LDHs吸附重金属离子的机理示意图如图3所示。
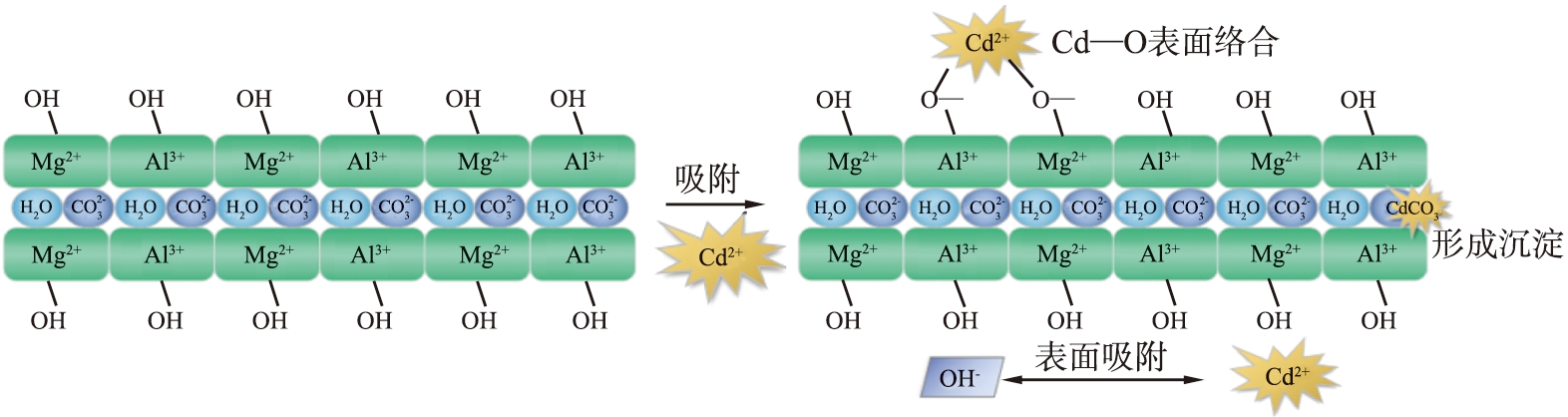
a)MgAl-LDH吸附Cd2+
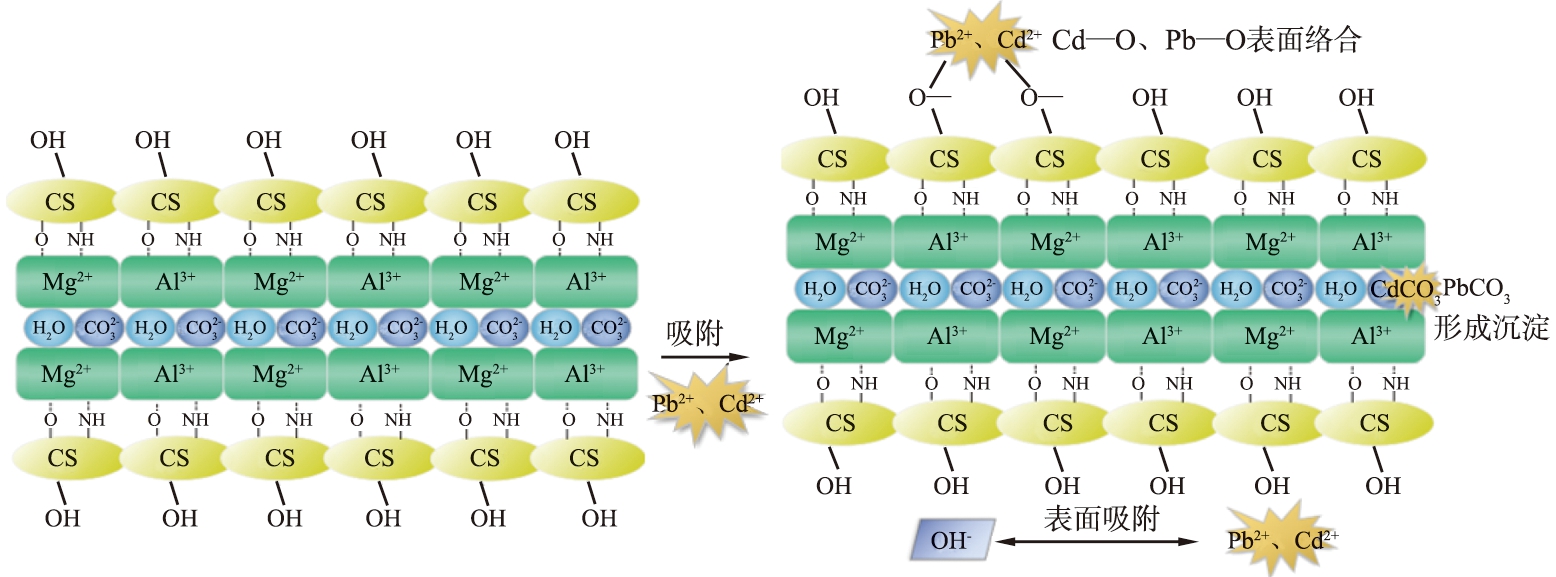
b)壳聚糖改性MgAl-LDH吸附Cd2+、Pb2+
图3 LDHs吸附重金属离子机理示意图
Fig.3 Schematic diagram of mechanism of heavy metal ions adsorption by LDHs
对于在水中以阴离子存在的铬酸盐存在阴离子的交换作用和吸附-还原耦合机制,后者是指LDHs的给电子基团将吸附的Cr6+还原为Cr3+,Cr3+再通过络合作用和同晶置换作用被LDHs吸附[23-24]。
此外,为充分利用LDH的吸附性能和TiO2的光催化性能,制备的LDH-TiO2复合材料通过吸附-光催化还原的协同作用去除水中的Cr6+,复合TiO2后的LDH材料通过紫外光照射后去除率可达97%以上,通过调控TiO2与LDH的比例可以改变吸附和光催化效率,实现了对Cr6+的高效去除[21,44]。
刘国等[45]比较研究了MgAl-LDH和EDTA插层LDH对Cd2+的吸附能力。在相同条件下,EDTA插层LDH对溶液中Cd2+的吸附容量远高于MgAl-LDHs,吸附Cd2+的主要机理为EDTA与Cd2+的络合作用。Zhang等[46]用(NH4)2SO4对LDH进行改性,改善了对Pb2+的吸附性能。Chen等[47]采用尿素水解法合成插入镧离子的膨润土改性类LDHs,可以有效地去除水中的重金属Cu2+、Pb2+和染料MO。
改性LDHs易于合成、成本低廉且可重复利用,具有超顺磁性的LDHs还可以在吸附完成后通过外加磁场快速分离固体和液体,因此,改性LDHs在吸附去除重金属离子方面具有广阔用途。
2.2 吸附去除有机污染物
有机污染物种类复杂、污染面广,常规吸附剂对它的去除收效甚微[2]。改性LDHs对于染料等有机污染具有很强的保留能力,能防止二次污染,在治理此类污染中显示出较强的优势,LDHs去除有机污染物情况如表2所示。
表2 LDHs吸附去除有机污染物情况
Tab.2 Adsorptive removal of organic pollutants by LDHs
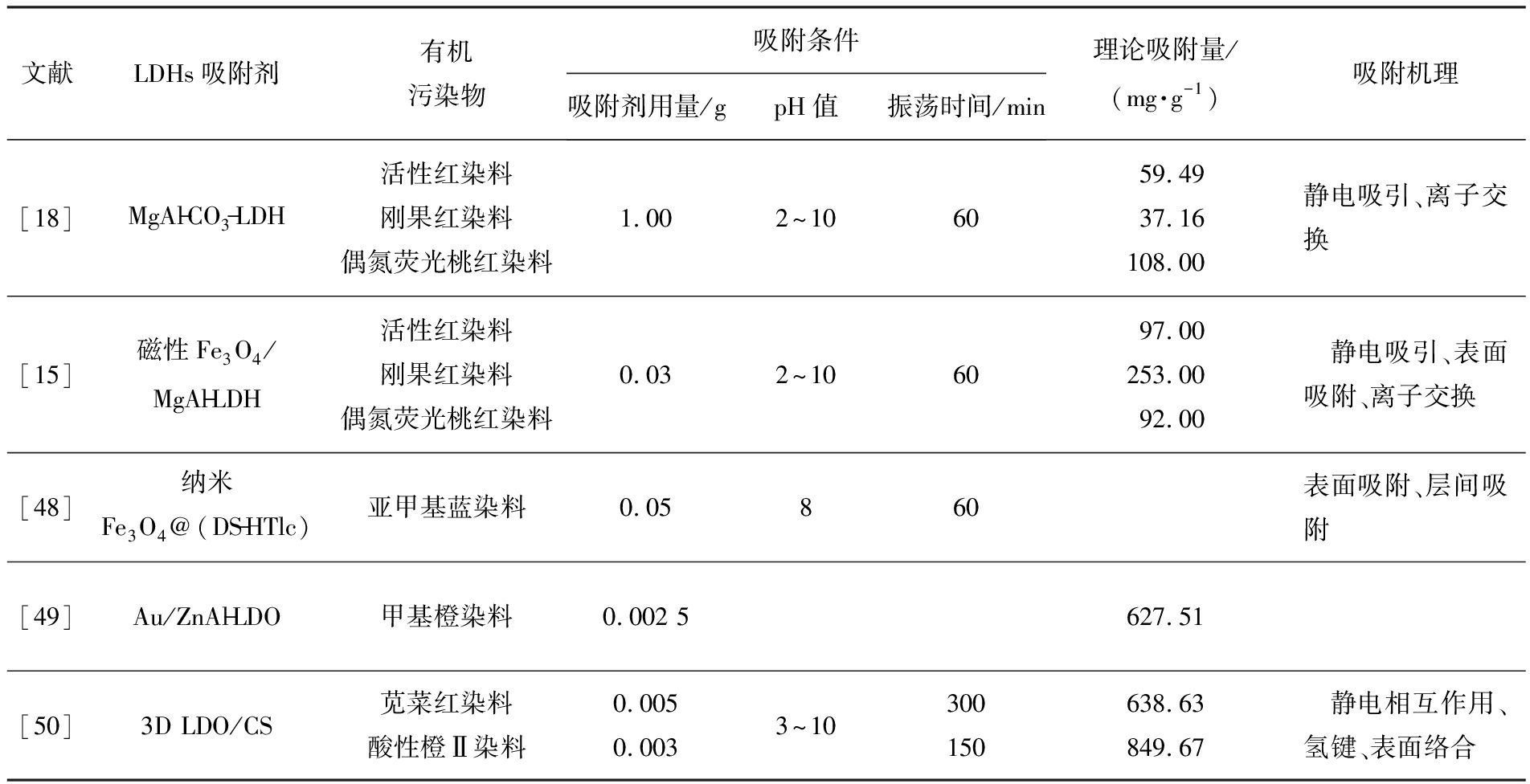
文献LDHs吸附剂有机污染物吸附条件吸附剂用量/gpH值振荡时间/min理论吸附量/(mg·g-1)吸附机理[18]MgAl-CO3-LDH活性红染料刚果红染料偶氮荧光桃红染料1.002^106059.4937.16108.00静电吸引、离子交换[15]磁性Fe3O4/MgAl-LDH活性红染料刚果红染料偶氮荧光桃红染料0.032^106097.00253.0092.00 静电吸引、表面吸附、离子交换[48]纳米Fe3O4@(DS-HTlc)亚甲基蓝染料0.05860表面吸附、层间吸附[49]Au/ZnAl-LDO甲基橙染料0.002 5627.51[50]3D LDO/CS苋菜红染料酸性橙Ⅱ染料0.0050.0033^10300150638.63849.67 静电相互作用、氢键、表面络合
由表2可知,Shan等[18]采用低饱和共沉淀法成功制备出的MgAl-LDH晶型良好,为典型的六边形层状结构,比表面积为104 m2/g,红外光谱峰中具有LDHs的特征光谱,能有效地去除水中活性红、刚果红和偶氮荧光桃红3种红色染料,饱和吸附量分别为59.49、37.16、108.0 mg/g,吸附机理为静电吸引和离子交换。
为了更有利于与粉末材料的分离,Shan等[15]利用Fe3O4@Mg-Al-LDH复合材料去除这3种红色染料,最大吸附量达97、253、92 mg/g,吸附速率很快,在30 min后达到平衡,而且受环境pH值的影响较小(pH值为2~10)。
毕浩宇等[48]以Fe3O4@HTlc纳米复合物为主体,以DS-为客体,采用离子交换法制备不同DS-离子含量的Fe3O4(DS-HTlc)磁性纳米复合体,对阳离子染料亚甲基蓝(MB)有较好的吸附效果,并通过磁分离实现吸附材料的回收。
Zhang等[49]首先通过共沉淀法制备Au/ZnAl-LDH,然后焙烧得到的Au/ZnAl-LDO对MO的吸附容量比其他一些低成本吸附剂大得多。
Lyu等[50]向ZnAl-LDH中添加碳球,采用自组装法制备三维ZnAl-LDH与碳球的复合材料,后经焙烧形成空心结构,焙烧产物是一种高效吸附废水有机染料的材料,可用于吸附酸性橙和苋菜红染料。
2.3 吸附去除无机阴离子
改性LDHs因其离子交换特性而对水体中的无机阴离子污染物有较好的去除效果,可用作高效阴离子吸附剂[2]。目前,多数研究者认为LDHs材料对阴离子污染物的去除机理主要源于其层间阴离子的交换性能、静电吸引、煅烧产物的“记忆效应”以及它们自身的吸附性能,LDHs去除无机阴离子污染物情况表如表3所示。
表3 LDHs吸附去除无机阴离子情况
Tab.3 Adsorptive removal of inorganic anions by LDHs
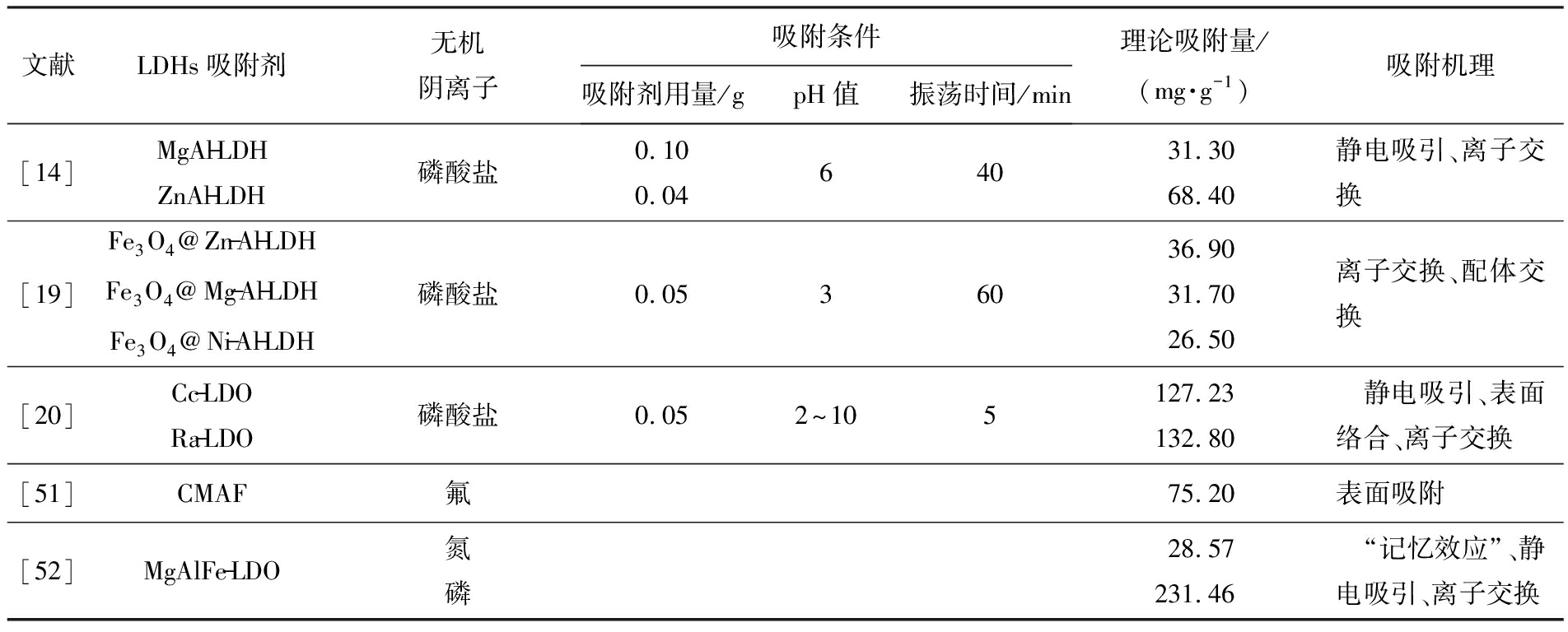
文献LDHs吸附剂无机阴离子吸附条件吸附剂用量/gpH值振荡时间/min理论吸附量/(mg·g-1)吸附机理[14]MgAl-LDHZnAl-LDH磷酸盐0.100.0464031.3068.40静电吸引、离子交换[19]Fe3O4@Zn-Al-LDHFe3O4@Mg-Al-LDHFe3O4@Ni-Al-LDH磷酸盐0.0536036.9031.7026.50离子交换、配体交换[20]Cc-LDORa-LDO磷酸盐0.052^105127.23132.80 静电吸引、表面络合、离子交换[51]CMAF氟75.20表面吸附[52]MgAlFe-LDO氮磷28.57231.46 “记忆效应”、静电吸引、离子交换
由表3可知,Yang等[14]采用共沉淀法合成了MgAl-LDH和ZnAl-LDH,样品晶型比较完整,吸附磷酸盐的最佳用量分别为4、1.6 g/L,两者对磷酸根的去除率均达到95%,是去除磷酸根的有效吸附剂。进一步利用磁性核壳结构的Fe3O4@ZnAl-、Fe3O4@MgAl-和Fe3O4@NiAl-LDH去除磷酸盐,具有较高的吸附容量,在10 s之内可用磁铁进行快速分离[19]。
Zhang等[20]将MgAl-LDH通过共沉淀法负载到白菜、油菜等生物质,限氧煅烧后得到具有较大比表面积和丰富表面官能团的2种生物炭-LDO复合材料,用量仅为0.05 g即可快速去除pH值范围在2~10的50 mg/L磷酸盐,5 min去除率即可达到92%以上。
孔垂鹏等[51]采用水热法合成MgAlFe-LDH(MAF),通过500 ℃煅烧后得到相应复合氧化物CMAF。与MAF相比,CMAF对F-的吸附去除效率显著提高,最大吸附容量可达75.2 mg/g,原因是其有2种除氟的途径,其中一种是表面吸附,另一种是在重构时F-作为层间阴离子进入LDH内部。
万京京等[52]研究了Fe3+掺杂对MgAl-LDO吸附氮磷的影响。LDO吸附硝酸根和磷酸根后会恢复为之前的层状结构,这说明MgAlFe-LDO吸附去除硝酸根和磷酸根的机理之一是发挥“记忆效应”的作用,形成2种离子的插层。当Mg、Al、Fe物质的量比为3∶0.6∶0.4时,MgAlFe-LDO对氮磷吸附性能较好。
3 结论与展望
改性LDHs具有易于合成、稳定性良好、比表面积大、吸附性能优越等特性,在吸附去除水中污染物的治理方面有着很好的前景。主要结论如下:
1)制备改性LDHs的共沉淀法工艺简单,合成周期短,条件易于控制;水热及溶剂热法具有可控制产品晶形,一般无需高温烧结;离子交换法反应时间短,可在对层间阴离子的数量和种类进行组装的同时保持LDHs原有的层状结构;焙烧复原法利用“记忆效应”实现LDHs重复利用。其中共沉淀法和水热法最为常用。
2)改性LDHs吸附重金属离子的机制主要有沉淀反应、络合作用、同晶置换、静电作用等,可被用来去除工业废水中的重金属离子,如Zn2+、Cu2+、Pb2+、Cd2+、Ni2+等。
3)改性LDHs对于染料等有机污染具有很强的保留能力,能防止二次污染,在治理此类污染中显示出较强的优势。
4)改性LDHs由于其层间阴离子的交换性能、静电吸引、煅烧产物的“记忆效应”以及它们自身的吸附性能,对水体中的无机阴离子污染物有较好的去除效果,可用作高效阴离子吸附剂。
改性LDHs在制备与应用上仍需在以下领域继续加强研究:
1)充分发挥LDHs和其他纳米材料的优势,采用多种方法制备高性能的LDHs复合材料,例如:氧化石墨烯与LDHs间存在协同作用,可利用氧化石墨烯良好的分散性以及在水溶液中有较大的表面积的特点,将其与LDHs复合从而改善吸附性能。
2)目前研究多停留在对单一污染物的去除上,而环境中的污染多以复合形式存在,因此需要加强对多种污染物共存时改性LDHs去除污染物的性能研究。
3)改性LDHs吸附污染物的机理研究对理解污染物的吸附过程具有重要作用,仍需综合采用谱学表征、界面化学方法和理论计算等手段开展进一步的深入研究。
4)改性LDHs的水处理应用目前仍主要处于实验室研究阶段,应用范围受限。而实际废水中污染物成分复杂,水量大,影响因素多,需要逐步开展改性LDHs在实际工程中的应用研究。
[1]WU M J,WU J Z,ZHANG J,et al.A review on fabricating heterostructures from layered double hydroxides for enhanced photocatalytic activities[J].Catalysis Science and Technology,2018,8:1207-1228.
[2]BUKHTIYAROVA M V.A review on effect of synthesis conditions on the formation of layered double hydroxides[J].Applied Clay Science,2019,269:494-506.
[3]王宁,庞宏伟,于淑君,等.层状双金属氢氧化物及复合材料对放射性元素铀的吸附及机理研究[J].化学学报,2019,77(2):143-152.
[4]MISHRA G,DASH B,PANDEY S.Layered double hydroxides:a brief review from fundamentals to applications evolving biomaterials[J].Applied Clay Science,2018,153:172-186.
[5]PANG H W,WU Y H,WANG X X,et al.Recent advances in composites of graphene and layered double hydroxides for water remediation:a review[J].Chemistry Asian Journal,2019,14(15):2542-2552.
[6]DAUD M,HAI A,BANAT F,et al.A review on the recent advances,challenges and future aspect of layered double hydroxides (LDH)-containing hybrids as promising adsorbents for dyes removal[J].Journal of Molecular Liquids,2019,288:1-13.
[7]任锦,梁良,周瑜,等.功能化层状双金属氢氧化物材料的应用进展[J].材料科学与工程学报,2019,37(3):509-516.
[8]SHENG T,YAO Y,CHEN T Y,et al.Recent advances in the application of layered double hydroxides in analytical chemistry:a reviews[J].Analytica Chimica Acta,2020,1103:32-48.
[9]ZUBAIR M,DAUD M,MCKAY G,et al.Recent progress in layered double hydroxides (LDH)-containing hybrids as adsorbents for water remediation[J].Applied Clay Science,2017,143:279-292.
[10]GU P C,ZHANG S,Li X,et al.Recent advances in layered double hydroxide-based nanomaterials for the removal of radionuclides from aqueous solution[J].Environmental Pollution,2018,240:493-505.
[11]陆英,程翔,邢波,等.尿素分解共沉淀法中反应时间对ZnAl类水滑石结构和磷吸附性能的影响[J].环境科学,2012,33(8):2868-2874.
[12]PRASAD C,TANG H,LIU W.Magnetic Fe3O4based layered double hydroxides (LDHs) nanocomposites (Fe3O4/LDHs):recent review of progress in synthesis,properties and applications[J].Journal of Nanostructure in Chemistry,2018,8(4):393-412.
[13]BUKHTIYAROVA M V.A review on effect of synthesis conditions on the formation of layered double hydroxides[J].Journal of Solid State Chemistry,2019,269:494-506.
[14]YANG K,YAN L G,YANG Y M,et al.Adsorptive removal of phosphate by Mg-Al and Zn-Al layered double hydroxides:kinetics,isotherms and mechanisms[J].Separation and Purification Technology,2014,124:36-42.
[15]SHAN R R,YAN L G,YANG K,et al.Magnetic Fe3O4/MgAl-LDH composite for effective removal of three red dyes from aqueous solution[J].Chemical Engineering Journal,2014,252:38-46.
[16]YAN L G,YANG K,SHAN R R,et al.Calcined ZnAl-Fe3O4/ZnAl-layered double hydroxides for efficient removal of Cr(Ⅵ) from aqueous solution[J].RSC Advances,2015,5(117):96495-96503.
[17]SHAN R R,YAN L G,YANG K,et al.Adsorption of Cd(Ⅱ) by Mg-A-CO3-and magnetic Fe3O4/Mg-Al-CO3-layered double hydroxides:kinetic,isothermal,thermodynamic and mechanistic studies[J].Journal of Hazardous Materials,2015,299:42-49.
[18]SHAN R R,YAN L G,YANG Y M,et al.Highly efficient removal of three red dyes by adsorption onto Mg-Al-layered double hydroxide[J].Journal of Industrial and Engineering Chemistry,2015,21:561-568.
[19]YAN L G,YANG K,SHAN R R,et al.Kinetic,isotherm and thermodynamic investigations of phosphate adsorption onto core-shell Fe3O4@LDHs composites with easy magnetic separation assistance[J].Journal of Colloid and Interface Science,2015,448:508-516.
[20]ZHANG Z R,YAN L G,YU H Q,et al.Adsorption of phosphate from aqueous solution by vegetable biochar/layered double oxides:fast removal and mechanistic studies[J].Bioresource Technology,2019,284:65-71.
[21]YANG Y T,YAN L G,LI J,et al.Synergistic adsorption and photocatalytic reduction of Cr(Ⅵ) using Zn-Al layered double hydroxide and TiO2 composites[J].Applied Surface Science,2019,492:487-496.
[22]ZHANG X,YAN L G,LI J,et al.Adsorption of heavy metals by L-cysteine intercalated layered double hydroxide:kinetic,isothermal and mechanistic studies[J].Journal of Colloid and Interface Science,2020,562:149-158.
[23]LI J,YU H Q,ZHANG X,et al.Crosslinking acrylamide with EDTA-intercalated layered double hydroxide for enhanced recovery of Cr(VI) and Congo red:adsorptive and mechanistic study[J].Frontiers of Environmental Science &Engineering,2020,14(28):239-247.
[24]LI J,YAN L G,YANG Y T,et al.Insight into the adsorption mechanisms of aqueous hexavalent chromium by EDTA intercalated layered double hydroxides:XRD,FTIR,XPS,and zeta potential studies[J].Journal of Molecular Liquids,2019,43:15915-15923.
[25]夏燕,朱润良,陶奇,等.阴离子表面活性剂改性水滑石吸附硝基苯的特性研究[J].环境科学,2013,34(1):226-230.
[26]陈航,陈鸿,高慧,等.管状纳米氧化物的制备与表征[J].中国粉体技术,2015,21(6):57-60.
[27]衷水平,陈良哲,伍赠玲,等.乙二胺四乙酸根插层镁-铝水滑石的制备与性能[J].中国粉体技术,2016,22(2):48-50.
[28]HASSANI K E,BEAKOU B H,KALNINA D,et al.Effect of morphological properties of layered double hydroxides on adsorption of azo dye methyl orange:a comparative study[J].Applied Clay Science,2017,140:124-131.
[29]衡惠敏,常艳,李良君,等.水热法合成纳米层状双金属氢氧化物[J].西南科技大学学报,2013,28(2):9-12,56.
[30]ZHAO X D,CAO J P,ZHAO J,et al.A hybrid Mg-Al layered double hydroxide/graphene nanostructure obtained via hydrothermal synthesis[J].Chemical Physics Letters,2014,605/606:77-80.
[31]HUANG Q Q,CHEN Y,YANG K,et al.Magnetic graphene oxide/MgAl-layered double hydroxide nanocomposite:one-pot solvothermal synthesis,adsorption performance and mechanisms for Pb2+,Cd2+,and Cu2+[J].Chemical Engineering Journal,2018,341:1-9.
[32]SUN J H,CHEN Y,YU H Q,et al.Removal of Cu2+,Cd2+ and Pb2+ from aqueous solutions by magnetic alginate microsphere based on Fe3O4/MgAl-layered double hydroxide[J].Journal of Colloid and Interface Science,2018,532:474-484.
[33]HOU T L,YAN L G,YANG S Y,et al.Efficient removal of graphene oxide by Fe3O4/MgAl-layered double hydroxide and oxide from aqueous solution[J].Journal of Molecular Liquids,2019,284:300-306.
[34]YANG F C,SUN S Q,CHEN X Q,et al.Mg-Al layered double hydroxides modified clay adsorbents for efficient removal of Pb2+,Cu2+ and Ni2+ from water[J].Applied Clay Science,2016,123:134-140.
[35]ZOU Y D,WANG P Y,YAO W,et al.Synergistic immobilization of ![]() by novel graphitic carbon nitride@layered double hydroxide nanocomposites from wastewater[J].Chemical Engineering Journal,2017,330(15):573-584.
by novel graphitic carbon nitride@layered double hydroxide nanocomposites from wastewater[J].Chemical Engineering Journal,2017,330(15):573-584.
[36]WEI M,SHI Z Y,EVANS D G,et al.Study on the intercalation and interlayer oxidation transformation of L-cysteine in a confined region of layered double hydroxides[J].Journal of Materials Chemistry,2006,16(21):2102-2109.
[37]GONZALEZ M A,PAVLOVIC I,DELGADO R,et al.Removal of Cu2+,Pb2+ and Cd2+ by layered double hydroxide-humate hybrid.Sorbate and sorbent comparative studies[J].Chemical Engineering Journal,2014,254:605-611.
[38]苏继新,殷晶,屈文,等.插层水滑石的组装及对对硝基甲苯的吸附[J].中国环境科学,2009,29(5):518-523.
[39]李燕,王国旺,王宁.改性层状双氢氧化物对铜离子(Ⅱ)和双酚A的协同吸附[J].应用化学,2015,32(7):816-824.
[40]YAO W,YU S J,WANG J,et al.Enhanced removal of methyl orange on calcined glycerol modified nanocrystallined Mg/Al layered double hydroxides[J].Chemical Engineering Journal,2017,307(1):476-486.
[41]HOU T L,YAN L G,LI J,et al.Adsorption performance and mechanistic study of heavy metals by facile synthesized magnetic layered double oxide/carbon composite from spent adsorbent[J].Chemical Engineering Journal,2020,384:123331.
[42]马明海,万顺利.改性水滑石处理垃圾渗滤液生化尾水的试验研究[J].工业水处理,2014,34(11):40-43.
[43]LYU F Y,YU H Q,LI J,et al.Efficient and fast removal of Pb2+ and Cd2+ from an aqueous solution using a chitosan/Mg-Al-layered double hydroxide nanocomposite[J].Journal of Colloid and Interface Science,2018,539:184-193.
[44]YANG Y T,LI J,YAN T,et al.Adsorption and photocatalytic reduction of aqueous Cr(Ⅵ) by Fe3O4-ZnAl-layered double hydroxide/TiO2 composites[J].Journal of Colloid and Interface Science,2019,562:493-501.
[45]刘国,吴茜,李君.乙二胺四乙酸插层水滑石吸附Cd(Ⅱ)的影响因素研究[J].环境工程,2015,33(7):41-45.
[46]ZHANG Z Q,ZENG H Y,LIU X J,et al.Modification of MgAl hydrotalcite by ammonium sulfate for enhancement of lead adsorption[J].Journal of the Taiwan Institute of Chemical Engineers,2016,60:361-368.
[47]CHEN Y,PENG J D,XIAO H,et al.Adsorption behavior of hydrotalcite-like modified bentonite for Pb2+,Cu2+ and methyl orange removal from water[J].Applied Surface Science,2017,420:773-781.
[48]毕浩宇,葛金宝,张雅,等.纳米Fe3O4@(DS-HTlc)的制备及吸附亚甲基蓝[J].水处理技术,2019,45(12):46-52.
[49]ZHANG Y X,HAO X D,KUANG M,et al.Preparation,characterization and dye adsorption of Au nanoparticles/ZnAl layered double oxides nanocomposites[J].Applied Surface Science,2013,283:505-512.
[50]LYU H X,HU K,FAN J S,et al.3D hierarchical layered double hydroxide/carbon spheres composite with hollow structure for high adsorption of dye[J].Applied Surface Science,2020,500:1-8.
[51]孔垂鹏,聂玉伦,胡春.Mg/Al/Fe复合氧化物吸附去除水体中氟化物的研究[J].环境工程学报,2010,4(1):110-114.
[52]万京京,郝瑞霞,马静雨,等.Fe(Ⅲ)掺杂Mg/Al-LDO作为氮磷吸附剂的研究[J].中国环境科学,2018,38(4):1295-1303.