吸入式给药是指药物经特殊装置从呼吸道吸入的一种新型非侵入给药方式,具有起效快、用量少、不良反应少、使用方便和患者依从性好等特点,成为近年来给药途径研究领域的热点之一。目前,已有少数鼻腔给药制剂被研发,如用于治疗糖尿病的胰岛素吸入粉雾剂Exubera和Afrezza,用于治疗哮喘的的干粉吸入剂Spiromax等。
微粉粒径是影响吸入给药的重要因素之一[1]。已有的研究表明,吸入式给药的给药效果不仅与药物颗粒的几何粒径有关,还与药物的空气动力学粒径有关,几何粒径为1~5 μm的颗粒虽可以到达肺部深处,但会被巨噬细胞吞噬,只有颗粒的空气动力学粒径为1~5 μm,而几何粒径不在1~5 μm之间的微粒才能满足肺部吸入式给药的要求[2-3]。
超临界流体技术具有绿色环保等特点,被广泛应用于制备微粉。目前,最常用的超临界流体微粉制备工艺主要有超临界溶液快速膨胀、超临界反溶剂法、超临界辅助物化法和气体饱和溶液法。其中,超临界反溶剂法具有可控的微粉粒径及粒径分布、不易发生团聚与共析、能够保持生物活性、适用于热敏性物质操作等优点[4],已被应用于众多领域,如制备炸药、催化剂、聚合物、生物高分子、药物等[5-7]。
本文中以非成瘾性镇咳药枸橼酸喷托维林为研究对象,采用自制的超临界反溶剂装置,系统研究了压力、温度、进样速率和溶剂等工艺参数对微粉粒径、粒径分布和形貌等的影响,制备了符合吸入式给药的橼酸喷托维林微粉。
1 实验
1.1 材料与仪器
二甲基亚砜、N,N-二甲基甲酰胺、甲醇、二氯甲烷(均为分析纯,北京化工厂);枸橼酸喷托维林(自制);CO2(纯度体积分数为99.9%,北京安泰隆实验设备有限公司)。
S4800型场发射扫描电镜(日本日立公司);Mastersizer 3000型激光粒度分析仪(英国Malvern公司);3321型动力学粒径谱仪(美国TSI公司)。
1.2 装置及流程
实验装置如图1所示,冰水浴冷却的CO2经高压柱塞泵升压、恒温水浴加热后,进入高压反应釜中,枸橼酸喷托维林溶液经高效液相泵和喷嘴喷入高压反应釜中,超临界CO2将溶液中的溶剂带出高压反应釜,同时枸橼酸喷托维林微粒析出。 CO2和溶剂的混合物进入冷凝器降温后,溶剂被回收,CO2排空或循环再利用。
1.3 方法和参数选择
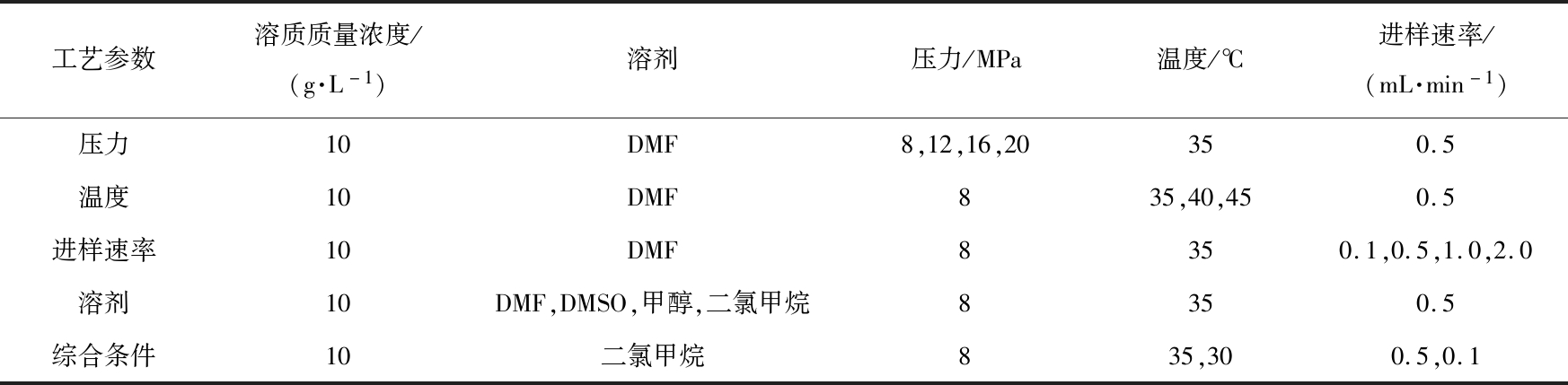
本实验中考察了压力、温度、进样速率和溶剂等工艺参数对制备的枸橼酸喷托维林微粉的粒径、粒径分布和形貌等的影响。具体实验操作条件如表1所示。
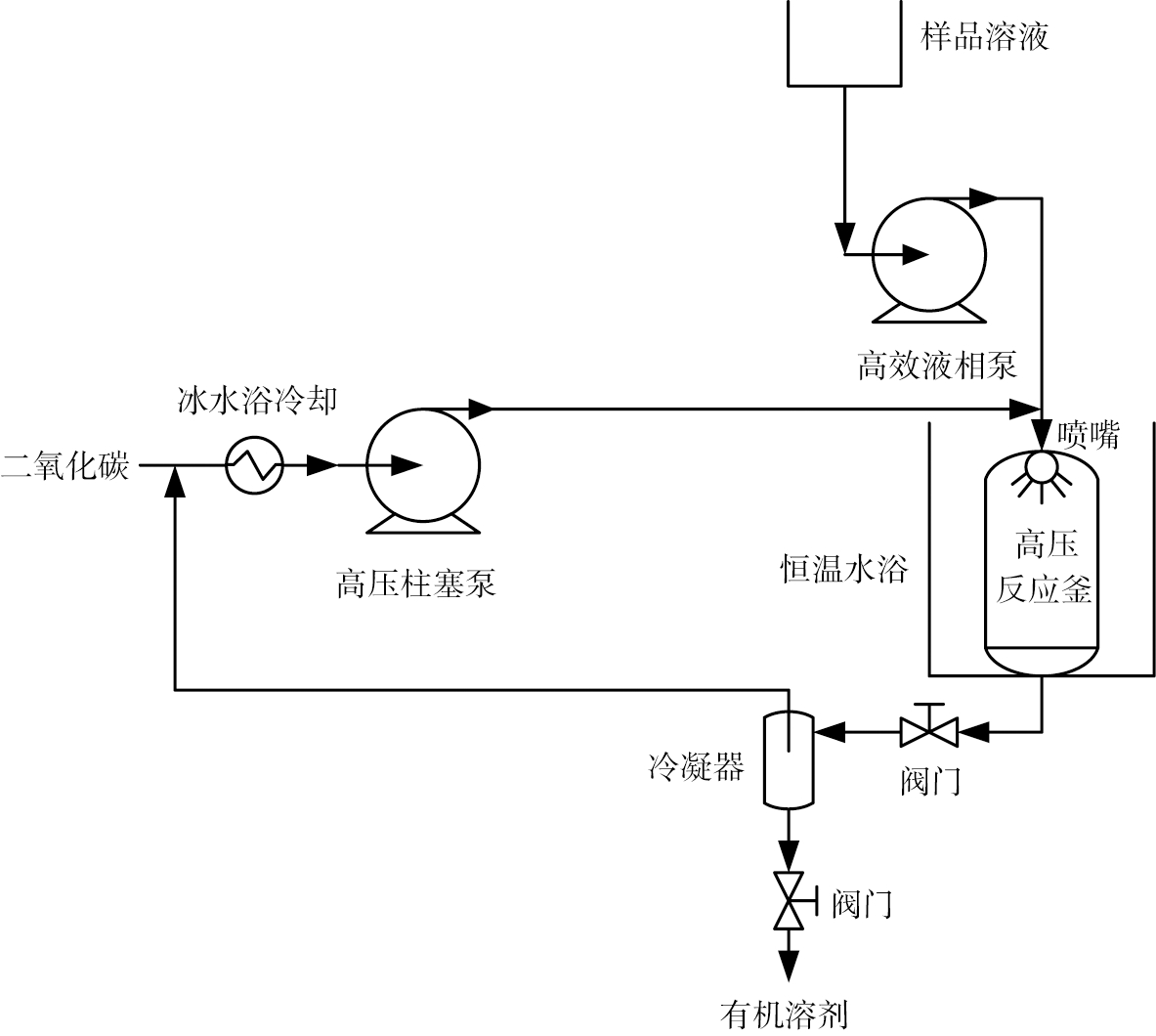
图1 超临界反溶剂装置示意图
Fig.1 Schematic drawing of supercritical antisolvent process
表1 实验过程操作参数
Tab.1 Process data of experiments
工艺参数溶质质量浓度/(g·L-1)溶剂压力/MPa温度/℃进样速率/(mL·min-1)压力10DMF8,12,16,20350.5温度10DMF835,40,450.5进样速率10DMF8350.1,0.5,1.0,2.0溶剂10DMF,DMSO,甲醇,二氯甲烷8350.5综合条件10二氯甲烷835,300.5,0.1
2 结果与讨论
2.1 压力对微粉性能的影响
图2、3分别为不同压力制备微粉的粒径及粒径分布图与扫描电镜图。由图2可以看出,随着压力的增大,制备枸橼酸喷托维林微粉的粒径增大,粒径分布变宽。由图3可以看出,微粉微观形貌均为表面光滑的片状结构,且在20 MPa时,出现明显的颗粒团聚现象。这是因为当高压CO2喷出喷嘴后,喷嘴出口处体积迅速膨胀,造成喷嘴附近温度下降,影响溶剂脱除效果和喷嘴雾化效果,导致颗粒出现团聚现象,粒径变大[8-9];另一方面,随着压力的增大,微粒的结晶生长速率也将显著增大,从而导致粒径尺寸增大,粒径分布变宽。
2.2 温度对微粉性能的影响
图4、5分别为不同温度制备微粉的粒径及粒径分布图与扫描电镜图像。
由图4可以看出,随着温度的升高,制备的枸橼酸喷托维林微粉粒径增大,粒径分布变宽。由图5可以看出,微粉微观形貌上均为表面光滑的片状结晶,但微粒粒径明显增大。这是因为超临界CO2的密度随着温度的升高而减小,CO2向溶剂的传质效率降低,颗粒粒径增大;此外,溶质分子动能随温度升高而增加,小颗粒相互碰撞聚集的机会增多,导致微球粒径增大,与文献[10]研究结果相同。
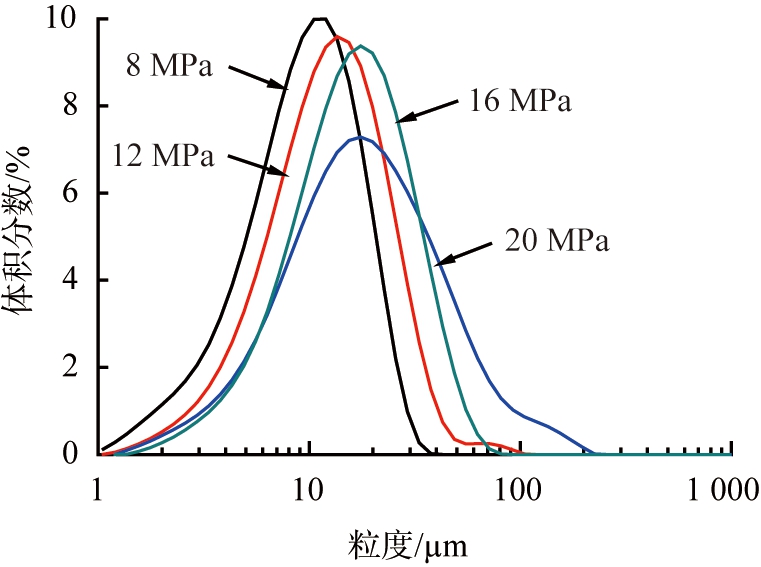
图2 不同压力制备微粉的粒径及粒径分布
Fig.2 Particle size distributions of samples prepared by different pressures

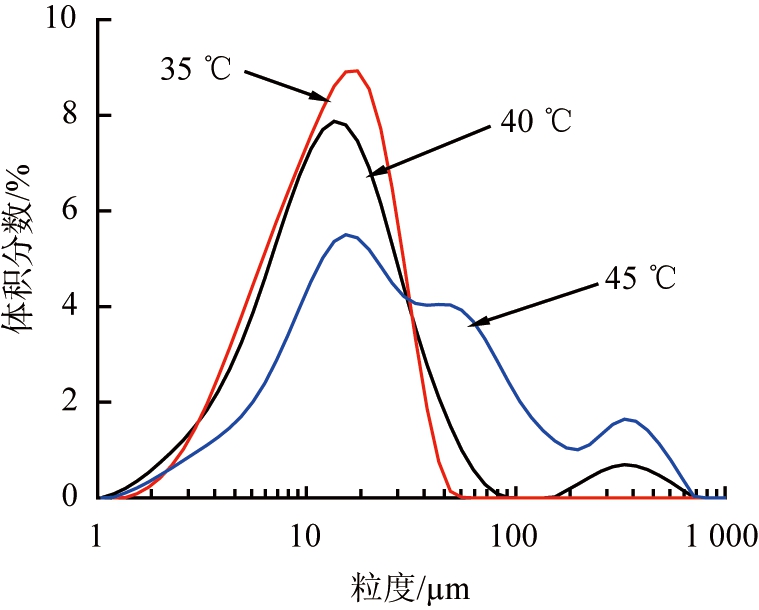
图4 不同温度制备微粉的粒径及粒径分布图
Fig.4 Particle size distributions of samples prepared by different temperatures

a 35 ℃

b 40 ℃

c 45 ℃
图5 不同温度制备微粉的扫描电镜图像
Fig.5 SEM images of samples prepared by different temperatures
2.3 进样速率对微粉性能的影响
图6、7分别为不同进样速率制备微粉的粒径及粒径分布图与扫描电镜图像。
由图6可以看出,随着进样速率的增大,制备的药物微粉的粒径变大,粒径分布明显变宽。
由图7可以看出,微粉微观形貌均为表面光滑的片状,且单个微粒的粒径明显变大。 这是因为随着进样速率的增大,单位时间内喷入结晶釜的样品量增加,晶核周围有足够的溶质分子供其生长,故形成的颗粒粒径较大; 另一方面,进样速率的增大会影响溶剂的雾化效果,液滴无法形成较小的液滴,致使传质效果减弱,瞬间成核数量减少,颗粒的生长速度大于析出速度,形成的颗粒粒径较大且分布较宽。
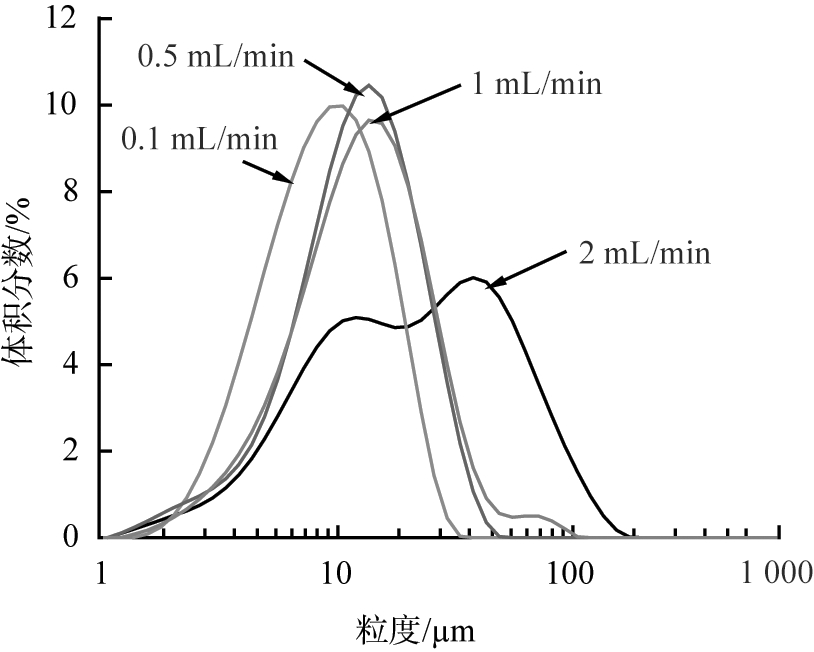
图6 不同进样速率制备微粉的粒径及粒径分布
Fig.6 Particle size distributions of samples prepared by different flow rates
2.4 溶剂选择对微粉性能的影响
图8为不同溶剂制备微粉的粒径及粒径分布图与扫描电镜图像。
由图8a可以看出,采用不同溶剂制备的枸橼酸喷托维林微粉粒径及粒径分布有明显变化,选用二氯甲烷作为溶剂,制备的微粉粒径较小,粒径分布较窄。这是因为二氯甲烷的黏度、沸点与挥发度均低于其他3种溶剂,更有利于被CO2萃取,形成较大过饱和度,促进溶质快速结晶析出而避免过分长大[11-12]。由电镜图可以看出,不同溶剂制备的枸橼酸喷托维林微粉的微观形貌均为片状,这与枸橼酸喷托维林的晶形有关;但片状结构也稍有不同,这是因为超临界反溶剂法中,不同的溶剂传质过程不同,形成不同表面形貌[13]。使用DMSO、 DMF和甲醇为溶剂,溶质均能够比较完整地形成核结晶与长大,微观形貌主要呈现表面光滑的片状结晶; 而使用二氯甲烷作为溶剂,由于萃取溶剂速率较快,许多溶质晶核形成后没有充分的条件顺利长大,因此呈现为不规则的表面不光滑的片状结构,且尺寸较小。

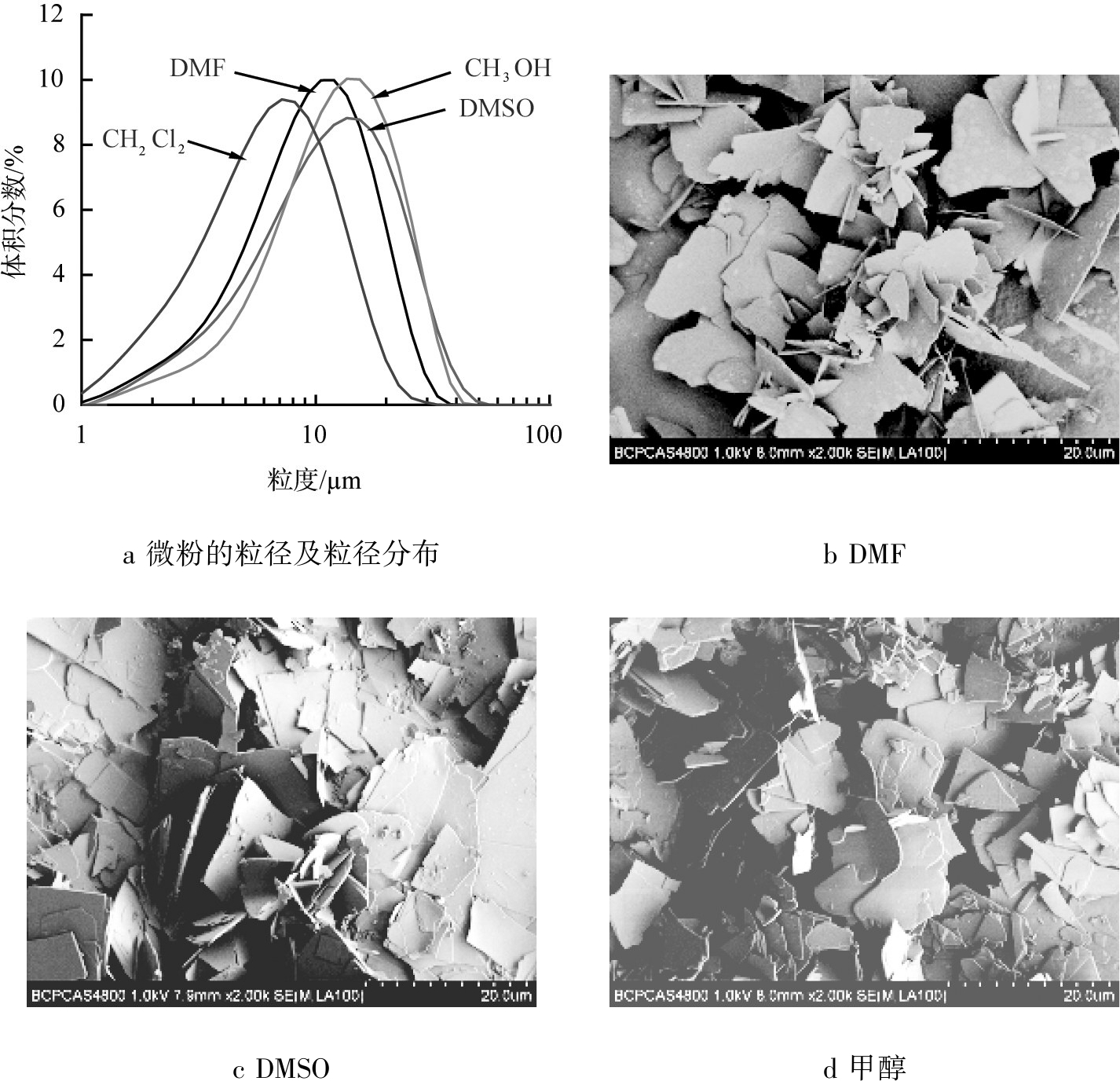

e 二氯甲烷
图8 不同溶剂制备微粉的粒径分布和扫描电镜图像
Fig.8 Particle size distributions and SEM images of samples prepared by different solvents
2.5 综合条件优化
通过优化各工艺参数,以二氯甲烷为溶剂,分别在低温、低压、低流速下制备的枸橼酸喷托维林微粉,微粉的粒径及粒径分布与扫描电镜结果见图9、 10。
由图9可以看出,随着温度、 流速的降低,制备的微粉粒径变小,粒径分布变窄; 在30 ℃、 8 MPa的亚临界状态下制备的微粉粒径最小,粒径分布最窄,几何粒径为0.5~12 μm; 并测定亚临界状态下制备微粉的空气动力学粒径为1.2 μm; 由几何粒径和空气动力学粒径可以看出,制备的微粉粒径符合吸入式给药的要求。由图10可以看出,随着温度和进样速率的降低,微粉的微观形貌由平板状的片状逐渐转变为折叠、扭曲状的片状。
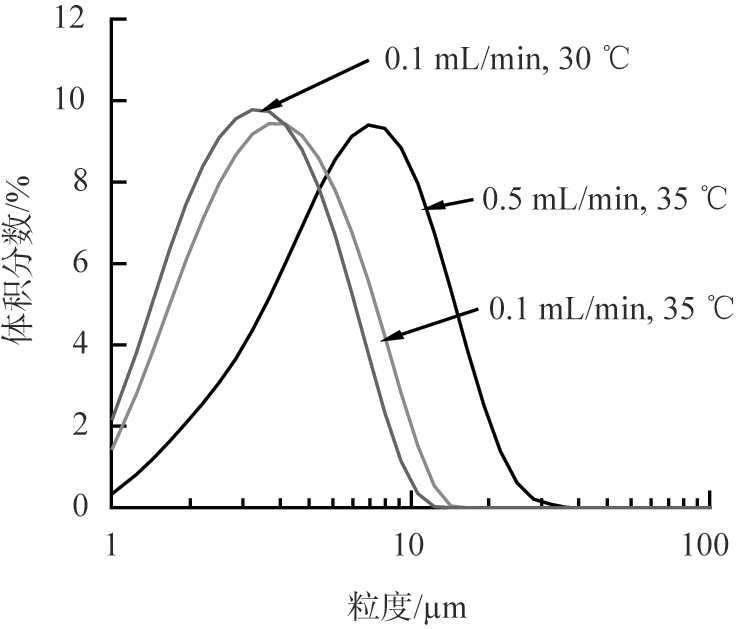
图9 优化条件制备微粉的粒径及粒径分布
Fig.9 Particle size distributions of samples prepared by optimal process parameters

a 0.5 mL/min,35 ℃

b 0.1 mL/min,35 ℃
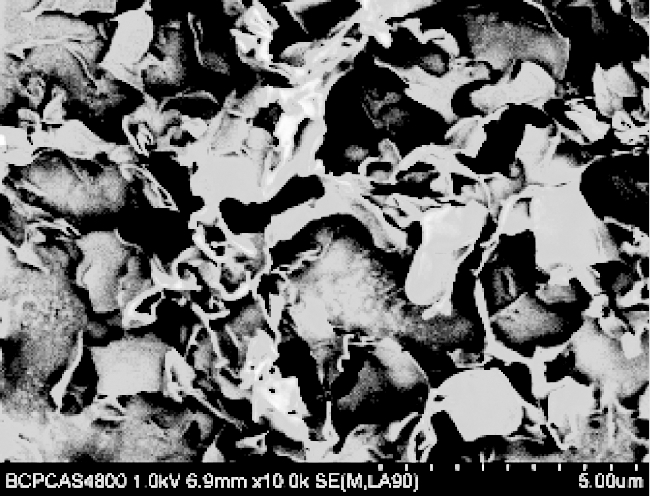
c 0.1 mL/min,30 ℃
图10 优化条件制备微粉的扫描电镜图像
Fig.10 SEM images of samples prepared by optimal process parameters
3 结论
1)不同溶剂、压力、温度和进样速率等工艺参数都会影响微粉的粒径,降低温度、压力、进样速率均能减小微粉的粒径,溶剂选择还会影响微粉的微观形貌。
2)通过优化工艺参数,在二氯甲烷为溶剂,进样速率为0.1 mL/min,温度为30 ℃、 压力为8 MPa的亚临界条件下,制备出的微粉几何粒径为0.5~12 μm,空气动力学粒径为1.2 μm,符合吸入式给药对微粉粒径的要求。
[1]WANG Y L,WANG Y P,YANG J,et a1. The application of a supercritical antisolvent process for sustained drug delivery[J]. Powder Technology,2006,164(2): 94-102.
[2]SHOYELE S A. Engineering protein particles for pulmonary drug delivery[J]. Methods in Molecular Biology,2008,437: 149-160.
[3]唐川. 超临界溶液浸渍法制备载药多孔微球用于肺部吸入式给药[J]. 大连大学学报,2017,38(6): 69-76.
[4]REVERCHON E,MARCO I D,ADAMI R,et al. Expanded micro-particles by supercritical antisolvent precipitation: interpretation of results[J]. The Journal of Supercritical Fluids,2008,44(1): 98-108.
[5]JIANG H X,WU X H,WANG C X,et al. CeO2-ZrO2-Al2O3 ternary oxides synthesized via supercritical anti-solvent and as a support for Pd catalyst for CO oxidation[J]. Catalysis Survey from Asia,2017,21: 37-44.
[6]KUDRYASHOVA E V,SUKHOVERKOV K V,DEYGEN I M,et al. Moxifloxacin micronization via supercritical antisolvent precipitation[J]. Russian Journal of Physical Chemistry B,2017,11(7): 1153-1162.
[7]VOROBEI A M,USTINOVICH K B,POKROVSKIY O I,et al. Preparation of hydroxypropylmethylcellulose microparticles using supercritical antisolvent precipitation[J]. Russian Journal of Physical Chemistry B,2015,9(8): 1103-1108
[8]蓝洪桥,张蕾,庄吴勇,等. 超临界抗溶剂雾化技术制备壳聚糖微粒[J]. 厦门大学学报(自然科学版),2010,49(1): 139-143.
[9]KROBER H,TEIPEL U. Materials processing with supercritical antisolvent precipitation: process parameters and morphology of tartaric acid[J]. The Journal of Supercritical Fluids,2002,22(3): 229-235.
[10]于文利,陈蓓怡,赵亚平,等. SEDS技术制备水飞蓟素纳米颗粒[J]. 高校化学工程学报,2005,9(5): 695-698.
[11]MIGUEL F,MARTIN A,GAMESE T,et al. Supercritical solvent precipitation of lycopene: effect of the operating parameters[J]. The Journal of Supercritical Fluids,2006,36(3): 225-235.
[12]VARUGHESE P,LI J,WANG W,et al. Supercritical antisolvent processing of γ-Indomethacin: effects of solvent,concentration,pressure and temperature on SAS processed indomethacin[J]. Powder Technology,2010,201(1): 64-69.
[13]DUKHIN S S,SHEN Y,DAVE R,et al. Drople mass transfer,intradrople nucleation and submicron particle production in two phase flow of solvent-supercritical antisolvent emulsion[J]. Colloids and surfaces A: Physicochemical and Engineering Aspects,2005,26(1/2/3): 163-176.