分子相关光谱法(photon correlation spectroscopy, PCS)及动态光散射法(dynamic light scattering, DLS)已成为测量亚微米-纳米级颗粒粒径的一种常规方法[1-3]。该方法可以在几分钟内统计出平均粒径。在此基础上,2种粒径分析的国家标准[4-5](GB/T 19627—2005和GB/T 209022—2012)及上海市地方计量标准[6](JJF(沪)4—2006)已编著实施,并且简单方便的商业化仪器亦已推出。单分散聚合物微球因自身具有粒径均一、比表面积大、化学稳定性高等优点,在高效色谱、标准计量、生物化学、医疗载体等多领域中被广泛应用[7-9]。
在粒径测量中,单分散聚合物微球常作为标准粒子对粒径检测仪器进行检测监控。3个粒径测试标准都推荐使用较窄粒径分布的聚苯乙烯乳胶球悬浮液作为标准物质,但对于标准物质水分散介质的选择并不统一。GB/T 19627—2005标准推荐使用新鲜的蒸馏水或去离子过滤水,认为对强电荷稳定化分散体系,可加入微量的盐类;GB/T 209022—2012标准并没有强调水的使用;而JJF(沪)4—2006标准推荐使用去离子水或蒸馏水制备的浓度为0.01 mol/L的氯化钠过滤溶液。
在实际应用中,以不同水样作为分散介质时,标准粒子平均粒径测量值会偏离粒子标称值。其主要原因是来自于颗粒表面的水化膜。对于一些颗粒物质,如胶体或矿物颗粒等,当颗粒处于水中时,在其表面附近的水分子由于吸引作用力[10],具有表面定向排列的趋势,从而在颗粒表面形成有序的边界层,这种现象即为水化作用[11],形成的边界层也叫作水化膜。Marian等[12]通过极化模型计算水化力胶体颗粒之间的作用力,认为当2个颗粒靠得足够近时,水化膜重叠并产生极大的排斥力,即水化力,水化作用越强,水化膜越厚,相应的水化斥力越强,溶液体系越稳定,一般水化斥力比静电斥力大1~2个数量级。
水化膜的存在有利有弊,它使煤泥水难以沉降,使生物分子稳定存在[13-16],也使颗粒粒径测试过程中所测得的表观粒径偏大。
本文中以粒径为(100±3) nm的聚苯乙烯微球为样品,对比超纯水(ultrapure water, UP, 电阻率≥18 MΩ·cm)、蒸馏水(屈臣氏)、反渗透水(reverse osmosis,RO电导率:1~5 μS/cm)、洞庭山矿泉水4种不同纯度的水分散介质所测得的平均粒径,其中UP水为空白溶液,研究在不同含盐量的分散介质下样品平均粒径的变化,分析离子对水化膜的作用,确定盐溶液浓度的选择范围,并以溶液电导率值作为一种评判方法,为粒度仪器系统验证的分散介质的选择提供依据。
1 实验
1.1 仪器与原料试剂
Nanophox纳米激光粒度仪(德国新帕泰克公司);UPH-I-5T优普超纯水机(上海川玉仪器有限公司);DDB-303A型便携式电导率仪(上海仪电科学仪器股份有限公司)。
聚苯乙烯微球(美国DUKE3100A微粒,美国国家标准技术研究院认证,平均粒径大小为(100±3) nm,标准偏差为7.8 nm); 氯化钠(纯度大于99.9%(质量分数))、氯化钾(纯度为99%~100.5%(质量分数))(均为分析纯,Amresco公司)。
1.2 方法
1.2.1 配置不同浓度的NaCl和KCl溶液
用UP水分别配制浓度为0.2、2 mol/L的NaCl和KCl溶液。对其进行稀释,配制成13种不同浓度(见表1)的体积均为10 mL的NaCl和KCl溶液。
为了减少稀释造成的浓度误差,其中1—10号溶液利用浓度为0.2 mol/L溶液稀释配制,12—13号溶液分别来利用浓度为2 mol/L溶液稀释配制。
表1 不同浓度的盐溶液配制方法
Tab.1 Preparation methods of salt solutions with different concentrations

编号12345678910111213浓度/(mol·L-1)5×10-51×10-45×10-41×10-35×10-31×10-22×10-24×10-28×10-20.10.20.30.4
1.2.2 粒径测试
向上述溶液中分别滴加1滴聚苯乙烯微球溶液,放置于水浴槽中,保持25 ℃恒温,选用波长为632.8 nm的氦氖激光器发射的激光光束照射到该悬浮液的中心位置。被悬浮颗粒散射后,在90 °散射方向上被检测器记录,由于颗粒连续地作布朗运动或热运动,在浓度很低时,颗粒的运动是由悬浮流体的温度、黏度和颗粒大小决定,检测到的散射光强度I(t)会随着时间涨落,检测器将这些信息传送至相关器中,相关器建立了散射光强度的时间相关函数G(τ):
G(τ)=〈I(t)·I(t+τ)〉,
(1)
式中:G(τ)为自相关函数;I(t)为光束在t时刻的散射强度;I(t+τ)为光束在t+τ时刻的散射强度。
最后计算得出粒子的平均粒径,这里测得的粒径指的是水动力粒径,即表观粒径。此相关函数只取决时间差,相关函数一般有2种,一种为自相关函数,另一种为交叉相关(又叫做互相关)函数,对应的原理如图1所示。自相关法(auto correlation, AC法)只有一束单色相干的激光光束,在给定的时间内,检测器记录被激光照射体积内的散射光总和,其散射光强度与自身的衰减值相关。交叉相关法(cross correlation, CC法)是由2束单色相干的激光光束,在同一体积中可以进行2次独立的散射测量,类似数学中的并集,2次散射强度相对一致才有效,可减少多重散射的影响,提高测试准确性。
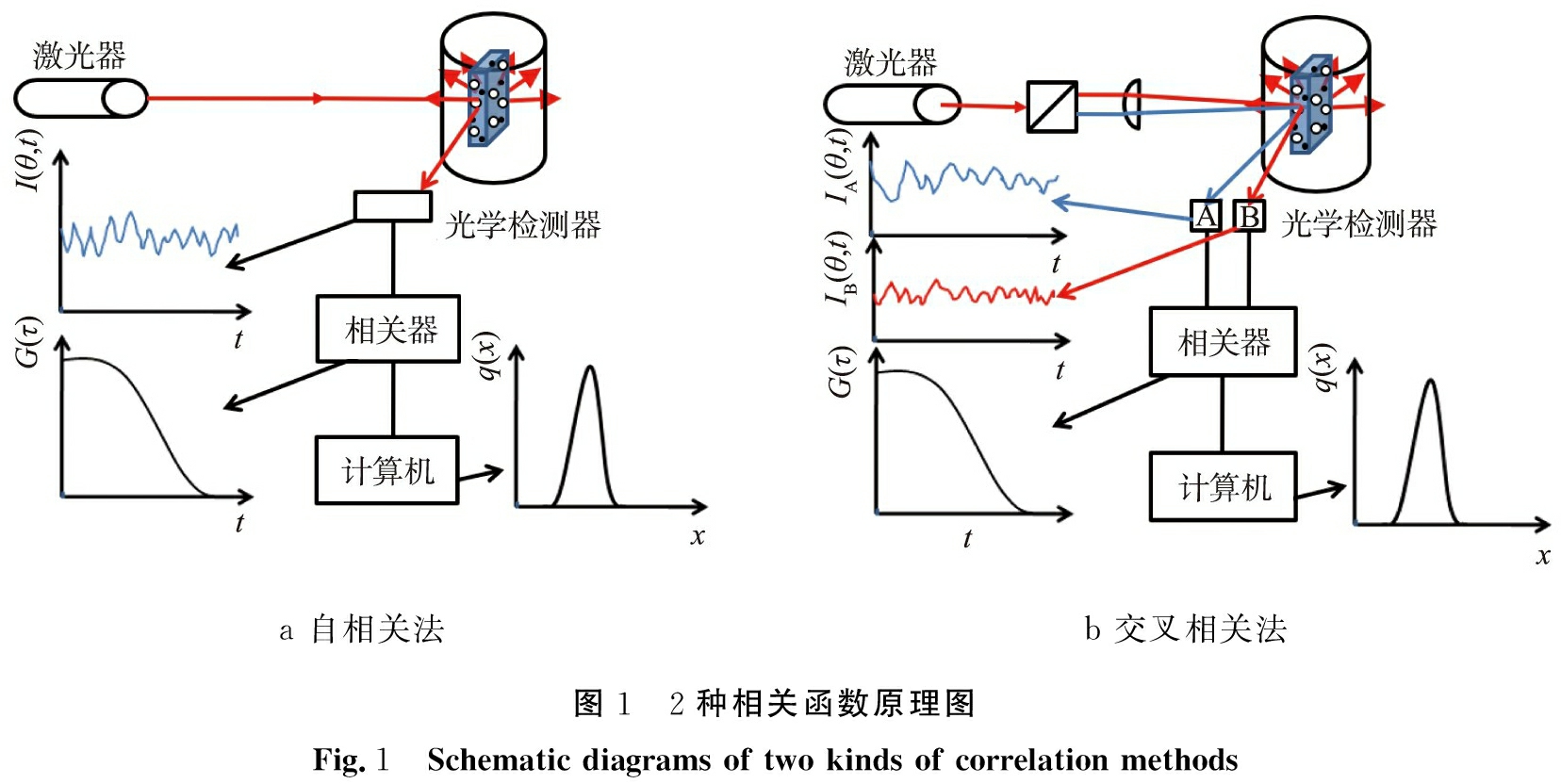
a 自相关法b 交叉相关法图1 2种相关函数原理图Fig.1 Schematic diagrams of two kinds of correlation methods
选用UP水、蒸馏水、RO水及矿泉水4种不同纯度的水作为分散介质,研究水化膜的存在及微量离子对粒径测量的影响。为了保证实验结果的可比性,统一选用CC法,并配制相同浓度的液体,所测得的溶液计数率在500~700千次/s(kilo-counts per second, kcps),其他测试条件都保持一致。
为了保证实验结果的准确性,比色皿用对应的水样润洗3次,并静止2 min,避免灰尘及气泡的影响,分别对4组液体进行7次测量。表2是聚苯乙烯微球分散在4种水样下的平均粒径统计表。
表2 聚苯乙烯微球分散在4种水质中的平均粒径
Tab.2 Average particle diameters of polystyrene microsphere dispersed in four kinds of water nm
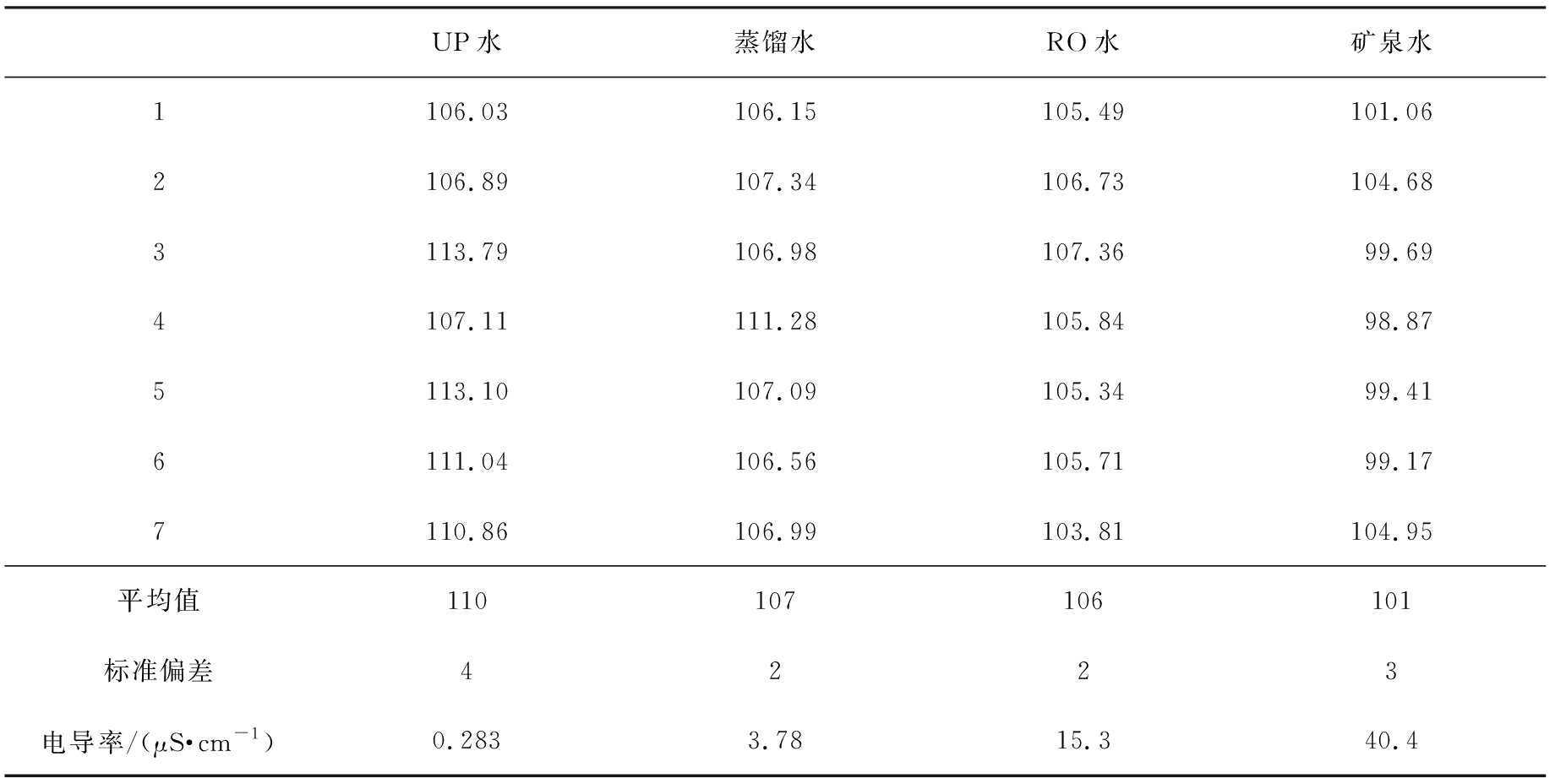
UP水蒸馏水RO水矿泉水1106.03106.15105.49101.062106.89107.34106.73104.683113.79106.98107.3699.694107.11111.28105.8498.875113.10107.09105.3499.416111.04106.56105.7199.177110.86106.99103.81104.95平均值110107106101标准偏差4223电导率/(μS·cm-1)0.2833.7815.340.4
2 结果与讨论
2.1 不同纯度水分散的粒径测试
UP水、蒸馏水、RO水及矿泉水作为分散介质的聚苯乙烯颗粒平均粒径分别为(110±4)、(107±2)、(106±2)、(101±3) nm,与标准物质所给的(100±3) nm粒径值对比,其相对误差分别为10%、7%、6%和1%。很明显,UP水、蒸馏水及RO水为分散介质所测得的结果极大偏离粒子标准值,而矿泉水测试结果较为理想。对比这4种水样处理方式,UP水是通过离子交换柱及纯化柱等手段提取,其电阻率≥18MΩ·cm,在这4种水样中纯度最大,离子浓度最小。蒸馏水通过蒸馏、冷凝方法提取出来,纯度也很高,RO水相对于UP水,其离子浓度相对较高,而矿泉水中含有微量矿物质,其离子浓度是这4种水样中最大的。
通过电导率测试,验证了这4种离子浓度大小,cUP水<c蒸馏水<cRO水<c矿泉水,初步可以得出,以UP水为分散介质的溶液,聚苯乙烯微球表面存在近10 nm厚的水化膜,而少量的离子可以压缩粒子表面的水化膜,有助于提高粒径测试的准确性。
2.2 不同含盐量的粒径测试
图2是不同NaCl或KCl浓度下,溶液的电导率及测得的平均粒径大小。从图中可以看出,溶液中随着NaCl或KCl含量的增加,所测得的标准粒子的平均粒径先减小至标称值,随后又缓慢增大,最后急剧增大。
在浓度为5×10-5~0.1 mol/L时,电导率与离子浓度呈线性关系。UP水中测得的粒径远大于标称值是因为聚苯乙烯微球表面由于范德华力、静电力等作用力,吸引水分子,使得粒子表面形成有序的水化膜,含水化膜的粒子体系又由于表面的静电斥力,降低了粒子之间的作用力,可以稳定存在,而激光纳米粒度仪测的是粒子表观粒径,所以测试结果远大于标准粒子标称值。
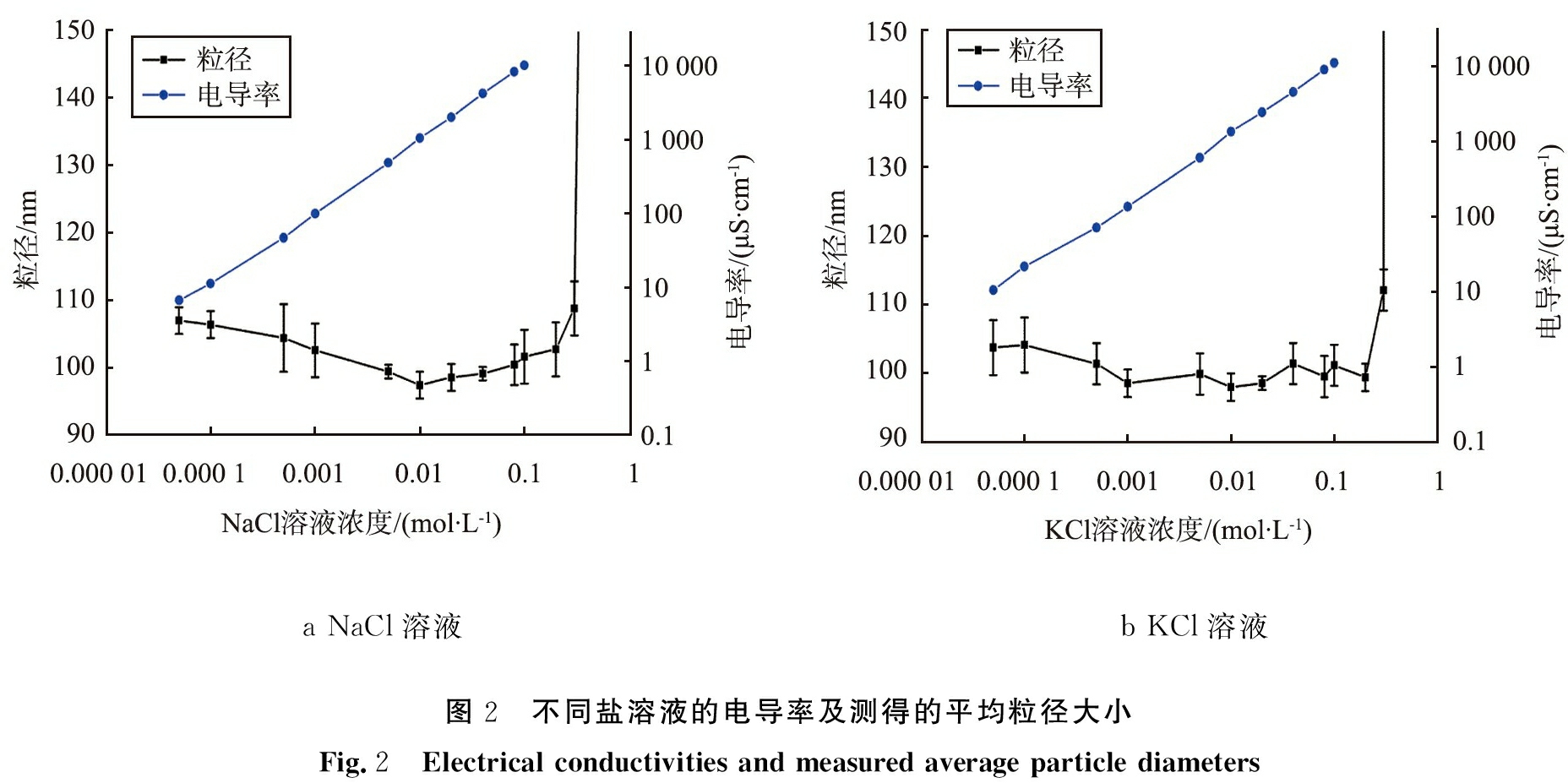
a NaCl溶液b KCl溶液图2 不同盐溶液的电导率及测得的平均粒径大小Fig.2 Electrical conductivities and measured average particle diameters
当溶液中加入少量的NaCl或KCl,由于NaCl与KCl是强电解质,在溶液中以离子形态存在,钠离子或钾离子又会与水分子形成水合离子,当盐浓度为5×10-5 mol/L时,离子会破坏或压缩水化膜,使得粒径测试结果减小,随着离子含量的增加,水化膜不断被压缩或破坏,直至水化膜几乎消失,此时所测得的平均粒径为粒子本身直径,故与粒子标称值相符。对比NaCl和KCl溶液压缩水化膜的过程来看,在相同浓度下,KCl溶液压缩水化膜能力比NaCl能力更强些。这是因为钠离子与水分子形成水合离子能力大于钾离子,虽然钾离子的半径大于钠离子的,但由于钠离子水合能力强,使得水合钠离子半径大于水合钾离子,致使KCl溶液的离子迁移率大于NaCl溶液,从电导率测试结果也可以看出相同浓度下,KCl溶液的电导率略大于NaCl溶液,因而KCl溶液相对于NaCl溶液更容易破坏或压缩粒子表面的水化膜。
随着盐含量的继续增加,粒子表面会形成稳定的双电子层,粒子之间的静电斥力不断减小,粒子间的相互作用力也随之不断增大,当盐浓度达到一定值时,粒子由于相互作用力而团聚,使得测得的平均粒径急剧增大。
图3为电导率、离子浓度与平均粒径的关系图。
从图3a中可知,UP水、蒸馏水及RO水的电导率很小,粒径测试结果偏大,对于矿泉水,其中含有相对较多的离子,而在这些离子中,2价离子如钙离子、镁离子等占比较大,而2价离子水合作用很小,从而更易压缩或破坏水化膜,故矿泉水的电导率虽然只有40.4 μS·cm-1,其粒径测量值却更接近标称值。
综上所述,少量盐的加入可以有效破除或压缩粒子表面水化膜。在有证标准样品的标称值内(本文中为(100±3) nm),对于氯化钾或氯化钠溶液,浓度选择范围比较大,即0.001~0.1 mol/L,甚至更大都可以,电导率处于100~10 000 μS·cm-1。从图3也可以看出,盐浓度为0.01 mol/L(电导率为1 000 μS·cm-1左右)处时,测得的平均粒径最小,所以在粒度仪器监控时,可以优先选用浓度为0.01 mol/L的氯化钠或氯化钾溶液。
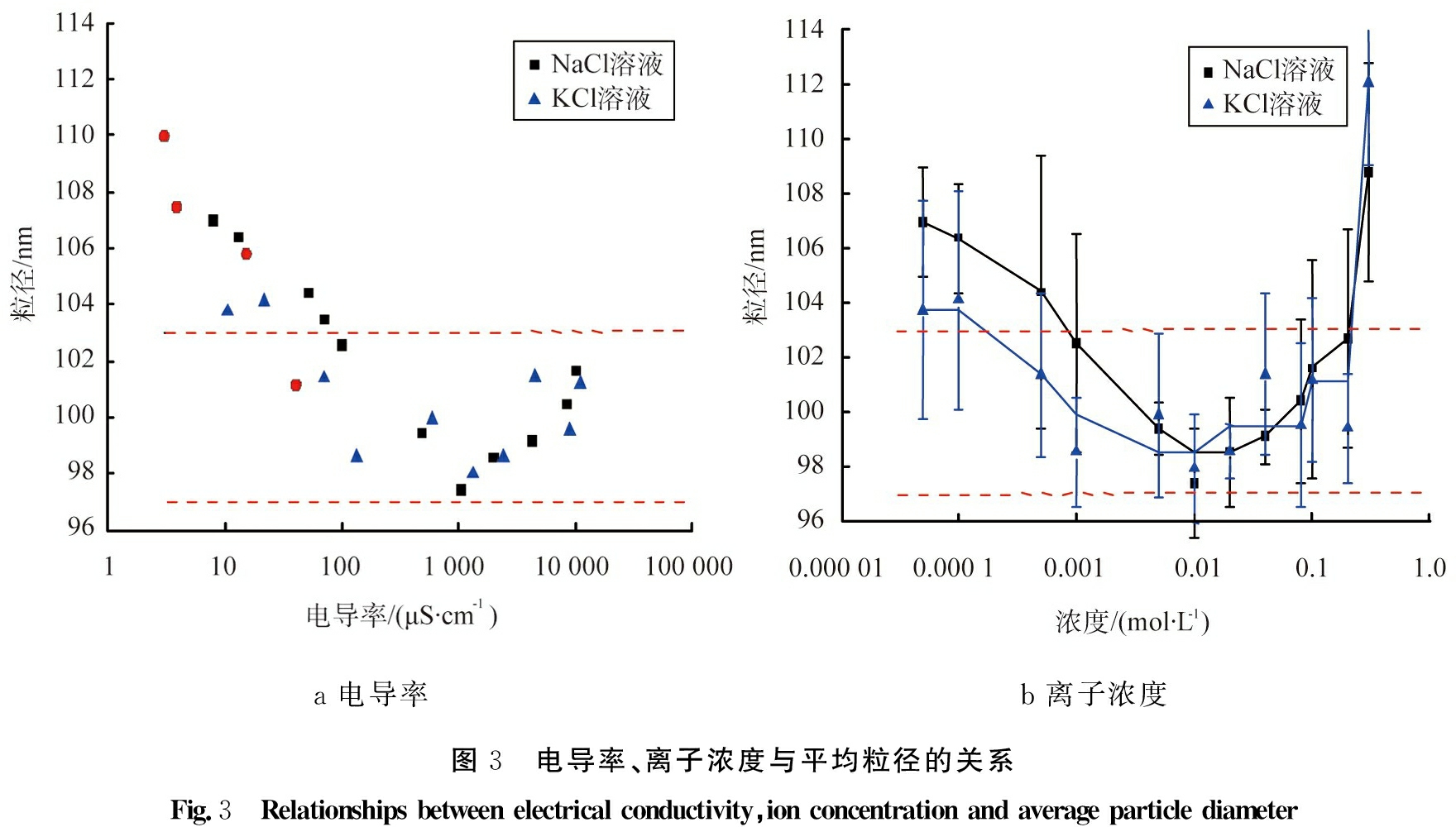
a 电导率b 离子浓度图3 电导率、离子浓度与平均粒径的关系Fig.3 Relationships between electrical conductivity,ion concentration and average particle diameter
2.3 不同测试方法的粒径测试
为了排除测试方法因素,选取上述测试结果最理想的分散介质矿泉水,重新配制稀溶液,分别对该溶液选用AC法及CC法进行测试,测试结果见表3。
表3 AC和CC法测得的聚苯乙烯微球分散在矿泉水溶液中的平均粒径统计表
Tab.3 Statistical table of average particle sizes of polystyrene microspheres dispersed in mineral water solution by AC and CC methods nm
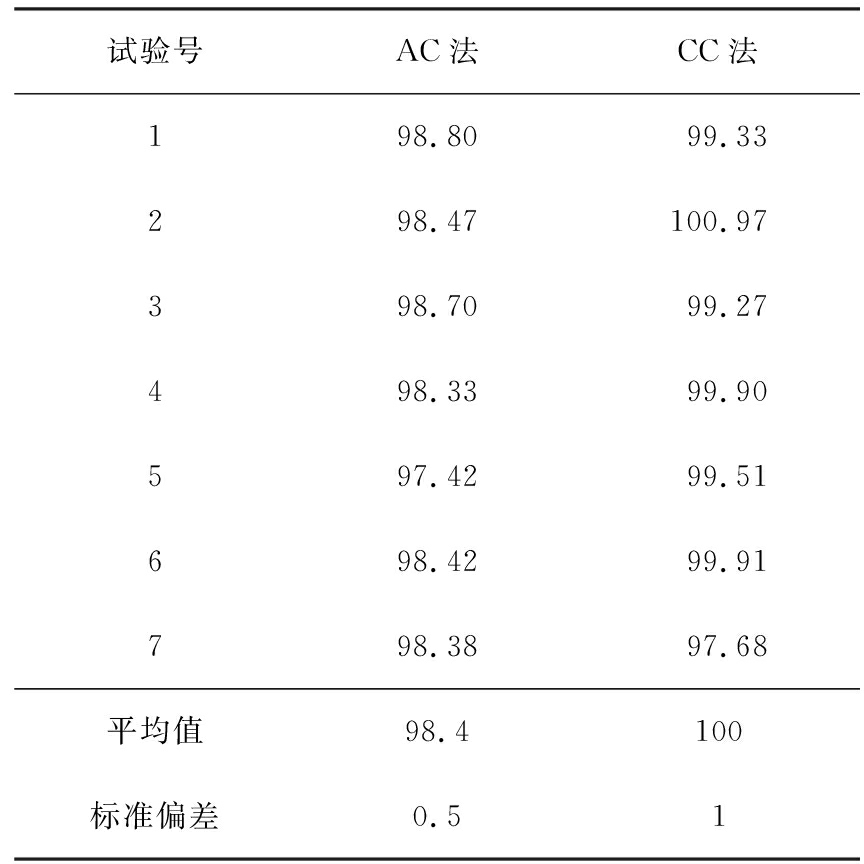
试验号AC法CC法198.8099.33298.47100.97398.7099.27498.3399.90597.4299.51698.4299.91798.3897.68平均值98.4100标准偏差0.51
2种方法测得的平均粒径分别为(98.4±0.5)、(100±1) nm,与标准粒子误差分别为2%和0。实验表明,相对来说,AC法由于多重散射的原因,结果略微偏小,但其影响不大,而且矿泉水测得结果都与标准物质证书中所给的值接近。对于另外3种水样也进行测试,其测试结论一致,其AC法测得的结果与CC法相当。
测试方法对聚苯乙烯微球的平均粒径影响比较小,排除测试方法因素,进一步说明盐含量在影响粒径测试中占主导作用。
3 结 论
1)对于聚苯乙烯微球分散介质体系,随着离子浓度的增加,粒径测量值先减小后增大。
2)在超纯水即离子浓度很低的溶液中,聚苯乙烯微球表面会形成一定厚度的水化膜,使粒径测量值大于粒子标称值;而少量离子的加入可以有效破除或压缩粒子表面水化膜,使得粒径测量值接近粒子标称值,从而提高平均粒径测量准确性;但随着离子浓度的不断增加,聚苯乙烯微球会随着粒子间相互作用力减小而团聚,使得测得的粒径急剧增大。
3)聚苯乙烯微球粒径在测试范围内,浓度为0.01 mol/L的氯化钠或氯化钾水溶液是最佳分散介质。
[1]XU R. Particle characterization: light scattering methods[M]. Dordrecht: Kluwer Academic Publishers, 2000: 397.
[2]GOKE K, ROESE E, ARNOLD A, et al. Control over particle size distribution by autoclaving poloxamer-stabilized trimyristin nanodispersions[J]. Molecular Pharmaceutics, 2016, 13(9): 3187-3195.
[3]BULAYCHENKO A I, POPOVETSKIV P S. Structure of adsorption layer of silver nanoparticles in sodium bis(2-ethylhexyl) sulfosuccinate solutions in n-decane as observed by photon-correlation spectroscopy and nonaqueous electrophoresis[J]. Langmuir, 2014, 30(43): 12729-12735.
[4]全国筛网筛分和颗粒分检方法标准化技术委员会.粒度分析:光子相关光谱法:GB/T 19627—2005[S]. 北京:中国标准出版社,2005.
[5]全国颗粒表征与分检及筛网标准化技术委员会.粒度分析:动态光散射法(DLS):GB/T 29022—2012[S]. 北京:中国标准出版社,2012.
[6]上海市计量测试技术研究院.光子相关光谱法粒度分析仪标准规范:JJF(沪)4—2006[S]. 上海:上海市质量技术监督局,2006.
[7]杨瑞娟,姜绪宝,朱晓丽. 单分散聚合物微球的制备及应用[J]. 山东化工,2017,42(6): 21-22.
[8]CHOLLAKUP R, SMITTHIPONG W, CHWOROS A. DNA-functionalized polystyrene particles and their controlled self-assembly[J]. RSC Advances, 2014, 4: 30648-30653.
[9]LIU B, FU Z, HAN Y, et al. Facile synthesis of large sized and monodispersed polymer particles using particle coagulation mechanism: an overview[J]. Colloid and Polymer Science, 2017, 295(5):749-757.
[10]ISRAELACHVILI J. Intermolecular and surface forces[M]. 3rd ed. Pittsburgh: Academic Press, 2011: 706.
[11]CHURAEV N V. Surface forces in wetting flotation and capillary phenomena[J]. Program in Colloid and Polymer Science, 1996, 101:45-50.
[12]MANCIU M, RUCKENSTEIN E. The polarization model for hydration/double layer interactions: the role of the electrolyte ions[J]. Advances in Colloid and Interface Science, 2004, 112: 109-128.
[13]MIN F F, PENG C L, LIU L Y. Investigation on hydration layers of fine clay mineral particles in different electrolyte aqueous solutions[J]. Powder Technology, 2015, 283: 368-372.
[14]DAHANAYAKE J N, MITCHELL-KOCH K R. Entropy connects water structure and dynamics in protein hydration layer[J]. Physical Chemistry Chemical Physics, 2018, 20: 14765-14777.
[15]吴伦. 基于原子力显微镜的煤粒表面水化膜和颗粒间相互作用力研究[D]. 徐州:中国矿业大学,2015.
[16]ISRAELACHVILI J, WENNERSTORM H. Role of hydration and water structure in biological and colloidal interactions[J]. Nature, 1996, 376: 219-224.