凡是以中医药理论为指导,用于防病治病的药物统称为中药,主要包括植物药、动物药和矿物药,其中绝大多数是植物药,占中药总数的85%以上[1]。植物细胞壁是阻碍有效成分吸收的最大障碍,研究可用于细胞破壁的中药制剂新技术对于提高中药的质量和生物利用度,降低药用资源的消耗和浪费,提升中药形象和促进中药现代化都具有十分重要的实际意义和应用价值[2]。
中药破壁饮片是将符合2015版《中国药典》要求并具有细胞结构的中药饮片,经现代破壁粉碎技术加工至d90<45 μm的粉体,经过无添加成型剂技术制成颗粒状饮片[3]。植物细胞经破壁后,细胞内的有效成分充分暴露,药物的释放速度及释放量会大幅提高[4]。与传统中药饮片比较,中药破壁饮片经过破壁粉碎之后,药效明显优于普通粗粉和传统饮片[5-7],药物利用率提高,减少资源浪费[8]。中药破壁粉作为其中间产品,粉体的各类性质(如粒径分布[9-10]、流动性[11]、比表面积[12])将影响最终产品中药破壁饮片的质量,影响最终产品的溶出、稳定性及吸收过程,甚至影响其他化学性质及临床疗效[13-14]。其中粒径是粉体的关键指标,研究表明随着粒径的减小,比表面积增大,粉体流动性稍有降低,吸湿性稍有增加,收率降低,有效成分溶出速率、溶出量以及相对累积溶出比率增加[15],所以对其粒径、流动性、比表面积等粉体性质的测定及控制具有重要意义。
本研究中以黄芪破壁粉为研究对象,制备10批次黄芪破壁粉,研究10批次黄芪破壁粉粉体学综合性质,为最终产品破壁饮片质量的控制提供参考。
1 实验
1.1 仪器设备及材料
D24UV型明澈超纯水机(美国Milipore公司);TC-30型流化床超音速气流粉碎分级机(江苏省南京龙立天目超微粉体技术有限公司);BT-1000粉体综合特性测试仪(丹东市百特仪器有限公司);MS105型电子分析天平(瑞士Mettler Toledo公司);CM-5型分光测色计(日本KONICA MINOLTA公司);3H-2000PS2型静态容量法比表面及孔径分析仪(贝士德仪器科技(北京)有限公司);KQ-400KOE型超声波清洗器(昆山市超声仪器有限公司);TopSizer激光粒度分析仪(珠海欧美克仪器有限公司)。
黄芪原药材,购自甘肃岷县顺兴和中药材有限公司,经广东省中山市中智药业集团有限公司贾世清中药师鉴定为豆科植物蒙古黄芪(Astragalus membranaceus (Fisch.)Bge.var.mongholicus(Bge.)Hsiao)的干燥根。由中山市中智药业集团有限公司加工制备成10批黄芪破壁粉,批号分别为20170601—20170610。
1.2 方法
1.2.1 粒径分布方法考察
1)最佳参数确定
分别称取黄芪破壁粉50、80、120、150 mg,加入蒸馏水50 mL,超声时间为5 min,超声频率为80%(560 W;40 kHz),利用激光粒度测定仪(遮光比设置为8%、循环水泵泵速2 000 r/min)测试样品粒径,以确定最佳样品量。
取黄芪破壁粉80 mg,分别设置不同超声时间为5、10、15、20 min,其他条件不变,以确定最佳时间。
设置不同泵速为2 000、2 500、3 000 r/min,其他条件不变,以确定最佳循环泵速。
设置超声仪器不同超声频率40%(280 W; 40 kHz)、60%(420 W; 40 kHz)、80%(560 W; 40 kHz),其他条件不变,以确定最佳超声频率。
设置激光粒径仪的遮光比分别设置为4%、8%、12%,其他条件不变,以确定最佳遮光比。
2)重复性考察
取批号为20170601的供试品黄芪破壁粉,按照筛选出的最佳测定参数,连续测定6次,分析粒径测定结果的RSD值。
1.2.2 堆密度测定方法考察
先称量密度容器质量m0,然后在粉体综合性质测试仪的振动筛上加料,至充满密度容器后停止加料,用刮板将多余粉体刮出,测质量m,堆密度以下式计算:
ρa=(m-m0)/100 。
同一批黄芪破壁粉体供试品,平行制备6份,按照上述方法测定,分析测定结果的RSD值。
1.2.3 比表面积测定方法考察
采用比表面积仪测定黄芪破壁粉体比表面积。考察比表面积仪不同分析参数对测定结果的影响,筛选最佳分析条件,建立黄芪破壁粉体的比表面积测定方法并进行方法学考察。
1)参数确定。分别取1 000、1 500、1 800、2 000 mg黄芪破壁粉样品,采用比表面仪测定其比表面积,脱气温度为60 ℃,脱气时间为8 h,考察不同样品量。
取黄芪破壁粉1 500 mg,平行8份,分为4组,脱气8 h,其他条件不变,设置脱气温度为40、60、80、100 ℃,考察不同脱气温度。
设置脱气时间为4、6、8、10 h,其他条件不变,考察不同脱气时间。
2)重复性考察。按照筛选出测定参数,重复6次测定黄芪破壁粉比表面积,计算6组数据的RSD值。
1.2.4 休止角测定方法学考察
打开振动筛开关,在振动筛上加料至样品落满试验台并呈对称的圆锥体后停止加料,使用测角器在3个不同位置测定休止角,取平均值,即为该样品的休止角θr。同一批试样,平行取6份,按照上述方法测定休止角,分析测定结果的RSD值。
1.2.5 色度测定方法学考察
取黄芪破壁粉,填满2/3样品皿,直接读取分光测色仪显示色度值(L*值、a*值、b*值)。取同一批黄芪破壁粉6份,分别测定6次,计算RSD值,得出重复性和精密度考察结果。
2 结果与分析
2.1 粒径分布方法学考察结果
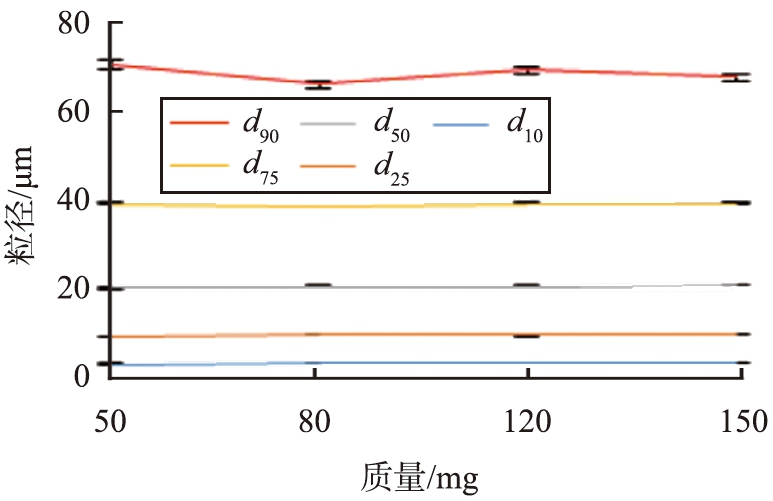
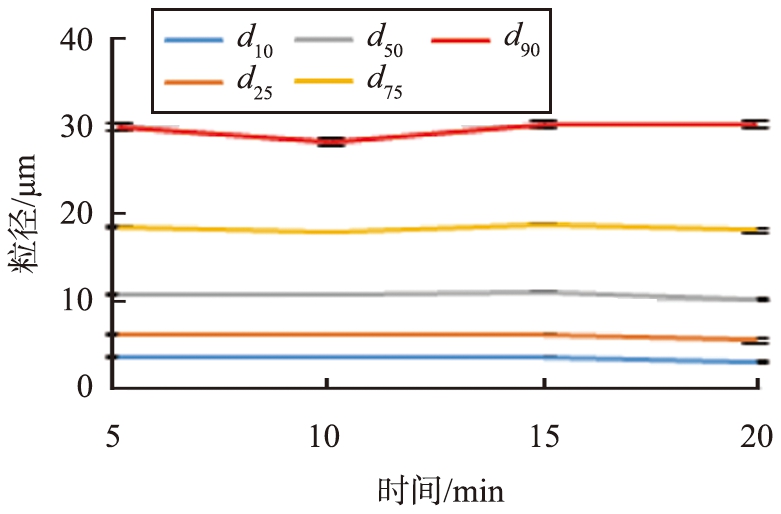
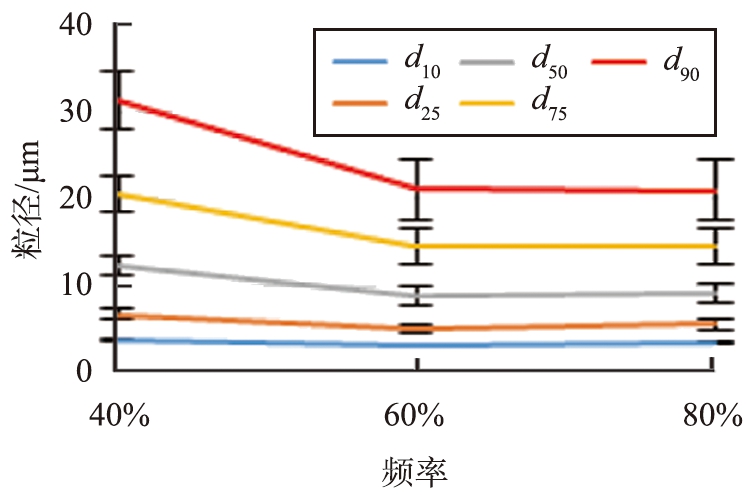
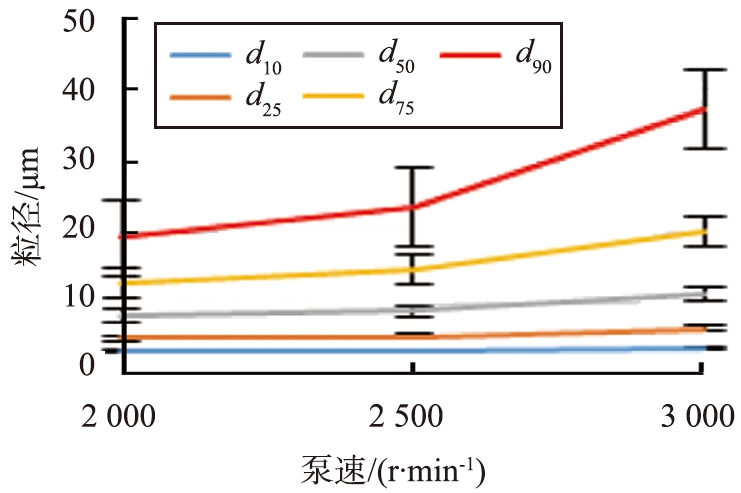
图1为粒径分布方法学考察影响因素的结果。由图可知,样品量为80 mg、超声时间为5 min、超声频率为80%时,样品分散完全且测定数据较稳定。随着循环泵泵速的提高,粒径增大,遮光比为8%时实验数据稳定。
最终选择的分析条件为:破壁粉为80 mg,以80%功率超声处理5 min,激光粒度测定仪遮光比为8%,循环水泵泵速为2 000 r/min。
考察结果见表1。方法及方法学考察显示,其重复性较好,可以用于黄芪破壁粉粒径测定。粒径测定结果见表2。
a 样品量
b 超声时间
c 超声频率
d 循环泵速
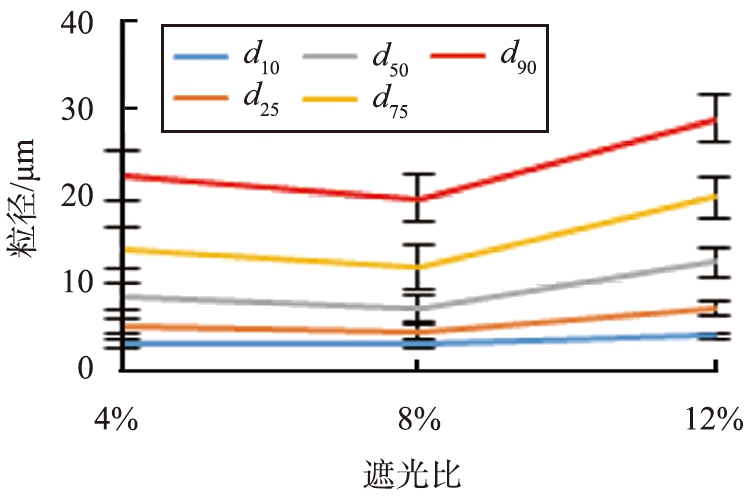
e 遮光比
图1 黄芪破壁粉粒径分布测定方法考察结果
Fig.1 Determination method for particle size distribution of ultrafine powder of Radix astragali
2.2 堆密度测定
黄芪破壁粉堆密度重复性考察结果见表3,RSD值为1.40%,说明测定方法重复性良好,可用于黄芪破壁粉堆密度测定。
堆密度的测定结果见表4,其中平均值±SD值为0.22±0.05。
表1 黄芪破壁粉粒径分布重复性考察
Tab.1 Repetitive investigation of particle size distribution of Radix astragali μm
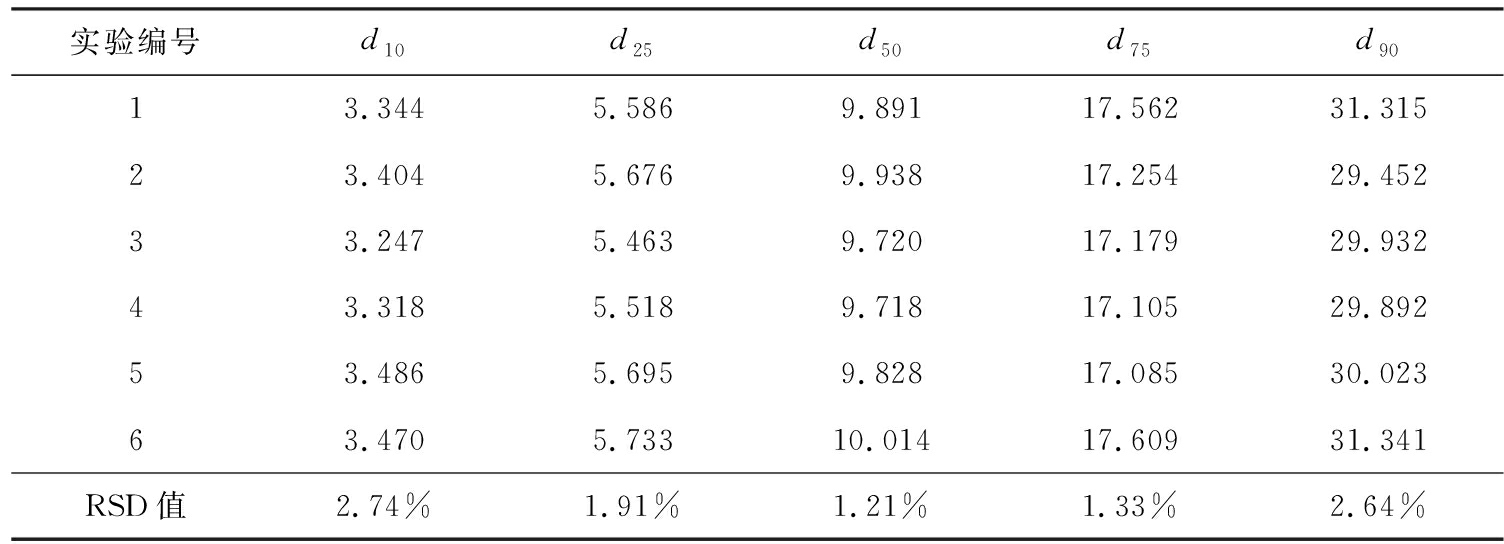
实验编号d10d25d50d75d9013.3445.5869.89117.56231.31523.4045.6769.93817.25429.45233.2475.4639.72017.17929.93243.3185.5189.71817.10529.89253.4865.6959.82817.08530.02363.4705.73310.01417.60931.341RSD值2.74%1.91%1.21%1.33%2.64%
表2 黄芪破壁粉粒径分布
Tab.2 Particle size distribution of ultrafine powder of Radix astragali μm
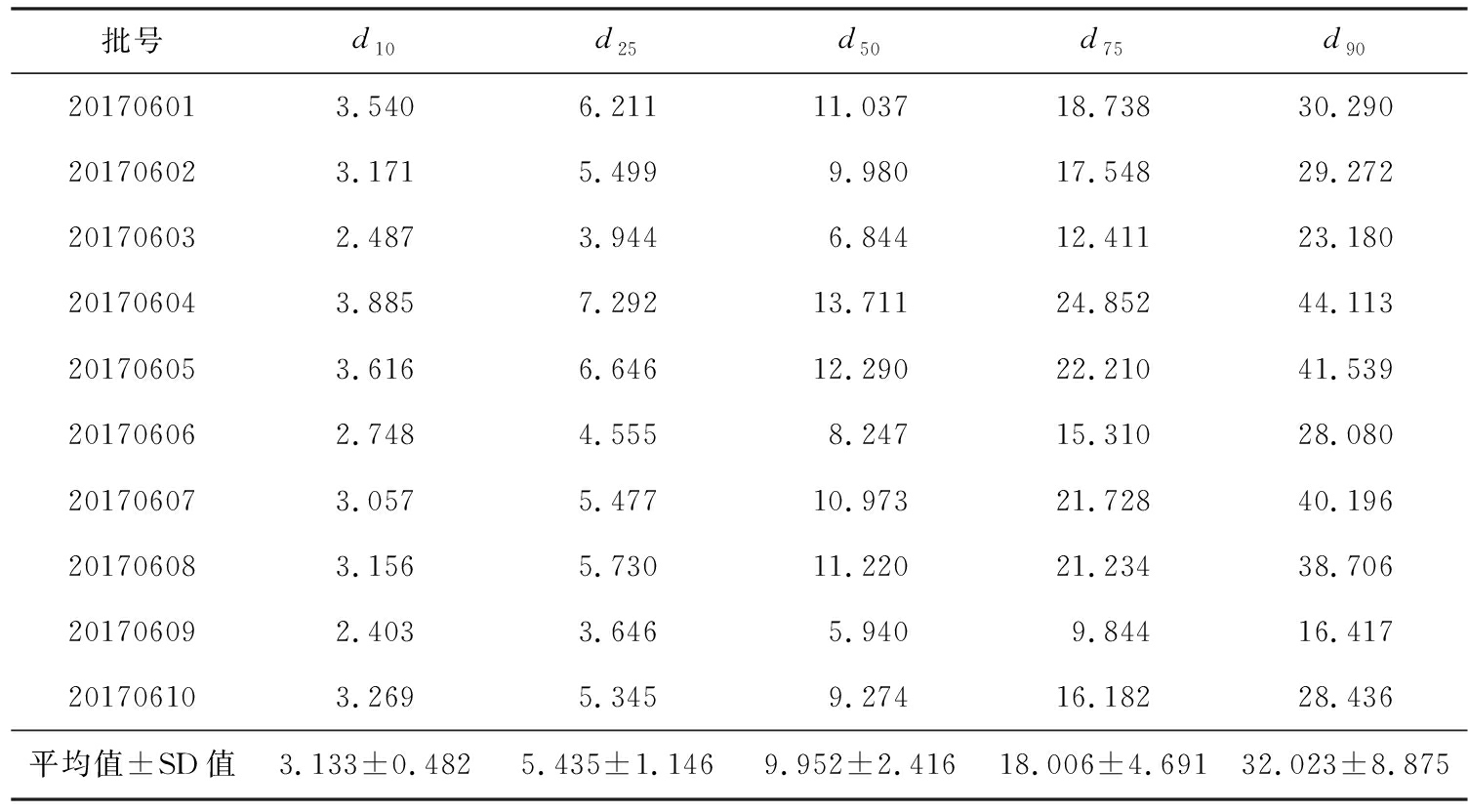
批号d10d25d50d75d90201706013.5406.21111.03718.73830.290201706023.1715.4999.98017.54829.272201706032.4873.9446.84412.41123.180201706043.8857.29213.71124.85244.113201706053.6166.64612.29022.21041.539201706062.7484.5558.24715.31028.080201706073.0575.47710.97321.72840.196201706083.1565.73011.22021.23438.706201706092.4033.6465.9409.84416.417201706103.2695.3459.27416.18228.436平均值±SD值3.133±0.4825.435±1.1469.952±2.41618.006±4.69132.023±8.875
表3 黄芪破壁粉堆密度重复性考察
Tab.3 Repeatability investigation of bulk density determination of ultrafine powder of Radix astragali

实验编号容器质量/g装样总质量/g堆密度/(g·cm-3)1407.450427.7900.2032407.450427.0500.1963407.450427.5500.2014407.450427.8500.2045407.450427.4800.2006407.450427.4700.200
2.3 比表面积测定
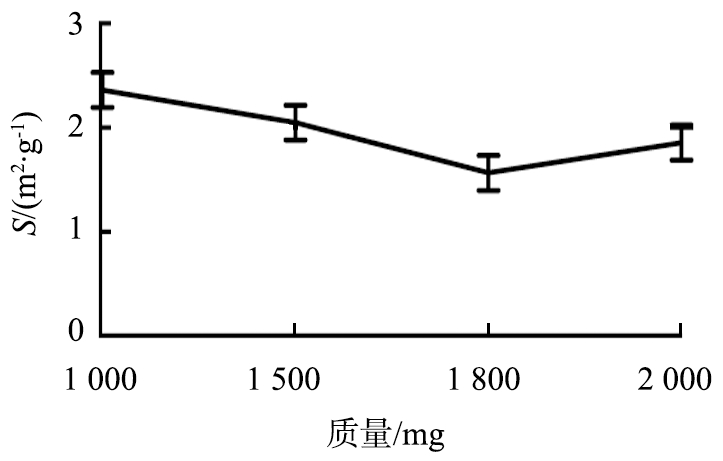
黄芪破壁粉在不同条件下比表面积测定的结果见图2。由图2a可知,1 000增加到1 800 mg的破壁粉的比表面积呈下降趋势,但由平行测定结果所得,在1 500 mg所测得黄芪破壁饮片比表面积测定平行测量数据重复性较好,所以样品量选择1 500 mg。
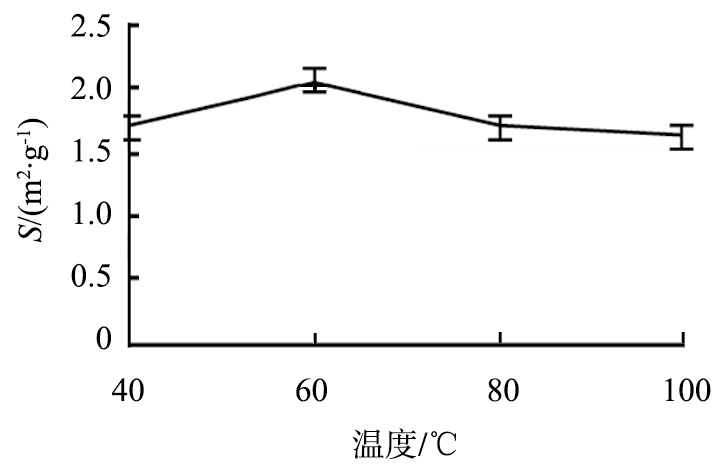
由图2b可知,60 ℃测得的比表面积最大,由平行试验可得60 ℃所测得黄芪破壁饮片比表面积测定平行测量数据重复性较好,故选择60 ℃作为脱气温度。
表4 黄芪破壁粉体堆密度测定
Tab.4 Density measurement of ultrafine powders of Radix astragali
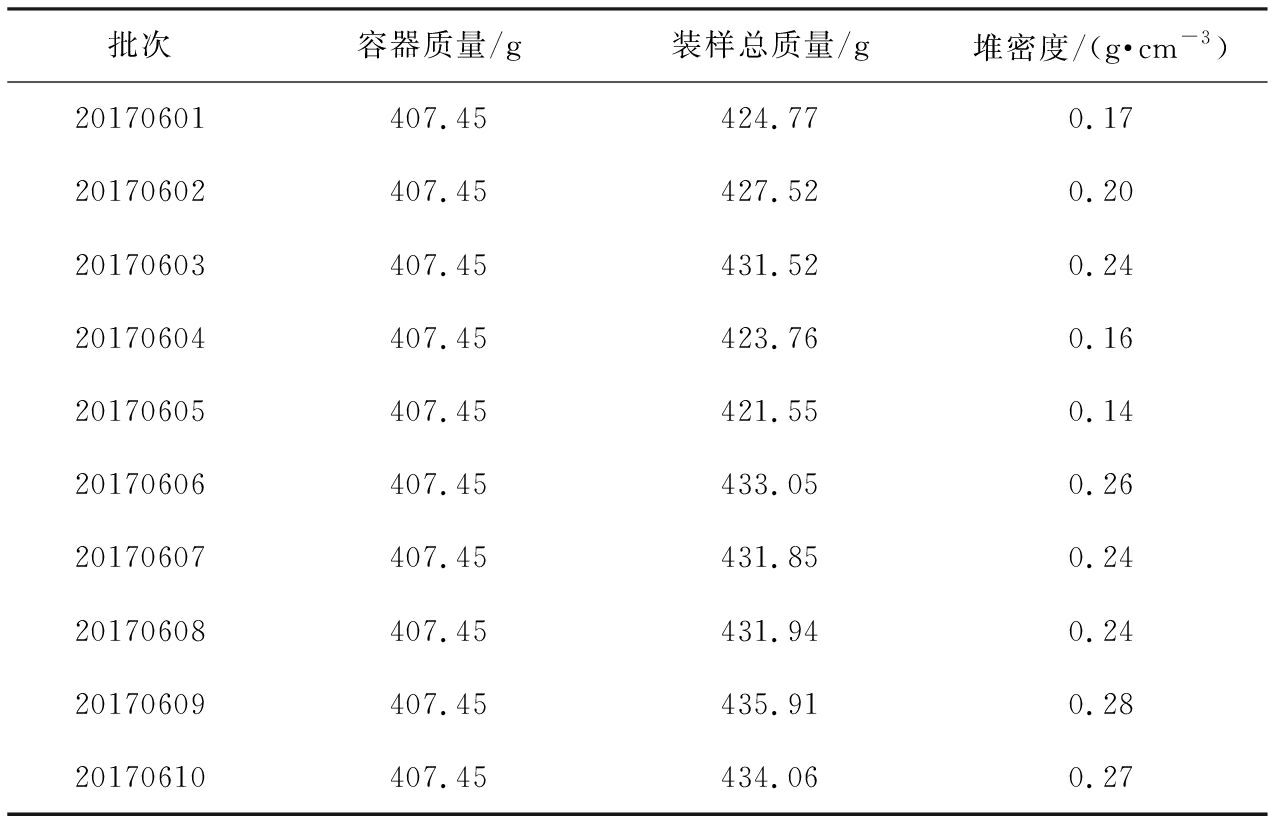
批次容器质量/g装样总质量/g堆密度/(g·cm-3)20170601407.45424.770.1720170602407.45427.520.2020170603407.45431.520.2420170604407.45423.760.1620170605407.45421.550.1420170606407.45433.050.2620170607407.45431.850.2420170608407.45431.940.2420170609407.45435.910.2820170610407.45434.060.27
a 取样量
b 脱气温度
c 脱气时间
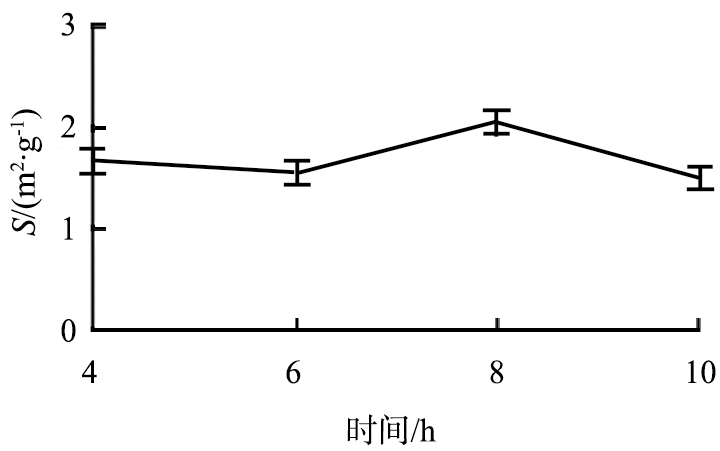
图2 黄芪破壁粉在不同条件下比表面积变化
Fig.2 Changes in specific surface area under different conditions of ultrafine powder of Radix astragali
由图2c可知,脱气时间为8 h所测得黄芪破壁饮片比表面积最大同时测定平行测量数据重复性较好,所以选择8 h作为脱气时间。
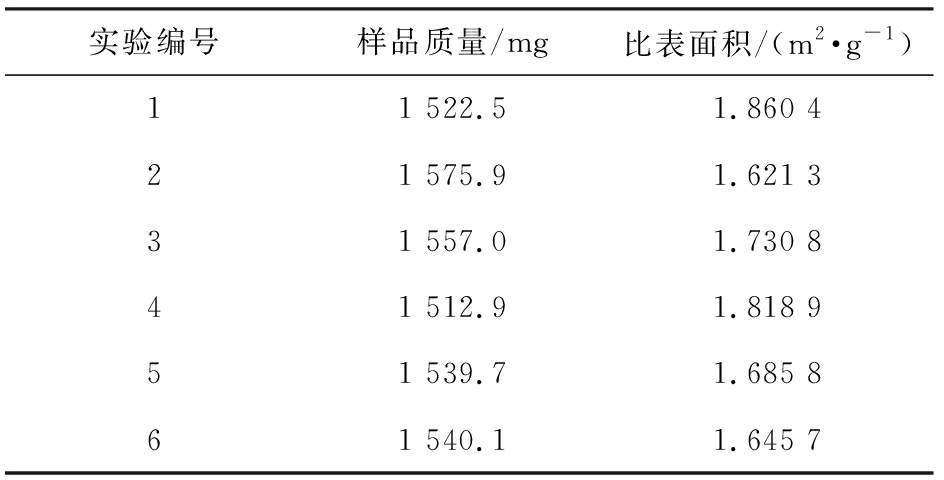
黄芪破壁粉比表面积重复性考察结果见表5。由表可见,测得黄芪破壁粉比表面积的RSD值分别为5.537%,重现性较好,可用于黄芪破壁粉比表面积的测定。
表5 比表面积重复性考察
Tab.5 Results of specific surface area repeatability
实验编号样品质量/mg比表面积/(m2·g-1)11 522.51.860 421 575.91.621 331 557.01.730 841 512.91.818 951 539.71.685 861 540.11.645 7
按照上述筛选出的取样量1 500 mg、60 ℃脱气8 h方法,测定10批次黄芪破壁粉比表面积,结果见表6。
2.4 休止角测定
重复性考察结果见表7,其中平均值为51.33 °,RSD为3.65%。由表可以看出,RSD<5%,说明重复性良好,可用于黄芪破壁粉休止角的测定。黄芪破壁粉休止角测定结果见表8。平均值±SD值为48.87±2.88。
2.5 色度测定
用色差计对各样品进行颜色测定,记录其L*值、a*值、b*值。根据公式计算![]()
(1)
式中:![]() 为总色值;L*为亮度;a*和b*为色度坐标;+a*表示红方向、-a*表示绿方向、+b*表示黄方向、-b*表示蓝方向,分别计算得出的各样品的总色值。
为总色值;L*为亮度;a*和b*为色度坐标;+a*表示红方向、-a*表示绿方向、+b*表示黄方向、-b*表示蓝方向,分别计算得出的各样品的总色值。
表6 黄芪破壁粉比表面积测定
Tab.6 Determination of specific surface area of Radix astragali
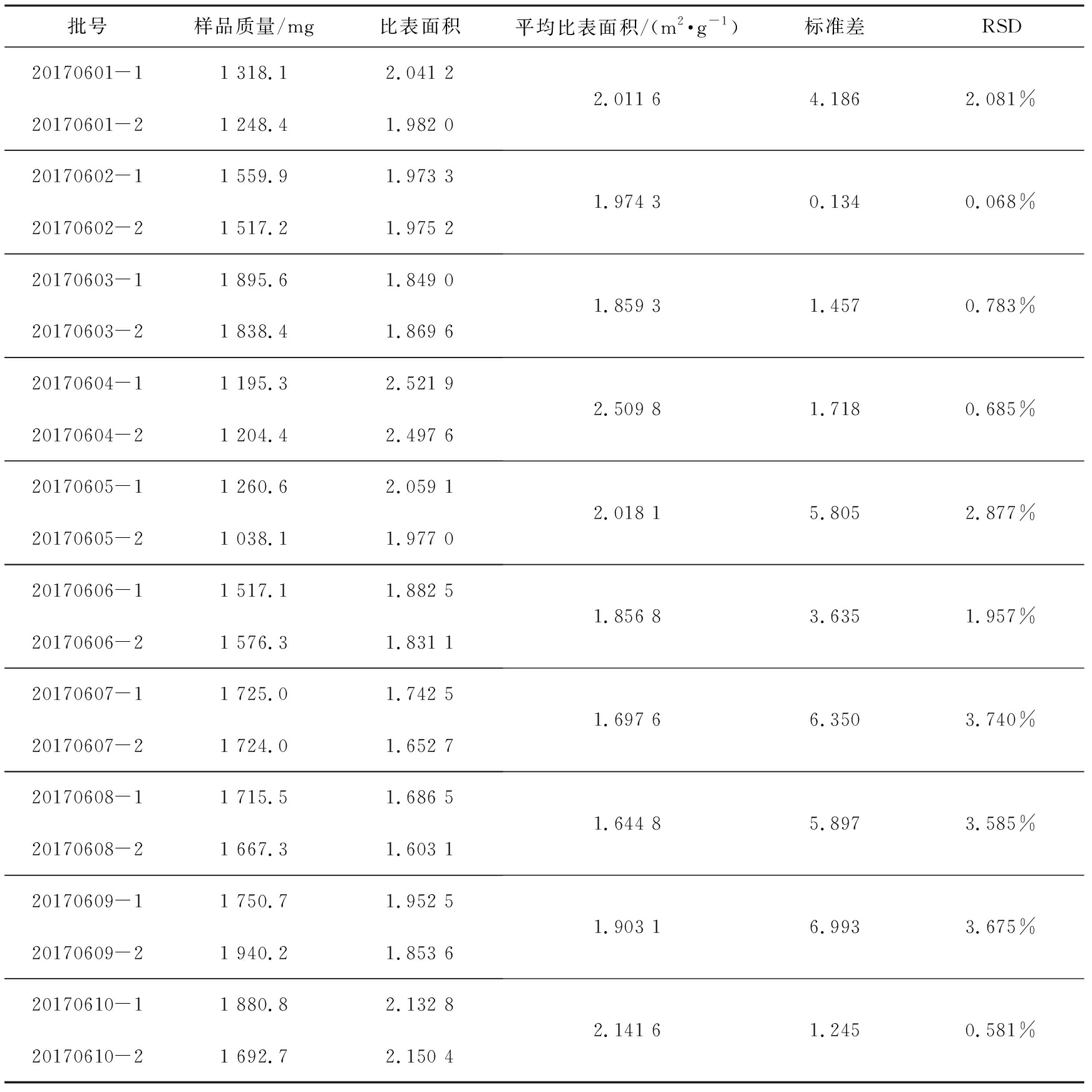
批号样品质量/mg比表面积平均比表面积/(m2·g-1)标准差RSD20170601-11 318.12.041 220170601-21 248.41.982 02.011 64.1862.081%20170602-11 559.91.973 320170602-21 517.21.975 21.974 30.1340.068%20170603-11 895.61.849 020170603-21 838.4 1.869 61.859 31.4570.783%20170604-11 195.32.521 920170604-21 204.42.497 62.509 81.7180.685%20170605-11 260.62.059 120170605-21 038.11.977 02.018 15.8052.877%20170606-11 517.11.882 520170606-21 576.31.831 11.856 83.6351.957%20170607-11 725.01.742 520170607-21 724.01.652 71.697 66.3503.740%20170608-11 715.51.686 520170608-21 667.31.603 11.644 85.8973.585%20170609-11 750.71.952 520170609-21 940.21.853 61.903 16.9933.675%20170610-11 880.82.132 820170610-21 692.72.150 42.141 61.2450.581%
表7 黄芪破壁粉休止角重复性考察
Tab.7 Repeated investigation of angle of repose of ultrafine powder of Radix astragali (°)
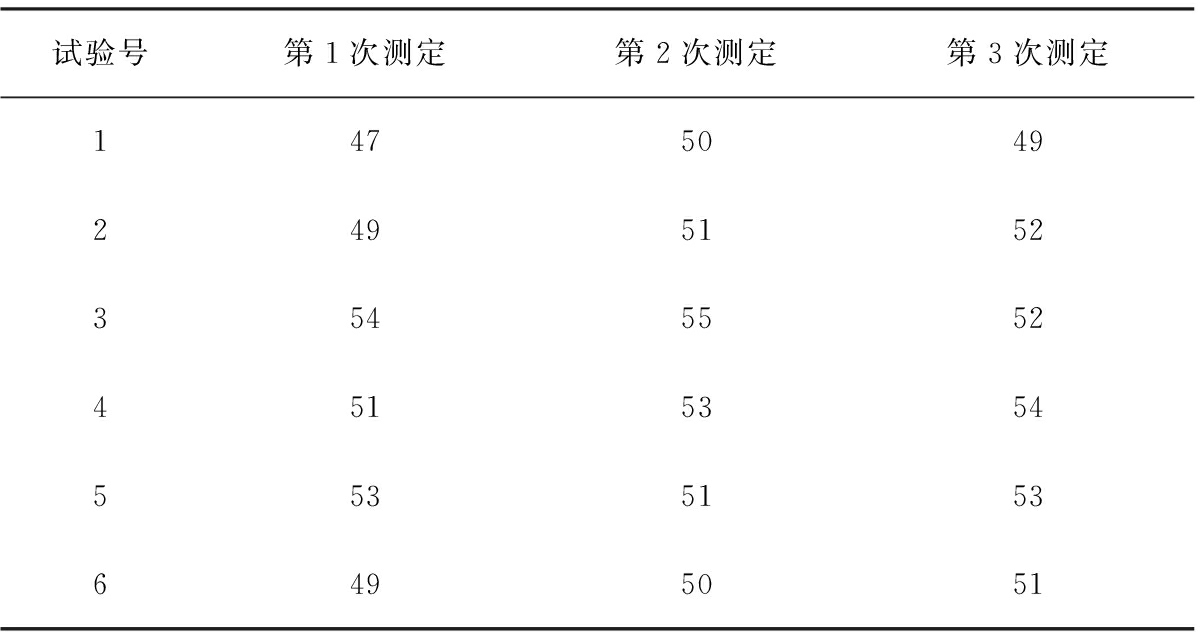
试验号第1次测定第2次测定第3次测定147504924951523545552451535455351536495051
黄芪破壁粉色度测定重复性及精密度考察结果见表9—10。从表9—10可知,![]() 的RSD值<1%,表现出较好颜色均一性,可进行色度测定。色度测定的结果见表11。
的RSD值<1%,表现出较好颜色均一性,可进行色度测定。色度测定的结果见表11。
表8 黄芪破壁粉休止角测定
Tab.8 Angle of ultrafine powder of Radix astragali
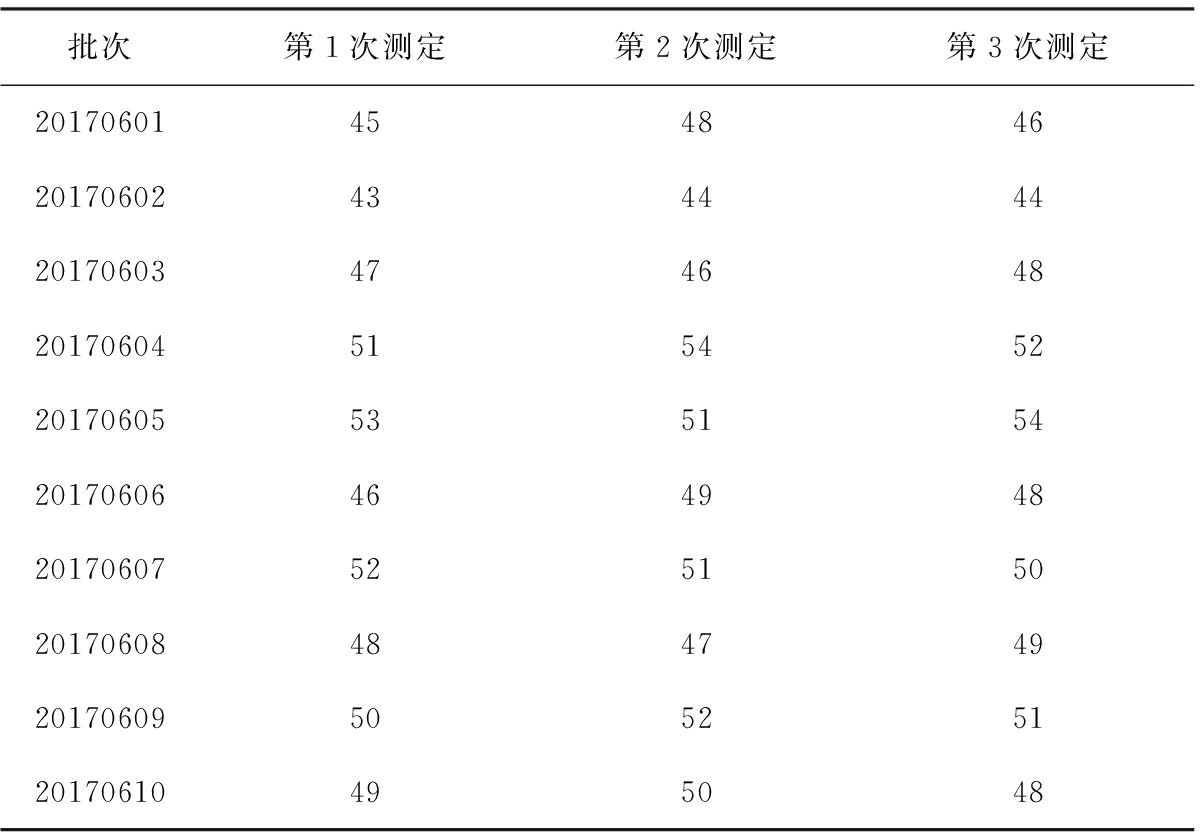
批次第1次测定第2次测定第3次测定20170601454846201706024344442017060347464820170604515452201706055351542017060646494820170607525150201706084847492017060950525120170610495048
表9 黄芪破壁粉色度测定重复性考察
Tab.9 Chromatic repeatability study of ultrafine powder of Radix astragali
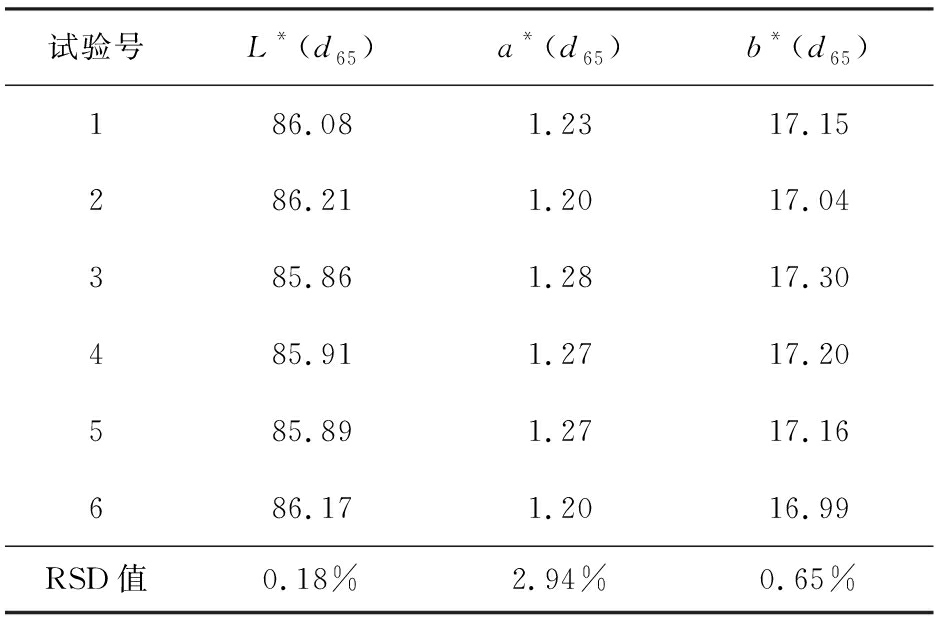
试验号L*(d65)a*(d65)b*(d65)186.081.2317.15286.211.2017.04385.861.2817.30485.911.2717.20585.891.2717.16686.171.2016.99RSD值0.18%2.94%0.65%
表10 黄芪破壁粉色度测定精密度考察结果
Tab.10 Chromatic measurement precision inspection results of ultrafine powder of Radix astragali
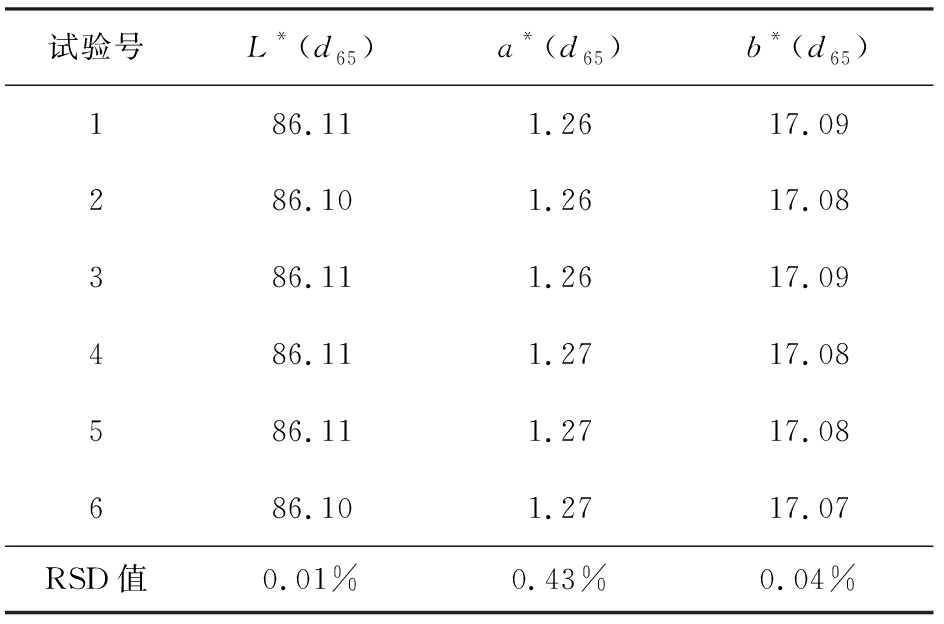
试验号L*(d65)a*(d65)b*(d65)186.111.2617.09286.101.2617.08386.111.2617.09486.111.2717.08586.111.2717.08686.101.2717.07RSD值0.01%0.43%0.04%
表11 黄芪破壁粉色度测定
Tab.11 Chromatic measurement of ultrafine powder of Radix astragali

批号L*(d65)a*(d65)b*(d65)E*ab20170601-187.120.6517.5788.8820170601-287.120.6617.5688.8720170602-285.350.9917.9587.2220170602-385.351.0117.9587.2220170603-286.111.2517.0987.8020170603-386.111.2517.1087.8020170604-287.680.2417.9989.5120170604-387.680.2617.9789.5020170605-186.900.4717.9888.7420170605-286.910.4817.9688.7520170606-187.810.4516.7589.3920170606-287.800.4716.7489.3820170607-187.860.1517.4489.5720170607-287.860.1817.4189.5720170608-187.530.2116.9789.1620170608-287.520.2216.9589.1520170609-187.320.6516.1288.8020170609-287.320.6616.1188.8020170610-187.340.8515.9288.7820170610-287.340.8715.9188.78
3 结论
1)黄芪破壁粉的粒径分布、堆密度、休止角、比表面积、色度等各指标考察确定的测定方法可靠可行。
2)方法学考察结果显示各指标方法在测定范围内可行。10批次黄芪破壁粉的粒径远小于45 μm,说明10批次样品的粒径大小符合要求,可用于生产。每批次黄芪破壁粉之间的堆密度、休止角、色度和比表面积差异性不大,说明10批次黄芪破壁粉的粉体性质较稳定。
[1]王广基, 邹珊刚, 陈传宏. 中国医药科学技术战略与政策研究[M]. 北京: 中国医药科技出版社, 2002.
[2]孙文格. 中医药应用超微粉碎技术的研究进展[J]. 中国药业, 2009, 18(20): 80-82.
[3]成金乐, 赖智填, 彭丽华. 中药破壁饮片研究[J]. 世界科学技术-中医药现代化, 2014, 16(2): 254-262.
[4]王宏洁, 司南, 边宝林. 饮片超微粉碎前后主要有效成分溶出量的对比研究[J]. 中国中药杂志, 2004, 29(11): 1111-1112.
[5]蔡璐, 梁少瑜, 戴开金, 等. 人参破壁饮片与细粉的体外溶出度比较[J]. 南方医科大学报, 2013, 33(10): 1547-1550.
[6]熊慧, 郭舟, 赵静文, 等. 栀子破壁饮片与细粉中栀子苷的体外溶出度比较[J]. 中国实验方剂学杂志, 2013, 19(21): 53-55.
[7]李越峰, 徐富菊, 张泽国, 等. 当归破壁饮片与当归饮片质量比较研究[J]. 中国临床药理学杂志, 2014, 30(12): 1124-1126.
[8]李德成, 刘庆燕. 超微粉碎技术在中药制剂中广泛应用的优越性[J]. 世界中医药, 2011, 6(5): 454-455.
[9]金贞姬, 李兰, 刘李. 不同粒径高山红景天超微粉在大鼠体内的吸收[J]. 中国医院药学杂志, 2013, 33(4): 296-299.
[10]鹿丽丽, 萧伟, 徐连明, 等. 不同粒径三七粉物理性质及体外溶出度的比较研究[J]. 世界科学技术——中医药现代化, 2013, 15(2): 305-309.
[11]袁亮, 张建琴, 林婷婷, 等. 离心造粒法制备复方丹参微丸[J]. 中国实验方剂学杂志, 2010, 16(5): 10-14.
[12]化玮, 刘洋, 艾国, 等. 3种中药最细粉的制备及理化性质考察[J]. 中国药房, 2013, 44(23): 3296-3302.
[13]赵国巍, 梁新丽, 罗娟, 等. 超微粉碎对血竭、红花及其混合粉体性质的影响[J]. 中国医院药学杂志, 2016, 36(22): 1963-1968
[14]王念明, 张定堃, 杨明, 等. 超微粉碎对黄芩粉体学性质的影响[J]. 中药材, 2013, 36(4): 640-644.
[15]邓雯, 杨泽锐, 程翔燕, 等. 不同粒径黄芪超微粉理化性质的研究[J]. 中国现代中药, 2017, 19(8): 1187-1192.