纳米SiO2作为一种重要的无机材料,具有小尺寸效应和表面界面效应,同时具有高磁阻性和低热导性,在高分子材料中应用可提升耐用性和理化性能[1-4]。由于纳米SiO2表面富含羟基, 不能很好地分散在非极性的聚合物基材料中,因此,对其进行表面疏水改性具有重要意义[5-8]。
纳米SiO2的改性方法有很多种,例如机械混合法、 酯化法、表面活性剂法、硅烷偶联剂法[9]。其中硅烷偶联剂法操作便捷,性能稳定,它与无机纳米粒子之间除了范德华力、氢键等相互作用外,还有化学键等作用,对纳米材料的疏水改性卓有成效[10-11]。Zhou等[12]用溶胶-凝胶法合成了二氧化硅气凝胶,用三甲基氯硅烷作为改性剂,这种修饰使得二氧化硅的水接触角变大,红外光谱显示有Si—CH3键的振动,热重分析表明500 ℃时二氧化硅气凝胶在空气中稳定。武江红等[13]以正硅酸乙酯(TEOS)为原料采用溶胶-凝胶法制备了纳米二氧化硅悬浮液,分别用KH560和KH570改性后,纳米二氧化硅的分散性变好且疏水性明显增强。
偶联剂法虽然被普遍采用,但大部分研究利用偶联剂自身先水解再与纳米SiO2进行化学反应,水解过程中反应产物会发生自缩合,阻碍了水解产物与纳米粉体表面羟基的作用, 偶联效能降低[14], 因此亟待开辟新方法。针对以上问题,为了获得最佳疏水改性效果,最大程度减少颗粒团聚,本文中利用改进的Stöber法合成纳米SiO2,用有机溶剂置换醇水混合液,采用脱醇缩合原理,以γ-甲基丙烯酰氧基丙基三甲氧基硅烷(KH570)作为改性剂对其进行原位改性,进一步表征红外光谱、扫描电镜和粒度分布情况,优化改性工艺条件,评价产物疏水效果,得到了性能稳定、分散均匀、疏水性好的球状纳米SiO2,为其在聚合物基材料中的应用奠定了基础。
1 实验
1.1 仪器与试剂
主要仪器有Nicolet6700型傅立叶变换红外光谱仪、S-4800型冷场发射扫描电子显微镜、5810r型高速离心机、DZX-1型真空干燥箱、Mastersizer 2000激光粒度仪、DF-101S型集热式磁力搅拌水浴锅。
试剂包括正硅酸乙酯(AR)、氨水(AR)、无水乙醇(AR)、KH570(AR)、冰醋酸(AR)、pH试纸等。
1.2 步骤
利用改进的Stöber法合成纳米SiO2,用有机溶剂置换醇水混合液,采用脱醇缩合原理进行原位改性,向体系中逐滴滴加KH570,接通自来水并打开磁力搅拌,在一定温度下水浴反应数小时,反应完毕后高速离心分离,依次醇洗、水洗膏体数遍,真空干燥、研磨后得白色蓬松的改性纳米SiO2粉体,其化学反应过程示意图如图1所示。
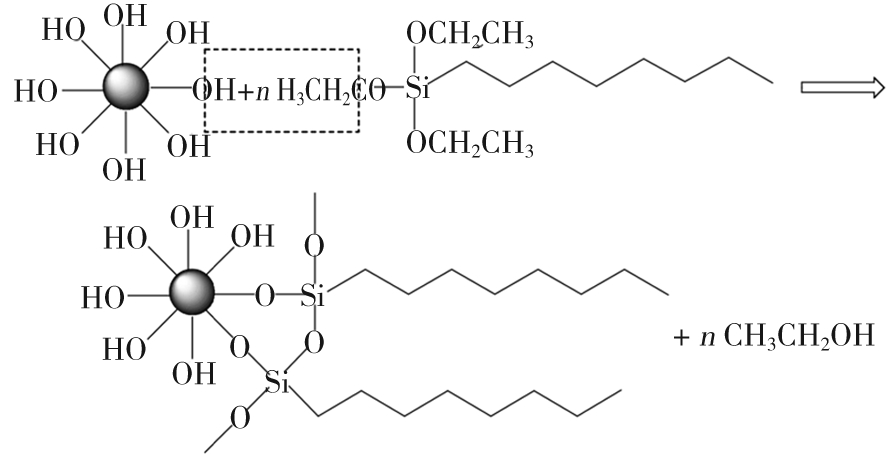
图1 硅烷偶联剂改性纳米SiO2示意图
Fig.1 Schematic diagram of modification of
nano-SiO2 by silane coupling agent
1.3 结构表征与性能测试
1.3.1 结构表征
采用KBr压片法对改性前后的纳米SiO2粉体进行红外光谱分析,扫描波数范围为4 000~400 cm-1;将改性前后的纳米SiO2进行洗涤、 固定、 脱水、 干燥及镀膜等处理之后, 用扫描电镜对其分散情况、 结构及其表面形貌进行表征; 将制取的改性纳米SiO2用乙醇稀释, 移取1 mL试样进行粒度分布测试。
1.3.2 亲油化度及吸水率计算
亲油化度计算: 量取25 mL去离子水置于烧杯中, 称取1 g上述改性纳米SiO2倒入水中, 用甲苯滴定至粉末完全浸润, 记录此时甲苯的体积为V(mL),则亲油化度表示为
(1)
式中:α为亲油化度,%;V为甲苯体积,mL。
吸水率计算:称取一定量的改性纳米SiO2,洒在干净的载玻片上,在粉末上逐滴滴加去离子水并搅拌,当粉末团聚时,吸走表面多余的水珠,记录团聚物的质量,则吸水率表示为
(2)
式中:τ为吸水率,%; m1为改性纳米SiO2粉末质量, g; m2为处理后团聚物的质量,g。
1.3.3 分散性测试
以水作极性溶剂, 以甲苯作非极性溶剂, 将改性纳米SiO2粉体超声分散于2种溶剂中, 观察分散状态。
1.3.4 沉降实验
向量筒中添加石蜡液至25 mL刻度,分别称取0.5 g未改性及改性纳米SiO2颗粒洒在石蜡液表面,记录颗粒在不同时刻从量筒中下降的体积。
1.3.5 润湿性测试
用压片机将改性前后的纳米SiO2粉末压成圆片,用精密针管移取5~10 μL水,记录水滴在圆片表面稳定时所形成的角度作为该点的接触角。重复测试,取10个座滴的接触角平均值作为水在该固体表面的接触角。
2 结果与讨论
2.1 红外光谱分析
分别测试原料KH570、纳米SiO2及产物改性纳米SiO2的红外光谱图, 如图2所示。图中a、 b、 c分别为KH570、 纳米SiO2和改性纳米SiO2的红外光谱, 其中2 927、 2 849 cm-1处为—CH3不对称伸缩振动峰, 3 430 cm-1处为—OH伸缩振动峰,1 735 cm-1处为硅烷偶联剂的—C![]() O的振动峰。由a、c可知,改性后的纳米SiO2出现了KH560的特征峰。由b、c可知,改性纳米SiO2的羟基峰比未改性的强度减弱。经分析,有机基团成功嫁接到纳米SiO2颗粒表面。
O的振动峰。由a、c可知,改性后的纳米SiO2出现了KH560的特征峰。由b、c可知,改性纳米SiO2的羟基峰比未改性的强度减弱。经分析,有机基团成功嫁接到纳米SiO2颗粒表面。
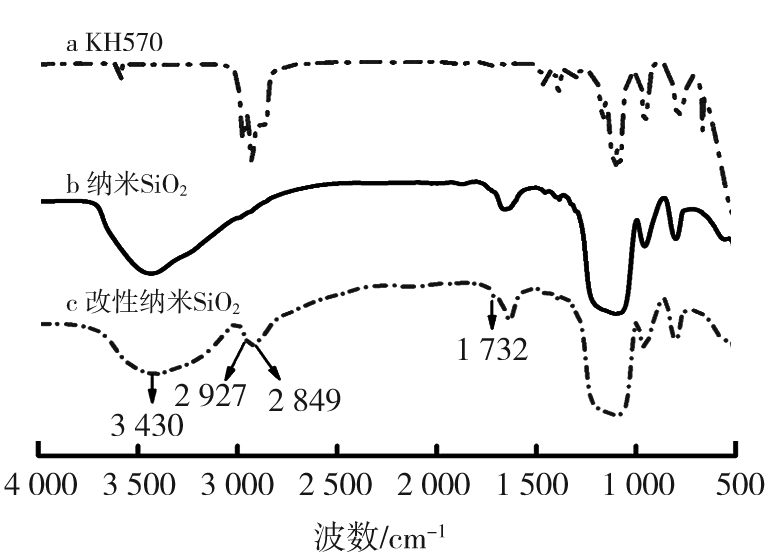
图2 KH570改性纳米SiO2红外光谱谱图
Fig.2 Infrared spectroscopy of nano-SiO2
modified by KH570
2.2 扫描电镜分析
分别测试了市面购置的未改性纳米SiO2及改性纳米SiO2的扫描电镜图像,表征其外观形貌和分散程度,其扫描电镜图像如图3所示。
从SEM图像中可以看出,市面购置的未改性纳米SiO2颗粒粒径由小到大分散不均,团聚现象非常严重,成簇状存在,且颗粒表面不光滑,会极大影响纳米效应的发挥。而对由改进Stöber法合成的纳米SiO2进行一步原位脱醇缩合改性后,颗粒形貌均匀,呈现规则的球状分布, 分散性良好,团聚程度较市面购置的纳米SiO2大幅减弱,这是由于采用脱醇缩合法改性纳米SiO2进程简便,减少了硅烷偶联剂的水解、缩合等中间过程,反应一步到位,保证了有机基团的接枝率。同时纳米SiO2疏水链在有机反应介质中能很好地伸展,阻碍了团聚。该方法制备出的纳米SiO2有利于在各类聚合物基材料中的分散,因此对其进行进一步深入研究。

a 市购纳米SiO2

b 改性纳米SiO2
图3 纳米SiO2扫描电镜图像
Fig.3 SEM images of nano-SiO2
2.3 粒度分析
采用激光粒度分析仪对改性后的纳米SiO2的粒度分布进行分析的结果如图4所示,可以看出改性纳米SiO2粒径约为50 nm,粒度分布较窄,说明制备出的改性纳米SiO2粒度比较均匀。

图4 改性纳米SiO2的粒度分布
Fig.4 Particle size distribution of modified nano-SiO2
2.4 工艺参数优化
以改性纳米SiO2的亲油化度及吸水率作为疏水指标,探究最佳的改性剂用量、改性温度和改性时间等工艺参数。工艺参数对亲油化度和吸水率的影响如图5所示。
2.4.1 改性剂用量
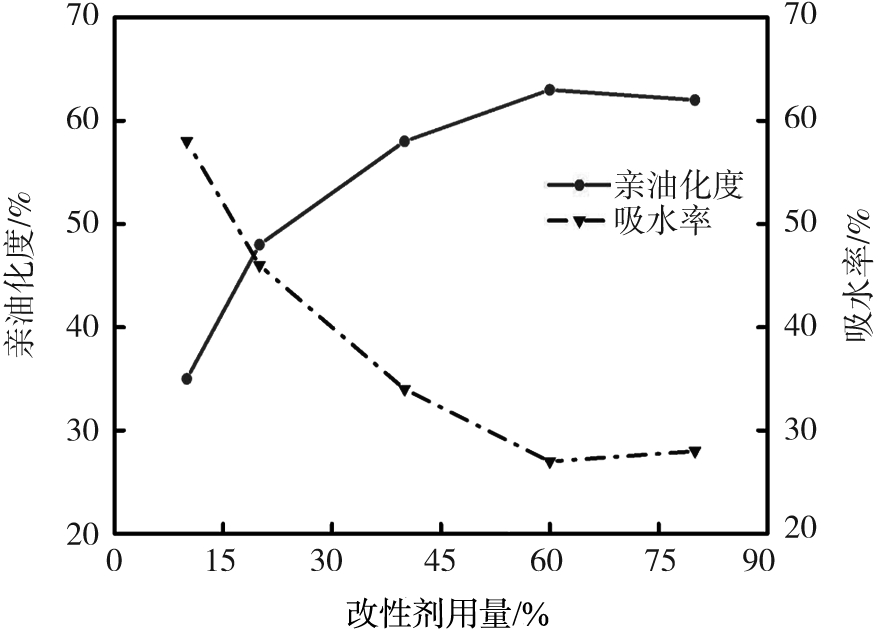
选取改性剂用量依次为10%、20%、40%、60%和80%,分别测试亲油化度和吸水率。改性剂用量的影响如图5a所示。
由图5a可知,随改性剂用量的增加,改性纳米SiO2的亲油化度增大,吸水率减小,浓度超过60%后趋于稳定,此时亲油化度为62%,吸水率为28%。浓度在60%范围内,接枝率随改性剂用量的增加而增大,用量超过60%后因空间位阻效应导致接枝率变化不明显,甚至略有减小[15]。综上所述,KH570对纳米SiO2的改性增强了纳米SiO2的疏水性,在改性剂浓度为60%时,疏水效果最好。
2.4.2 改性温度
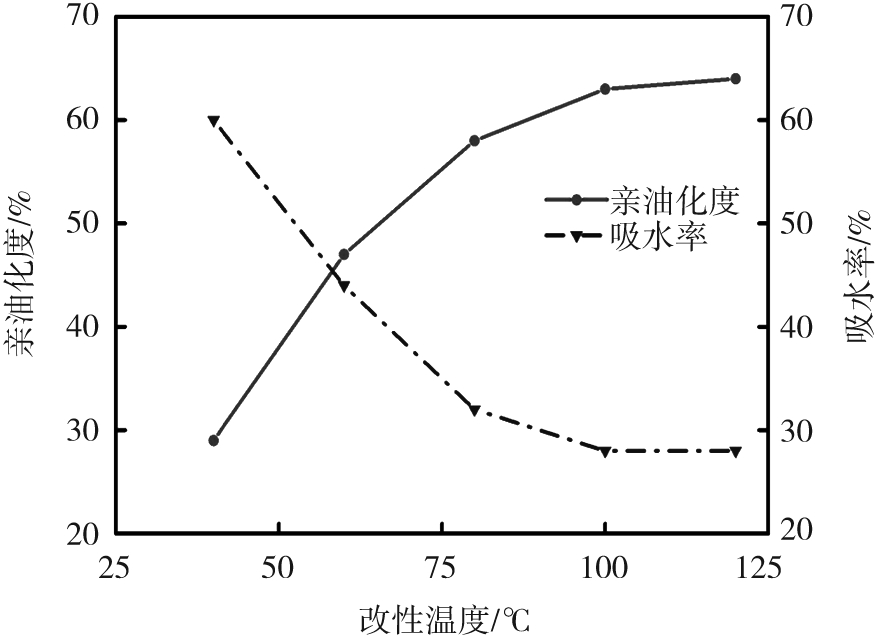
选取改性温度依次为40、60、80、100、120 ℃,分别测试亲油化度和吸水率,影响结果如图5b所示。
从图5b可看出,随改性温度的提高,改性后纳米SiO2的亲油化度增大,吸水率减小,超过100 ℃后趋于稳定,原因是温度过低时,不能提供充足的能量致使反应不完全;温度过高时,反应速率急剧提高,反应热来不及散出,导致颗粒团聚严重。综上所述,在改性温度为100 ℃时,疏水效果最好。
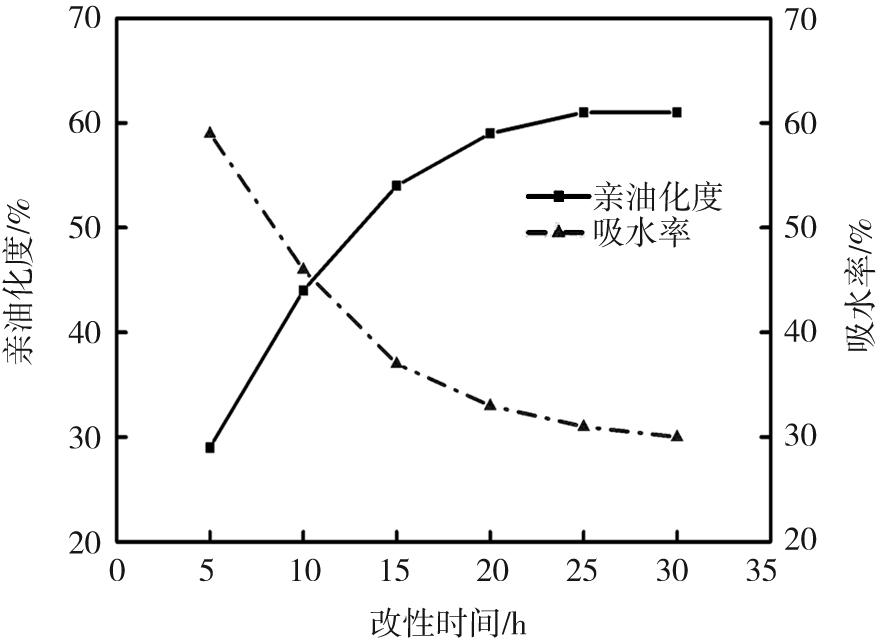
2.4.3 改性时间
选取改性时间依次为5、 10、 15、 20、 25 h, 分别测试亲油化度和吸水率, 影响结果如图5c所示。 由图5c可知, 随改性时间的增加, 改性后纳米SiO2的亲油化度增大, 吸水率减小, 超过25 h后趋于稳定。 由于改性时间过短时, 有机链的接枝不完全, 改性时间过长时, 接枝已达到饱和, 继续增加时间不仅改性效果不明显而且造成能源的浪费, 因此, 在改性时间为25 h时, 疏水效果最好。
a 改性剂用量
b 改性温度
c 改性时间
图5 工艺参数对亲油化度和吸水率的影响
Fig.5 Influence of technological parameters on oil-wet
coefficent and bibulous rate
2.5 疏水效果评价
2.5.1 分散性测试
将改性纳米SiO2粉体超声分散于水及甲苯中,其溶解情况如图6所示。
图6a、6b反映了未改性及改性纳米SiO2在水中的分散情况,未改性纳米SiO2能很好地分散于水中形成均匀的悬浮液,而改性后的纳米SiO2难以分散,在水表面形成一层难溶的粉末膜,说明有机基团包裹于纳米SiO2表面,使其获得了良好的疏水性。图6b、6c反映了改性纳米SiO2在水及甲苯中的分散情况,改性后纳米SiO2由亲水性转变为疏水性,能较好地被甲苯润湿,因此通过表面改性能使纳米SiO2在甲苯中均匀分散,进而能提高在聚合物基质中的分散性。
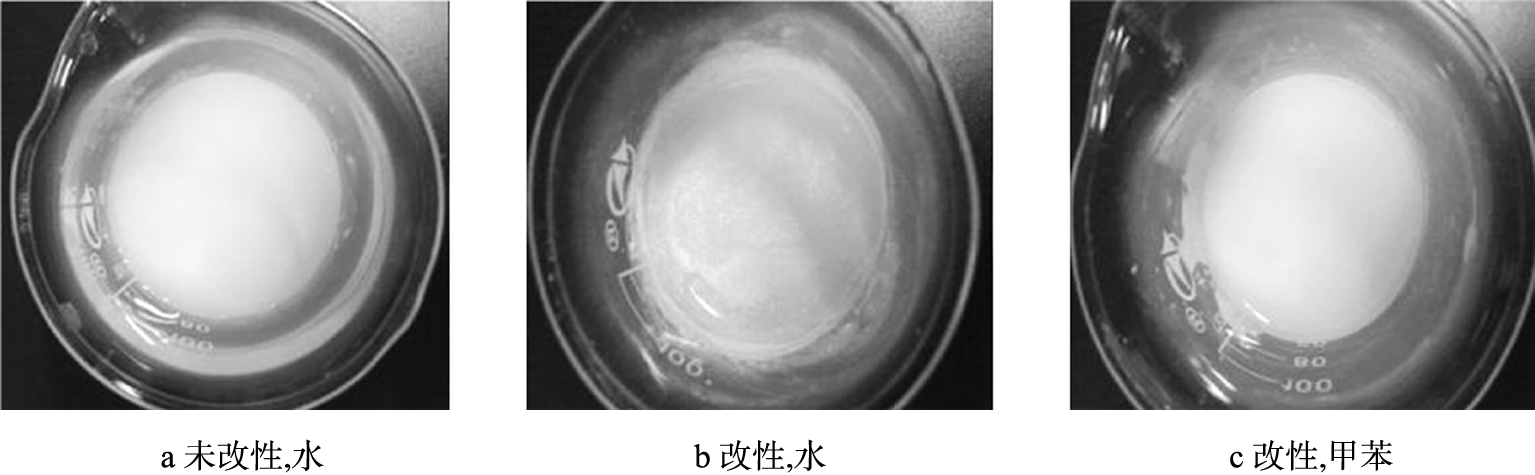
图6 纳米SiO2在水和甲苯中的分散情况
Fig.6 Dispersion of nano silica in water and toluene
2.5.2 沉降实验
对改性后的纳米SiO2进行在石蜡中的沉降实验,结果如图7所示,分别表征了改性剂浓度依次为20%、40%、60%、80%时、不同时间对改性纳米SiO2在石蜡中的沉降体积的影响。随着改性剂浓度的增加,沉降体积减小,沉降速率变慢,在石蜡中的稳定时间增长。其中当KH570浓度为20%时,50 d内纳米SiO2的沉降体积为23 mL;当KH570浓度为80%时,50 d内纳米SiO2的沉降体积仅为7.5 mL,且最终在石蜡液中稳定时间达一年以上。由此可以得出,随改性剂浓度的增加,改性纳米SiO2能够逐渐稳定存在于有机介质中。
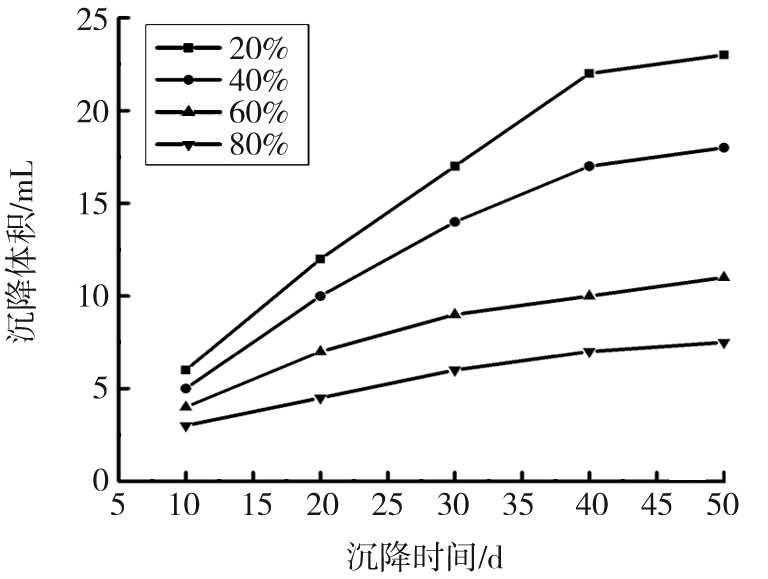
图7 纳米SiO2在石蜡中的沉降实验
Fig.7 Settlement test of nano-silica in paraffin
2.5.3 润湿测试
改性前后的接触角变化能够直观地反映表面性质的变化,接触角越大则表明疏水性越强,测试结果如图8所示。
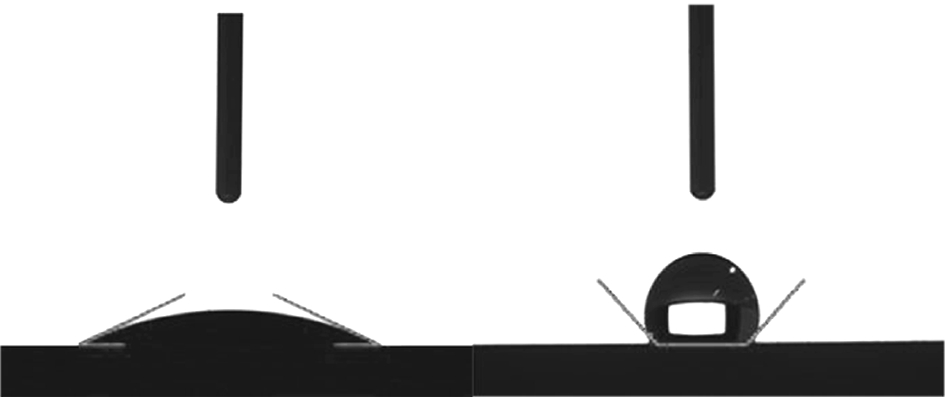
a 改性前 b 改性后
图8 改性前后纳米SiO2的接触角
Fig.8 Contact angle of unmodified and modified nano-SiO2
润湿性测试结果表明,水滴在未改性的纳米SiO2圆片表面铺展,此时接触角为23.1 °,经KH570表面改性后,水滴在改性纳米SiO2圆片表面拱起成球形,此时接触角增加至129.8 °。说明改性纳米SiO2表面被有机基团包裹,削弱了纳米SiO2的极性,表面能降低,润湿性由强亲水性转变为强疏水性。另一方面,纳米SiO2表面粗糙度由于基团的接枝增加,在一定程度下表面越粗糙,材料疏水性越强[16-17],因此若将其添加到聚合物基材料中,将能减弱界面间的作用,形成稳定的聚合物-纳米复合材料,这对于提高聚合物的机械性能,增强材料使用寿命,扩大在各领域的应用具有重要意义。
3 结论
1)利用硅烷偶联剂KH570采用脱醇缩合原理原位改性纳米SiO2制备出的球状纳米SiO2颗粒,颗粒形态规则,分散均匀,粒度约为50 nm。
2)通过优化工艺参数后得出:最佳改性剂浓度为60%,最佳改性温度为100 ℃,最佳改性时间为25 h;改性后纳米SiO2吸水率能有效减小至28%,亲油化度增大至62%。
3)从分散性测试、沉降实验和润湿性测试3方面评价了改性纳米SiO2的疏水效果。 改性后纳米SiO2分散性显著增强, 在石蜡中的沉降速率变慢, 其中由80%浓度的KH570改性的纳米SiO2能稳定存在1年以上, 接触角由23.1 °增大至129.8 °, 由强亲水性转变为强疏水性。
[1]席旻龙, 张幼维. 气相法二氧化硅疏水处理剂用量对液体硅橡胶性能的影响[J]. 有机硅材料, 2017, 31(1):33-35.
[2]SI Y F, GUO Z G. Superwetting materials of oil-water emulsion separation[J]. Chemistry Letters, 2015, 44(7): 874-883.
[3]WANG X, WANG P, JIANG Y, et al. Facile surface modification of silica nanoparticles with a combination of noncovalent and covalent methods for composites application[J]. Composites Science & Technology, 2014,15(104):1-8.
[4]储艳兰,张凯. 纳米二氧化硅的研究现状与进展[J]. 赤峰学院学报(自然科学版), 2013, 29(5):122-123.
[5]GHADIMI A, MOHAMMADI T, KASIRI N. A novel chemical surface modification for the fabrication of PEBA/SiO2 nanocomposite membranes to separate CO2 from syngas and natural gas streams[J]. Industrial & Engineering Chemistry Research, 2014, 53(44): 17476-17486.
[6]LIN Y F, ZHANG A Q, SUN J N, et al. Properties of natural rubber vulcanizates/nanosilica composites prepared based on the method of in-situ generation and coagulation[J]. Journal of Macromolecular Science, Part B, 2013, 52(11): 1494-1507.
[7]公绪强, 王雅祺, 张利, 等. 改性纳米二氧化硅增强增韧聚对苯二甲酸丁二醇酯[J]. 材料导报, 2016, 30(4):52-56.
[8]周鑫, 杨飞, 李传宪, 等. 无机纳米SiO2的表面改性研究[J]. 化工新型材料, 2015, 43(2):167-170.
[9]陈凯玲, 赵蕴慧, 袁晓燕. 二氧化硅粒子的表面化学修饰:方法、 原理及应用[J]. 化学进展, 2013, 25(1):95-104.
[10]何淑婷, 刘宝春. 纳米SiO2的表面改性[J]. 应用化工, 2017, 46(4):693-697.
[11]BURGEAT-LAMI E, ESPIARD P, GUYOT P A. Ethyl acrylate latexes encapsulating nanoparticles of silica:1. functionalization and dispersion of silica[J]. Polymer, 1995, 36(23):4385-4389.
[12]ZHOU X C, ZHONG L P, XU Y P. Surface modification of silica aerogels with trimethylchlorosilane in the ambient pressure drying[J]. Inorganic Materials, 2008, 44(9):976-979.
[13]武江红, 杜志平, 台秀梅. 偶联剂改性纳米SiO2的制备与表征[J]. 印染助剂, 2013, 30(7):11-13.
[14]SHIN Y, LEE D, LEE K, et al. Surface properties of silica nanoparticles modified with polymers for polymer nanocomposite applications[J]. Journal of Industrial and Engineering Chemistry, 2008, 14(4):515-519.
[15]任小明, 赵辉, 朱妍娇, 等. 纳米二氧化硅粒子的改性研究[J]. 湖北大学学报(自然科学版), 2016, 38(6):522-526.
[16]李小兵, 刘莹. 材料表面润湿性的控制与制备技术[J]. 材料工程,2008, 52(4):74-80.
[17]JIANG L, WANG R, YANG B, et al. Binary cooperative complem-entary nanoscale interfacial materials[J]. Pure and Applied Chemistry, 2000, 72(1/2): 73-81.